В химии и молекулярной физике флуктуационные (или нежесткие ) молекулы — это молекулы , которые подвергаются динамике, при которой некоторые или все их атомы обмениваются между эквивалентными по симметрии позициями. [1] Поскольку практически все молекулы являются флуктуационными в некоторых отношениях, например, вращения связей в большинстве органических соединений , термин флуктуационный зависит от контекста и метода, используемого для оценки динамики. Часто молекула считается флуктуационной, если ее спектроскопическая сигнатура демонстрирует уширение линий (за пределами того, что диктуется принципом неопределенности Гейзенберга ) из-за химического обмена. [2] В некоторых случаях, когда скорости медленные, флуктуальность обнаруживается не спектроскопически, а с помощью изотопной маркировки и других методов. [3]
Многие металлоорганические соединения проявляют флюксионность. [4] Однако флюксионность распространена повсеместно.
Температурно-зависимые изменения в спектрах ЯМР являются результатом динамики, связанной с флюкциональными молекулами, когда эта динамика происходит со скоростями, сопоставимыми с разностями частот, наблюдаемыми с помощью ЯМР. Эксперимент называется DNMR и обычно включает в себя регистрацию спектров при различных температурах. В идеальном случае низкотемпературные спектры можно отнести к «пределу медленного обмена», тогда как спектры, зарегистрированные при более высоких температурах, соответствуют молекулам при «пределе быстрого обмена». Как правило, высокотемпературные спектры проще, чем те, которые зарегистрированы при низких температурах, поскольку при высоких температурах эквивалентные участки усредняются. До появления DNMR кинетика реакций измерялась на неравновесных смесях, отслеживая приближение к равновесию.
Многие молекулярные процессы демонстрируют текучесть, которую можно исследовать на шкале времени ЯМР. [5] Помимо примеров, выделенных ниже, другие классические примеры включают перегруппировку Коупа в буллвалене и инверсию кресла в циклогексане .
Для процессов, которые слишком медленные для традиционного анализа DNMR, применима техника спинового насыщения переноса (SST, также называемая EXSY для обменной спектроскопии). Эта техника переноса намагниченности дает информацию о скорости, при условии, что скорости превышают 1/ T 1 . [6]
Хотя это встречается реже, некоторая динамика также наблюдается в масштабе времени ИК-спектроскопии . Одним из примеров является перенос электронов в димере смешанной валентности металлических кластеров . Применение уравнения для коалесценции двух сигналов, разделенных на 10 см −1, дает следующий результат: [7]
Очевидно, что процессы, вызывающие уширение линий в ИК-шкале времени, должны быть намного быстрее, чем процессы, вызывающие обмен в шкале времени ЯМР.
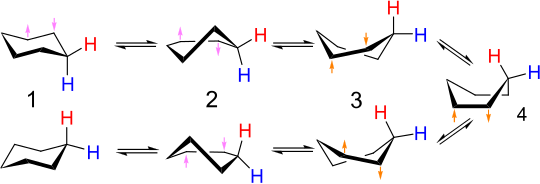
Взаимное превращение эквивалентных конформеров стульев циклогексана (и многих других циклических соединений) называется переворотом кольца . Связи углерода и водорода, которые являются аксиальными в одной конфигурации, становятся экваториальными в другой, и наоборот. При комнатной температуре две конформации стульев быстро уравновешиваются . Спектры ЯМР протона и углерода-13 циклогексана показывают только синглеты вблизи комнатной температуры. При низких температурах синглет в спектре ЯМР 1 H декалесцирует, но спектр ЯМР 13 C остается неизменным. [9]

Прототипической флюксионной молекулой является пентафторид фосфора . Его спектр ЯМР 19 F состоит из дублета, связанного с 31 P, что указывает на то, что экваториальные и аксиальные центры фтора быстро меняются местами в шкале времени ЯМР. Спектроскопия ЯМР фтора-19 даже при температурах до -100 °C не позволяет отличить аксиальное и экваториальное окружение фтора. Кажущаяся эквивалентность возникает из-за низкого барьера для псевдовращения через механизм Берри , посредством которого аксиальные и экваториальные атомы фтора быстро меняются положениями. [10] Пентакарбонил железа (Fe(CO) 5 ) следует шаблону, установленному для PF 5 : в спектре ЯМР 13 C вблизи комнатной температуры наблюдается только один сигнал ), тогда как при низких температурах можно разрешить два сигнала в соотношении 2:3. В тетрафториде серы (SF4 ) наблюдается аналогичная картина, хотя это соединение имеет всего четыре лиганда.
Хорошо изученным флюксионным ионом является ион метания CH+
5. [11] Даже при абсолютном нуле нет жесткой молекулярной структуры; атомы H всегда находятся в движении. Точнее, пространственное распределение протонов в CH+
5во много раз шире, чем его родительская молекула CH 4 , метан. [12] [13]
В то время как нежесткость обычна для пентакоординированных видов, шестикоординированные виды обычно принимают более жесткую октаэдрическую молекулярную геометрию , характеризующуюся плотноупакованным массивом из шести лигирующих атомов, окружающих центральный атом. Такие соединения перестраиваются внутримолекулярно через скручивание Рэя-Датта и скручивание Байлара , но барьеры для этих процессов обычно высоки, так что эти процессы не приводят к уширению линий. Для некоторых соединений динамика происходит через диссоциацию лиганда, давая пентакоординированный промежуточный продукт, который подчиняется механизмам, обсуждаемым выше. Еще один механизм, демонстрируемый Fe(CO) 4 (SiMe 3 ) 2 и связанными с ним гидридными комплексами, представляет собой внутримолекулярную скремблировку лигандов по граням тетраэдра, определяемого четырьмя лигандами CO. [14]
Классическим примером флюктуационной молекулы является диметилформамид (ДМФ). [15]

При температурах около 100 °C спектр ЯМР 1 H 500 МГц ДМФ показывает только один сигнал для метильных групп. Однако вблизи комнатной температуры видны отдельные сигналы для неэквивалентных метильных групп. Скорость обмена можно рассчитать при температуре, при которой два сигнала просто сливаются. Эта «температура коалесценции» зависит от измерительного поля. Соответствующее уравнение имеет вид
где Δν 0 — разность частот (в Гц) обменивающихся участков. Эти частоты получены из предельного низкотемпературного спектра ЯМР. При этих более низких температурах динамика, конечно, продолжается, но вклад динамики в уширение линии незначителен.
Например, если Δν 0 = 1ppm при 500 МГц,
Соединение Fe(η 5 -C 5 H 5 )(η 1 -C 5 H 5 )(CO) 2 проявляет явление «кольцевого свиста».
При 30 °C спектр 1 H ЯМР показывает только два пика, один типичный (δ5,6) для η 5 -C 5 H 5 и другой, приписанный η 1 -C 5 H 5 . Синглет, приписанный лиганду η 1 -C 5 H 5 , расщепляется при низких температурах из-за медленного перескока центра Fe с углерода на углерод в лиганде η 1 -C 5 H 5 . [16] Было предложено два механизма, при этом консенсус в пользу пути сдвига 1,2 . [17]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )