
Атомный радиус химического элемента является мерой размера его атома , обычно это среднее или типичное расстояние от центра ядра до самого удаленного изолированного электрона . Поскольку граница не является четко определенным физическим объектом, существуют различные неэквивалентные определения атомного радиуса. Четыре широко используемых определения атомного радиуса: радиус Ван-дер-Ваальса , ионный радиус , металлический радиус и ковалентный радиус . Обычно из-за сложности выделения атомов для отдельного измерения их радиусов атомный радиус измеряется в химически связанном состоянии; однако теоретические расчеты проще, если рассматривать атомы изолированно. Зависимости от среды, зонда и состояния приводят к множеству определений.
В зависимости от определения этот термин может применяться к атомам в конденсированном веществе , ковалентно связанным в молекулах или в ионизированном и возбужденном состояниях ; и его значение может быть получено посредством экспериментальных измерений или вычислено на основе теоретических моделей. Значение радиуса может зависеть от состояния атома и контекста. [1]
Электроны не имеют ни определенных орбит, ни четко определенных пробегов. Скорее, их положения следует описывать как распределения вероятностей , которые постепенно сужаются по мере удаления от ядра, без резкого обрезания; их называют атомными орбиталями или электронными облаками. Более того, в конденсированном состоянии и молекулах электронные облака атомов обычно в некоторой степени перекрываются, и часть электронов может перемещаться по большой области, охватывающей два или более атомов.
Согласно большинству определений радиусы изолированных нейтральных атомов колеблются от 30 до 300 пм ( триллионные доли метра) или от 0,3 до 3 ангстрем . Следовательно, радиус атома более чем в 10 000 раз превышает радиус его ядра (1–10 фм ) [2] и менее 1/1000 длины волны видимого света (400–700 нм ).
Для многих целей атомы можно моделировать как сферы. Это лишь грубое приближение, но оно может дать количественные объяснения и предсказания многих явлений, таких как плотность жидкостей и твердых тел, диффузия жидкостей через молекулярные сита , расположение атомов и ионов в кристаллах , а также размер и форма. молекул . [ нужна цитата ]
В 1920 году, вскоре после того, как стало возможным определять размеры атомов с помощью рентгеновской кристаллографии , было высказано предположение, что все атомы одного и того же элемента имеют одинаковые радиусы. [3] Однако в 1923 году, когда стало доступно больше данных о кристаллах, было обнаружено, что приближение атома как сферы не обязательно справедливо при сравнении одного и того же атома в разных кристаллических структурах. [4]
Широко используемые определения атомного радиуса включают:
В следующей таблице показаны эмпирически измеренные ковалентные радиусы элементов, опубликованные Дж. К. Слейтером в 1964 году. [9] Значения указаны в пикометрах (пм или 1×10 -12 м) с точностью около 5 пм. Оттенок поля варьируется от красного до желтого по мере увеличения радиуса; серый цвет указывает на отсутствие данных.
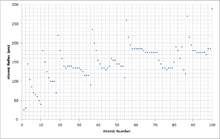
Изменение атомного радиуса с увеличением атомного номера можно объяснить расположением электронов в оболочках фиксированной емкости. Оболочки обычно заполняются в порядке возрастания радиуса, поскольку отрицательно заряженные электроны притягиваются положительно заряженными протонами ядра. По мере увеличения атомного номера в каждой строке таблицы Менделеева дополнительные электроны переходят в ту же самую внешнюю оболочку; радиус которого постепенно сокращается из-за увеличения заряда ядра. У благородного газа внешняя оболочка полностью заполнена; следовательно, дополнительный электрон следующего щелочного металла перейдет в следующую внешнюю оболочку, что приводит к внезапному увеличению атомного радиуса.
Увеличение заряда ядра частично уравновешивается увеличением числа электронов — явление, известное как экранирование ; что объясняет, почему размер атомов обычно увеличивается с каждым столбцом. Однако есть одно заметное исключение, известное как сокращение лантаноидов : блок 5d-элементов намного меньше, чем можно было бы ожидать, из-за слабого экранирования 4f-электронов.
По сути, атомный радиус уменьшается по периодам из-за увеличения числа протонов. Следовательно, между протонами и электронами существует большее притяжение, поскольку противоположные заряды притягиваются, и большее количество протонов создает более сильный заряд. Большее притяжение приближает электроны к протонам, уменьшая размер частицы. Следовательно, атомный радиус уменьшается. Вниз по группам атомный радиус увеличивается. Это связано с тем, что существует больше энергетических уровней и, следовательно, большее расстояние между протонами и электронами. Кроме того, экранирование электронов приводит к уменьшению притяжения, поэтому оставшиеся электроны могут уйти дальше от положительно заряженного ядра. Следовательно, размер или атомный радиус увеличивается.
В следующей таблице суммированы основные явления, влияющие на атомный радиус элемента:
Электроны в подоболочке 4f , которая постепенно заполняется от лантана ( Z = 57) до иттербия ( Z = 70), не особенно эффективно экранируют растущий ядерный заряд от дальнейших подоболочек. Элементы, следующие сразу за лантанидами, имеют атомные радиусы, которые меньше, чем можно было бы ожидать, и почти идентичны атомным радиусам элементов, находящихся непосредственно над ними. [10] Следовательно, лютеций на самом деле немного меньше иттрия , гафний имеет практически тот же атомный радиус (и химический состав), что и цирконий , а тантал имеет атомный радиус, аналогичный ниобию , и так далее. Эффект сжатия лантаноидов заметен вплоть до платины ( Z = 78), после чего он маскируется релятивистским эффектом , известным как эффект инертной пары . [ нужна цитата ]
Из-за сокращения лантаноидов можно сделать 5 следующих наблюдений:
Сокращение d-блока менее выражено, чем сокращение лантаноидов, но возникает по той же причине. В данном случае именно плохая экранирующая способность 3d-электронов влияет на атомные радиусы и химический состав элементов, следующих сразу за первым рядом переходных металлов , от галлия ( Z = 31) до брома ( Z = 35). [10]
В следующей таблице показаны атомные радиусы, рассчитанные на основе теоретических моделей, опубликованных Энрико Клементи и другими в 1967 году . [11] Значения указаны в пикометрах (мкм).