В химии рацемизация — это превращение оптически активного соединения в рацемическую (оптически неактивную) форму под действием тепла или химической реакции. Это создает молярное соотношение энантиомеров 1:1 и называется рацемической смесью (т. е. содержит равное количество (+) и (− ) форм). Плюс- и минус-формы называются правовращающими и левовращающими . [1] D- и L-энантиомеры присутствуют в равных количествах, полученный образец описывается как рацемическая смесь или рацемат. Рацемизация может протекать через ряд различных механизмов, и она имеет особое значение в фармакологии, поскольку различные энантиомеры могут иметь различные фармацевтические эффекты.
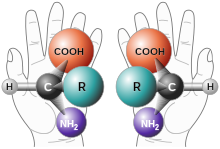
Хиральные молекулы имеют две формы (в каждой точке асимметрии), которые различаются по своим оптическим характеристикам: левовращающая форма ( (−)-форма ) будет вращаться против часовой стрелки в плоскости поляризации луча света, тогда как правовращающая форма ( (+)-форма ) будет вращаться по часовой стрелке в плоскости поляризации луча света. [1] Две формы, которые не являются суперпозитивными при вращении в трехмерном пространстве, называются энантиомерами . Обозначение не следует путать с обозначением молекул D и L , которое относится к сходству по структуре с D -глицеральдегидом и L -глицеральдегидом. Кроме того, ( R )- и ( S )- относятся к химической структуре молекулы, основанной на правилах приоритета Кана-Ингольда-Прелога для наименования, а не на вращении света. Обозначение R/S является основным обозначением, используемым для +/- в настоящее время, поскольку обозначения D и L используются в основном для сахаров и аминокислот. [2]
Рацемизация происходит, когда одна чистая форма энантиомера преобразуется в равное количество обоих энантиомеров, образуя рацемат . Когда есть равное количество правовращающих и левовращающих молекул, чистое оптическое вращение рацемата равно нулю. Энантиомеры также следует отличать от диастереомеров , которые представляют собой тип стереоизомеров, имеющих различные молекулярные структуры вокруг стереоцентра и не являющихся зеркальными отражениями.
Частичная или полная рацемизация стереохимии в растворах является результатом механизмов SN1 . Однако, когда в реакции замещения происходит полная инверсия конфигурации стереохимии , ответственной является реакция SN2 . [3]
В твердом состоянии рацемические смеси могут иметь физические свойства, отличные от свойств любого из чистых энантиомеров из-за дифференциальных межмолекулярных взаимодействий (см. раздел «Биологическое значение»). Изменение чистого энантиомера в рацемат может изменить его плотность, температуру плавления, растворимость, теплоту плавления, показатель преломления и его различные спектры. Кристаллизация рацемата может привести к отдельным (+) и (−) формам или к одному рацемическому соединению. Однако в жидком и газообразном состояниях рацемические смеси будут вести себя с физическими свойствами, которые идентичны или почти идентичны их чистым энантиомерам . [4]
В целом, большинство биохимических реакций являются стереоселективными, поэтому только один стереоизомер будет производить предполагаемый продукт, в то время как другой просто не будет участвовать или может вызывать побочные эффекты. Следует отметить, что L -форма аминокислот и D -форма сахаров (в первую очередь глюкозы) обычно являются биологически реактивной формой. Это связано с тем, что многие биологические молекулы являются хиральными, и, таким образом, реакции между определенными энантиомерами производят чистые стереоизомеры. [5] Также следует отметить тот факт, что все аминокислотные остатки существуют в L- форме. Однако бактерии производят D -аминокислотные остатки, которые полимеризуются в короткие полипептиды, которые можно найти в стенках бактериальных клеток. Эти полипептиды хуже усваиваются пептидазами и синтезируются бактериальными ферментами вместо трансляции мРНК, которая обычно производит L -аминокислоты. [5]
Стереоселективная природа большинства биохимических реакций означает, что разные энантиомеры химического вещества могут иметь разные свойства и эффекты на человека. Многие психотропные препараты демонстрируют различную активность или эффективность между изомерами, например, амфетамин часто выпускается в виде рацемических солей, в то время как более активный декстроамфетамин резервируется для рефрактерных случаев или более серьезных показаний; другим примером является метадон , один изомер которого обладает активностью опиоидного агониста, а другой — антагониста NMDA . [6]
Рацемизация фармацевтических препаратов может происходить in vivo . Талидомид в виде ( R ) энантиомера эффективен против утренней тошноты , в то время как ( S ) энантиомер является тератогенным , вызывая врожденные дефекты при приеме в первом триместре беременности. Если человеку вводят только один энантиомер, обе формы могут быть обнаружены позже в сыворотке крови. [7] Поэтому препарат не считается безопасным для использования женщинами детородного возраста, и хотя он имеет другие применения, его использование строго контролируется. [8] [9] Талидомид может использоваться для лечения множественной миеломы . [10]
Другим часто используемым препаратом является ибупрофен , который является противовоспалительным только в качестве одного энантиомера, в то время как другой биологически инертен. Аналогично, стереоизомер ( S ) гораздо более реактивен, чем энантиомер ( R ) в циталопраме (Celexa), антидепрессанте, который ингибирует обратный захват серотонина, активен. [11] [5] [12] Поэтому конфигурационная стабильность препарата является областью интересов в фармацевтических исследованиях. [13] Производство и анализ энантиомеров в фармацевтической промышленности изучаются в области хирального органического синтеза.
Рацемизация может быть достигнута простым смешиванием равных количеств двух чистых энантиомеров. Рацемизация может также происходить при химическом взаимопревращении. Например, когда ( R )-3-фенил-2- бутанон растворяется в водном этаноле, содержащем NaOH или HCl , образуется рацемат. Рацемизация происходит посредством промежуточной енольной формы, в которой бывший стереоцентр становится плоским и, следовательно, ахиральным. [14] : 373 Входящая группа может приближаться с любой стороны плоскости, поэтому существует равная вероятность того, что протонирование обратно в хиральный кетон даст либо R- , либо S -форму, что приведет к рацемату.
Рацемизация может происходить посредством некоторых из следующих процессов:
Скорость рацемизации (от L -форм до смеси L -форм и D -форм) использовалась как способ датирования биологических образцов в тканях с низкой скоростью оборота, криминалистических образцов и ископаемых в геологических отложениях. Этот метод известен как аминокислотное датирование .
В 1843 году Луи Пастер открыл оптическую активность в паравинной, или рацемической, кислоте, содержащейся в виноградном вине. Он смог разделить два энантиомерных кристалла, которые вращали поляризованный свет в противоположных направлениях. [11]