Реакция сдвига вода -газ (WGSR) описывает реакцию угарного газа и водяного пара с образованием углекислого газа и водорода :
Реакция конверсии водяного газа была открыта итальянским физиком Феличе Фонтана в 1780 году. Лишь намного позже была осознана промышленная ценность этой реакции. До начала 20 века водород получали путем реакции пара под высоким давлением с железом с образованием оксида железа и водорода. С развитием промышленных процессов, требующих водорода, таких как синтез аммиака Габера-Боша , потребовался менее дорогой и более эффективный метод производства водорода . В качестве решения этой проблемы WGSR объединили с газификацией угля для производства водорода.
WGSR — это очень ценная промышленная реакция, которая используется при производстве аммиака, углеводородов , метанола и водорода . Его наиболее важное применение связано с конверсией окиси углерода при паровой конверсии метана или других углеводородов при производстве водорода. [1] В процессе Фишера-Тропша WGSR является одной из наиболее важных реакций, используемых для балансировки соотношения H 2 /CO. Он обеспечивает источник водорода за счет монооксида углерода, что важно для производства водорода высокой чистоты для использования в синтезе аммиака.
Реакция конверсии вода-газ может быть нежелательной побочной реакцией в процессах с участием воды и монооксида углерода, например, в процессе Монсанто на основе родия . В процессе Cativa на основе иридия используется меньше воды, что подавляет эту реакцию.
WGSR может повысить эффективность топливных элементов за счет увеличения производства водорода. WGSR считается важнейшим компонентом снижения концентрации угарного газа в элементах, чувствительных к отравлению угарным газом, таких как топливный элемент с протонообменной мембраной (PEM) . [2] Преимущества этого применения двояки: реакция конверсии водяного газа не только эффективно снизит концентрацию монооксида углерода, но также повысит эффективность топливных элементов за счет увеличения производства водорода. [2] К сожалению, современные коммерческие катализаторы, которые используются в промышленных процессах конверсии водяного газа, несовместимы с топливными элементами. [3] Учитывая высокий спрос на чистое топливо и решающую роль реакции конверсии водяного газа в водородных топливных элементах, разработка катализаторов конверсии водяного газа для применения в технологии топливных элементов является областью текущих исследовательских интересов.
Катализаторы для применения в топливных элементах должны будут работать при низких температурах. Поскольку WGSR происходит медленно при более низких температурах, когда равновесие благоприятствует производству водорода, реакторы WGS требуют большого количества катализаторов, что увеличивает их стоимость и размер, выходящие за рамки практического применения. [2] Коммерческий катализатор LTS, используемый на крупных промышленных предприятиях, также является пирофорным в неактивном состоянии и, следовательно, представляет угрозу безопасности для потребительского применения. [3] Разработка катализатора, способного преодолеть эти ограничения, актуальна для реализации водородной экономики.
Реакция WGS используется в сочетании с твердой адсорбцией CO 2 при конверсии водяного газа с усиленной сорбцией (SEWGS) для получения потока водорода под высоким давлением из синтез-газа . [4]
Равновесие этой реакции существенно зависит от температуры, а константа равновесия уменьшается с повышением температуры, то есть более высокое образование водорода наблюдается при более низких температурах.

С повышением температуры скорость реакции увеличивается, но получение водорода становится менее выгодным термодинамически [5] , поскольку реакция конверсии водяного газа является умеренно экзотермической ; этот сдвиг химического равновесия можно объяснить согласно принципу Ле Шателье . В интервале температур 600–2000 К константа равновесия WGSR имеет следующую зависимость: [3]
Чтобы воспользоваться как термодинамикой , так и кинетикой реакции, реакцию конверсии водяного газа в промышленном масштабе проводят в несколько адиабатических стадий , состоящих из высокотемпературного сдвига (HTS), за которым следует низкотемпературный сдвиг (LTS) с межсистемным охлаждением. [6] Первоначальный HTS использует преимущества высоких скоростей реакции, но приводит к неполной конверсии монооксида углерода. Последующий низкотемпературный реактор конверсии снижает содержание монооксида углерода до <1%. Коммерческие катализаторы HTS основаны на оксиде железа – оксиде хрома , а катализатор LTS – на основе меди. Медный катализатор подвержен отравлению серой . Соединения серы удаляются перед реактором LTS с помощью защитного слоя. Важным ограничением для HTS является соотношение H 2 O/CO, при котором низкие соотношения могут привести к побочным реакциям, таким как образование металлического железа, метанирование , отложение углерода и реакция Фишера-Тропша.
Сообщается, что типичный состав коммерческого катализатора ВТС составляет 74,2% Fe 2 O 3 , 10,0% Cr 2 O 3 , 0,2% MgO (остальный процент относится к летучим компонентам). [7] Хром стабилизирует оксид железа и предотвращает спекание . Работа ВТС-катализаторов происходит в диапазоне температур от 310°С до 450°С. Температура увеличивается по длине реактора из-за экзотермического характера реакции. Таким образом, температура на входе поддерживается на уровне 350 °C, чтобы предотвратить превышение температуры на выходе 550 °C. Промышленные реакторы работают в диапазоне от атмосферного давления до 8375 кПа (82,7 атм). [7] Поиск высокоэффективных катализаторов HT WGS остается интенсивной темой исследований в области химии и материаловедения. Энергия активации является ключевым критерием оценки каталитической эффективности реакций WGS. На сегодняшний день одни из самых низких значений энергии активации были обнаружены для катализаторов, состоящих из наночастиц меди на материалах носителя церия , [8] с такими низкими значениями, как Ea = 34 кДж / моль, относительно генерации водорода.
Катализаторы для низкотемпературной реакции WGS обычно основаны на керамических фазах, нагруженных медью или оксидом меди. Хотя наиболее распространенные носители включают оксид алюминия или оксид алюминия с оксидом цинка, другие носители могут включать оксиды редкоземельных элементов, шпинели или перовскиты. [9] Типичный состав коммерческого катализатора LTS составляет 32-33% CuO, 34-53% ZnO, 15-33% Al 2 O 3 . [3] Активным каталитическим компонентом является CuO. Функция ZnO — обеспечить структурную поддержку, а также предотвратить отравление меди серой. Al 2 O 3 предотвращает диспергирование и усадку гранул. Реактор конверсии LTS работает в диапазоне 200–250 °C. Верхний температурный предел обусловлен склонностью меди к термическому спеканию. Эти более низкие температуры также уменьшают возникновение побочных реакций, которые наблюдаются в случае ВТС. Благородные металлы, такие как платина, нанесенная на церий, также использовались для LTS. [10]
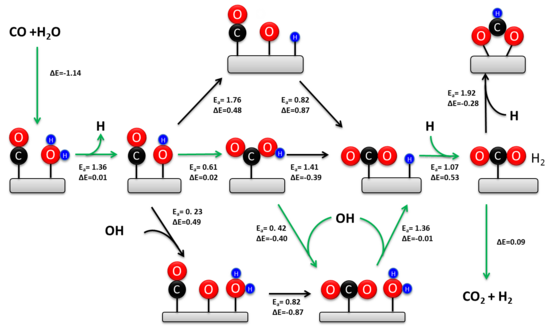
WGSR тщательно изучается уже более ста лет. Кинетически значимый механизм зависит от состава катализатора и температуры. [6] [14] Было предложено два механизма: ассоциативный механизм Ленгмюра-Хиншелвуда и окислительно-восстановительный механизм. Окислительно-восстановительный механизм обычно считается кинетически значимым во время высокотемпературного WGSR (> 350 ° C) на промышленном железохромовом катализаторе. [5] Исторически сложилось так, что вокруг механизма при низких температурах было гораздо больше споров. Недавние экспериментальные исследования подтверждают, что ассоциативный карбоксильный механизм является преобладающим низкотемпературным путем в катализаторах переходных металлов на носителе из оксидов металлов. [15] [13]
В 1920 году Армстронг и Хилдич впервые предложили ассоциативный механизм. В этом механизме CO и H 2 O адсорбируются на поверхности катализатора с последующим образованием интермедиата и десорбцией H 2 и CO 2 . Обычно H 2 O диссоциирует на катализаторе с образованием адсорбированных OH и H. Диссоциированная вода реагирует с CO с образованием промежуточного карбоксила или формиата. Промежуточное соединение впоследствии дегидрируется с образованием CO 2 и адсорбированного H. Два адсорбированных атома H рекомбинируются с образованием H 2 .
Вокруг кинетически значимого промежуточного соединения в ходе ассоциативного механизма ведутся серьезные разногласия. Экспериментальные исследования показывают, что оба промежуточных продукта способствуют скорости реакции на катализаторах переходных металлов, нанесенных на оксиды металлов. [15] [13] Однако карбоксильный путь составляет около 90% от общей скорости из-за термодинамической стабильности адсорбированного формиата на оксидном носителе. Активный центр образования карбоксила состоит из атома металла, примыкающего к адсорбированному гидроксилу. Этот ансамбль легко формируется на границе раздела металл-оксид и объясняет гораздо более высокую активность переходных металлов, нанесенных на оксиды, по сравнению с протяженными металлическими поверхностями. [13] Частота оборотов WGSR пропорциональна константе равновесия образования гидроксила, что объясняет, почему восстанавливаемые оксидные носители (например, CeO 2 ) более активны, чем невосстанавливаемые носители (например, SiO 2 ) и протяженные металлические поверхности (например, Пт). В отличие от активного центра образования карбоксила, образование формиата происходит на протяженных металлических поверхностях. Формиат-промежуточное соединение можно удалить во время WGSR с помощью атомно-дисперсных катализаторов переходных металлов на оксидном носителе, что еще раз подтверждает кинетическое доминирование карбоксильного пути. [16]
Окислительно-восстановительный механизм включает изменение степени окисления каталитического материала. В этом механизме CO окисляется атомом О, присущим каталитическому материалу, с образованием CO 2 . Молекула воды подвергается диссоциативной адсорбции на вновь образовавшейся О-вакансии с образованием двух гидроксилов. Гидроксилы диспропорционируются, образуя H 2 и возвращая каталитическую поверхность обратно в ее предреакционное состояние.
Механизм включает нуклеофильную атаку воды или гидроксида на центр M-CO с образованием металлокарбоновой кислоты . [2] [17]
WGSR является экзергоническим , со следующими термодинамическими параметрами при комнатной температуре (298 К):
В водном растворе реакция менее экзергонична. [18]
При преобразовании диоксида углерода в полезные материалы реакция конверсии вода-газ используется для получения монооксида углерода из водорода и диоксида углерода. Иногда это называют обратной реакцией конверсии воды и газа . [19]
Водяной газ определяется как топливный газ, состоящий в основном из оксида углерода (CO) и водорода (H 2 ). Термин «сдвиг» в водогазовом сдвиге означает изменение соотношения состава водяного газа (CO:H 2 ). Соотношение можно увеличить путем добавления CO 2 или уменьшить путем добавления в реактор пара.