Рифамицины — это группа антибиотиков , которые синтезируются либо естественным образом бактерией Amycolatopsis rifamycinica , либо искусственно. Они являются подклассом более крупного семейства ансамицинов . Рифамицины особенно эффективны против микобактерий и поэтому используются для лечения туберкулеза , проказы и инфекций комплекса Mycobacterium avium (MAC).
Группа рифамицина включает классические препараты рифамицина, а также производные рифамицина рифампицин ( или рифампин), рифабутин , рифапентин , рифалазил и рифаксимин . Рифамицин, продаваемый под торговым названием Aemcolo, одобрен в Соединенных Штатах для лечения диареи путешественников в некоторых случаях. [1] [2] [3]
Название «рифамицин» (первоначально «рифомицин») произошло от французского фильма 1955 года «Рифифи» . [4] : S402
Streptomyces mediterranei был впервые выделен в 1957 году из образца почвы, собранного недалеко от прибрежного города Сен-Рафаэль на юге Франции. Название было первоначально дано двумя микробиологами, работающими с итальянской фармацевтической компанией Group Lepetit SpA в Милане , итальянкой Грацией Береттой и Пинхасом Маргалитом из Израиля. [5]
В 1969 году бактерия была переименована в Nocardia mediterranei , когда другой ученый по имени Тиманн обнаружил, что у нее типичная для вида Nocardia клеточная стенка . Затем, в 1986 году, бактерия была снова переименована в Amycolatopsis mediterranei , как первый вид нового рода, потому что ученый по имени Лешевалье обнаружил, что в клеточной стенке отсутствует миколовая кислота , и она не может быть инфицирована фагами Nocardia и Rhodococcus. Основываясь на последовательностях рибосомальной РНК 16S , Бала и др. переименовали вид в 2004 году в Amycolatopsis rifamycinica .
Рифамицины были впервые выделены в 1957 году из ферментационной культуры Streptomyces mediterranei в лаборатории Gruppo Lepetit SpA в Милане двумя учеными Пьеро Сенси и Марией Терезой Тимбал, работавшими с израильским ученым Пинхасом Маргалитом. Первоначально было обнаружено семейство близкородственных антибиотиков, названных рифамицинами A, B, C, D, E. Единственным компонентом этой смеси, достаточно стабильным для выделения в чистом виде, был рифамицин B, который, к сожалению, был слабо активен. Однако дальнейшие исследования показали, что, хотя рифамицин B был по существу неактивен, он спонтанно окислялся и гидролизовался в водных растворах, давая высокоактивный рифамицин S. Простое восстановление рифамицина S дало гидрохиноновую форму, названную рифамицином SV, которая стала первым членом этого класса, вошедшим в клиническое применение в качестве внутривенного антибиотика. Дальнейшая химическая модификация Рифамицина SV дала улучшенный аналог Рифамид, который также был введен в клиническую практику, но был также ограничен внутривенным применением. После обширной программы модификаций в конечном итоге был произведен Рифампин, который доступен для приема внутрь и стал основой терапии туберкулеза [4]
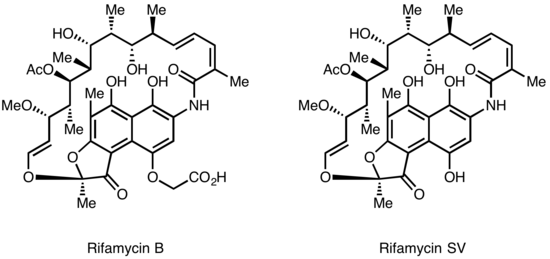
Лепетит подал заявку на патентную защиту рифамицина В в Великобритании в августе 1958 года и в США в марте 1959 года. Британский патент GB921045 был выдан в марте 1963 года, а патент США 3 150 046 был выдан в сентябре 1964 года. Широко распространено мнение, что этот препарат помог победить проблему лекарственно-устойчивого туберкулеза в 1960-х годах.
Рифамицины использовались для лечения многих заболеваний, наиболее важным из которых является туберкулез, связанный с ВИЧ. Систематический обзор клинических испытаний альтернативных схем профилактики активного туберкулеза у ВИЧ-отрицательных лиц с латентным туберкулезом показал, что еженедельный, непосредственно наблюдаемый режим рифапентина с изониазидом в течение трех месяцев был таким же эффективным, как ежедневный, самостоятельный режим изониазида в течение девяти месяцев. Но режим рифапентина-изониазида имел более высокие показатели завершения лечения и более низкие показатели гепатотоксичности . Однако частота побочных эффектов, ограничивающих лечение, была выше в режиме рифапентина-изониазида. [6]
Рифамицины обладают уникальным механизмом действия, селективно ингибируя бактериальную ДНК-зависимую РНК-полимеразу , и не проявляют перекрестной резистентности с другими антибиотиками при клиническом использовании. Однако, несмотря на их активность против бактерий, устойчивых к другим антибиотикам , сами рифамицины страдают от довольно высокой частоты резистентности. Из-за этого рифампин и другие рифамицины обычно используются в сочетании с другими антибактериальными препаратами. Это обычно практикуется в терапии туберкулеза и служит для предотвращения образования мутантов, устойчивых к любому из препаратов в комбинации. Рифампин быстро убивает быстро делящиеся штаммы бацилл, а также «персистерные» клетки, которые остаются биологически неактивными в течение длительных периодов времени, что позволяет им избегать действия антибиотиков. [7] Кроме того, рифабутин и рифапентин оба использовались против туберкулеза, приобретенного у ВИЧ-инфицированных пациентов. Хотя терапия туберкулеза остается наиболее важным применением рифампина, растущая проблема серьезных инфекций с множественной лекарственной устойчивостью привела к использованию для их лечения комбинаций антибиотиков, содержащих рифампицин.
Антибактериальная активность рифамицинов основана на ингибировании синтеза бактериальной ДНК-зависимой РНК. [8] Это связано с высоким сродством рифамицинов к прокариотической РНК-полимеразе . Селективность рифамицинов зависит от того факта, что они имеют очень слабое сродство к аналогичному ферменту млекопитающих. Данные о кристаллической структуре антибиотика, связанного с РНК-полимеразой, указывают на то, что рифамицин блокирует синтез, вызывая сильные стерические столкновения с растущим олигонуклеотидом (механизм «стерической окклюзии»). [9] [10] Если рифамицин связывается с полимеразой после начала процесса удлинения цепи, ингибирования биосинтеза не наблюдается, что соответствует механизму стерической окклюзии. Одношаговая резистентность высокого уровня к рифамицинам возникает в результате изменения одной аминокислоты в бактериальной ДНК-зависимой РНК-полимеразе.
Первая информация о биосинтезе рифамицинов была получена из исследований с использованием стабильного изотопа углерода-13 и ЯМР-спектроскопии для установления происхождения углеродного скелета. Эти исследования показали, что цепь анса произошла из ацетата и пропионата , как и у других поликетидных антибиотиков. Было показано, что нафталиновый хромофор произошел из пропионатной единицы, связанной с семиуглеродной аминогруппой неизвестного происхождения. Общая схема биосинтеза начинается с необычной исходной единицы, 3-амино-5-гидроксибензойной кислоты ( AHBA ), через поликетидный путь типа I ( PKS I ), в котором удлинение цепи осуществляется с использованием 2 ацетатных и 8 пропионатных единиц. [11] Считается, что AHBA произошел из пути Шикимата , однако это не было включено в биосинтетический механизм. Это связано с наблюдением, что 3 аналога аминокислот превращаются в AHBA в бесклеточных экстрактах A. mediterranei . [12]
Кластер rif отвечает за биосинтез рифамицинов. Он содержит гены rifG через rifN , которые, как было показано, биосинтезируют AHBA.[10] Считается, что RifK , rifL , rifM и rifN действуют как трансаминазы для образования предшественника AHBA канозамина. [13] [14] «RifH» кодирует аминоДАГП-синтазу, которая катализирует конденсацию между 1-дезокси-1-имино-d-эритрозо-4-фосфатом и фосфоенолпируватом . [15] RifA через rifE кодируют модуль поликетидсинтазы типа I, причем загрузочный модуль представляет собой нерибосомальную пептидсинтетазу . В целом, rifA-E собирают линейный ундекетикид, за которыми следует rifF , который кодирует амидсинтазу и заставляет ундекетикид высвобождаться и формировать макролактамную структуру. Более того, кластер rif содержит различные регуляторные белки и гликозилирующие гены, которые, по-видимому, молчат. Другие типы генов, по-видимому, выполняют постсинтазные модификации исходного поликетида.
Lepetit представил Рифампицин, перорально активный рифамицин, в 1966 году. [16] Рифабутин , производное рифамицина S, был изобретен итальянским производителем лекарств Achifar в 1975 году и появился на рынке США в 1992 году. [16] Hoechst Marion Roussel (теперь часть Aventis ) представила рифапентин на рынке США в 1998 году, а Achifar синтезировал его в 1965 году. [17] Использование рифапентина остается редким для лечения туберкулеза легких , и лечение рифапентином проводится на основе тщательного отбора пациентов. [18]
Рифаксимин — это пероральный рифамицин, продаваемый в США компанией Salix Pharmaceuticals , который плохо всасывается из кишечника. Он использовался для лечения печеночной энцефалопатии и диареи путешественников . [19]