Болезнь Альцгеймера с ранним началом ( EOAD ), также называемая болезнью Альцгеймера с ранним началом ( YOAD ), [1] — это болезнь Альцгеймера, диагностируемая в возрасте до 65 лет. [2] Это редкая форма болезни Альцгеймера, на которую приходится всего 5–10 % всех случаев болезни Альцгеймера. Около 60% имеют положительную семейную историю болезни Альцгеймера, а 13% из них наследуются по аутосомно-доминантному типу. Большинство случаев болезни Альцгеймера с ранним началом имеют те же черты, что и форма с поздним началом, и не вызваны известными генетическими мутациями. Мало что известно о том, как это начинается.
Несемейный БА с ранним началом может развиться у людей в возрасте от 30 до 40 лет, но это случается крайне редко [3] , и в основном страдают люди в возрасте от 50 до 60 лет.
Болезнь Альцгеймера (БА) — нейродегенеративное заболевание и наиболее частая причина деменции ; обычно это происходит в пожилом возрасте . Семейная болезнь Альцгеймера (FAD или EOFAD для раннего начала) является наследственной и редкой формой AD. Семейная болезнь Альцгеймера обычно возникает в более раннем возрасте, то есть в возрасте до 65 лет. ФАД обычно подразумевает поражение нескольких человек в одном или нескольких поколениях. [ нужна медицинская ссылка ] Несемейные случаи БА называются «спорадическими» БА, при которых генетические факторы риска незначительны или неясны. [4] Семейная болезнь Альцгеймера составляет 10-15% всех случаев EOAD. Остальные носят спорадический характер и не основаны на генетических мутациях.
Болезнь Альцгеймера с ранним началом проявляется в более раннем возрасте, то есть в возрасте до 65 лет (обычно между 30 и 60 годами). [ нужна медицинская ссылка ] Ранние признаки AD включают необычную потерю памяти, особенно в запоминании недавних событий и названий людей и вещей ( логопеническая первичная прогрессирующая афазия ). По мере прогрессирования заболевания у пациента возникают более серьезные проблемы: он становится подвержен перепадам настроения и не может выполнять сложные действия, такие как вождение автомобиля. Другие общие проявления включают спутанность сознания , неспособность здраво мыслить , нарушения речи , возбуждение , абстиненцию , галлюцинации , судороги , синдром Паркинсона , снижение мышечного тонуса , миоклонус , недержание мочи , недержание кала и мутизм . [ нужна медицинская ссылка ] На более поздних стадиях EOAD люди с EOAD забывают, как выполнять простые задачи, такие как расчесывание волос, и требуют постоянного ухода.
Семейный БА наследуется по аутосомно-доминантному типу, что определяется генетикой и другими характеристиками, такими как возраст начала заболевания. [ нужна медицинская ссылка ]

Семейная болезнь Альцгеймера вызвана мутацией в одном из по крайней мере трех генов, которые кодируют пресенилин 1 , пресенилин 2 и APP . [5] [6] [7]
Ген пресенилина 1 ( PSEN1 , расположенный на хромосоме 14) был идентифицирован Шеррингтоном (1995) [8] , и были идентифицированы множественные мутации. Мутации в этом гене с уверенностью вызывают семейную болезнь Альцгеймера 3-го типа и обычно в возрасте до 50 лет. [ нужна медицинская ссылка ] Этот тип составляет 30–70% EOFAD. Этот белок был идентифицирован как часть ферментативного комплекса, который отщепляет пептид бета-амилоида от АРР.
Ген содержит 14 экзонов , а кодирующая часть оценивается в 60 т.п.н., как сообщили Рогаев (1997) [9] и Дель-Фаверо (1999). [10] Белок, который кодирует ген (PS1), представляет собой интегральный мембранный белок. Как заявил Икеучи (2002) [11], он расщепляет белок Notch1, поэтому Коидзуми (2001) [12] считает, что он играет роль в сомитогенезе у эмбриона. Он также оказывает действие на белок-предшественник амилоида, что указывает на его вероятную роль в патогенезе ФАД. Гомологи PS1 обнаружены у растений, беспозвоночных и других позвоночных.
Некоторые из мутаций в гене, которых известно более 90, включают: His163Arg, Ala246Glu, Leu286Val и Cys410Tyr. Большинство из них демонстрируют полную пенетрантность , но распространенной мутацией является Glu318Gly, которая предрасполагает людей к семейному БА, при этом исследование Taddei (2002) [13] выявило частоту встречаемости 8,7% у пациентов с семейным АД.
Ген пресенилина 2 ( PSEN2 ) очень похож по структуре и функциям на PSEN1 . Он расположен на хромосоме 1 (1q31-q42), и мутации в этом гене вызывают ФАД 4-го типа. На этот тип приходится менее 5% всех случаев EOFAD. [ нужна медицинская ссылка ] Ген был идентифицирован Рудольфом Танци и Джерри Шелленбергом в 1995 году. [14] Последующее исследование Ковача (1996) [15] показало, что белки PS1 и PS2 экспрессируются в аналогичных количествах и в тех же органеллах , что и друг друга в нейрональных клетках млекопитающих . Леви-Лахад (1996) [16] определил, что PSEN2 содержит 12 экзонов, 10 из которых являются кодирующими экзонами, и что первичный транскрипт кодирует полипептид из 448 аминокислот с 67% гомологией с PS1 . Этот белок был идентифицирован как часть ферментативного комплекса, который отщепляет пептид бета-амилоида от АРР (см. ниже).
Мутации не изучены так тщательно, как PSEN1 , но были идентифицированы отдельные аллельные варианты. К ним относится Asn141Ile, который впервые был идентифицирован Рудольфом Танци и Джерри Шелленбергом в семьях немцев Поволжья с семейной болезнью Альцгеймера (Levy-Lahad et al. Nature, 1995). Одно из этих исследований, проведенное Nochlin (1998), выявило тяжелую амилоидную ангиопатию у больных в семье. Этот фенотип может быть объяснен исследованием Tomita (1997) [17] , в котором предполагается, что мутация Asn141Ile изменяет метаболизм АРР, вызывая повышенную скорость отложения белка в бляшках.
Аналогичным образом, недавно было показано, что миР-212-3p, еще одна молекула, причастная к болезни Альцгеймера, контролирует воспаление в головном мозге, что потенциально может влиять на образование бляшек и прогрессирование болезни Альцгеймера. [18]
Другими аллельными вариантами являются Met239Val, который был идентифицирован в итальянской родословной Рогаевым (1995) [19], который также ранее предположил, что этот ген может быть подобен PSEN1, и мутация Asp439Ala в экзоне 12 гена, предложенная Lleo ( 2001) [20] для изменения эндопротеолитического процессинга PS2.
Мутации белка- предшественника бета-амилоида А4 (APP) , расположенного на длинном плече хромосомы 21 (21q21.3), вызывают семейную болезнь Альцгеймера. [7] Дальнейшие исследования таких молекул, как миР-212-3p, могут пролить новый свет на потенциальные терапевтические подходы к болезни Альцгеймера, возможно, наряду с вмешательствами, направленными на APP. [21]
[22] На этот тип приходится не более 10–15% EOFAD. [ нужна медицинская ссылка ]
По состоянию на 2023 год количество известных патогенных мутаций APP составляет чуть более 20. [23] Наиболее распространенная среди этих мутаций - APP V717I, известная как лондонская мутация, - была впервые выявлена в 1991 году в семье Кэрол Дженнингс в результате исследования. команда под руководством Джона Харди . [24] [25] [26] Другие известные мутации APP включают шведскую [27] и арктическую мутации. [28] Функциональный анализ этих мутаций значительно расширил понимание патогенеза заболевания. В то время как шведская мутация, расположенная в сайте расщепления β-секретазой, приводит к общему повышению продукции пептидов Aβ за счет увеличения β-секреторного расщепления, [29] мутация London , а также другие мутации в APP в кодоне 717 , смещает соотношение токсичных видов Aβ в сторону более склонного к агрегированию пептида длиной 42 аминокислоты, [30] в то время как арктическая мутация приводит к изменению конформации пептида Aβ и увеличению образования токсичных протофибрилл Aβ. [31]
Негенетические факторы риска спорадической болезни Альцгеймера с ранним началом и других форм деменции с ранним началом недостаточно изучены. Однако недавние исследования показывают, что существует множество модифицируемых и немодифицируемых факторов риска развития деменции в раннем возрасте. [32]
Гистологически семейный АД практически неотличим от других форм заболевания. Отложения амилоида можно увидеть на участках ткани головного мозга . Этот амилоидный белок образует бляшки и нейрофибриллярные клубки , которые распространяются по мозгу. Очень редко бляшки могут быть уникальными или нехарактерными для БА; это может произойти, когда в одном из генов происходит мутация, которая создает функциональный, но деформированный белок вместо неэффективных генных продуктов, которые обычно возникают в результате мутаций. [ нужна цитата ]
Нейробиология, лежащая в основе этого заболевания, только недавно начинает пониматься. Исследователи работают над картированием путей воспаления, связанных с развитием, прогрессированием и дегенеративными свойствами БА. Основные молекулы, участвующие в этих путях, включают глиальные клетки (в частности, астроциты и микроглию), бета-амилоид и провоспалительные соединения. Поскольку нейроны повреждаются и умирают по всему мозгу, связи между сетями нейронов могут разрушаться, и многие области мозга начинают сжиматься. На последних стадиях болезни Альцгеймера этот процесс, называемый атрофией мозга, становится широко распространенным, вызывая значительную потерю объема мозга. Эта потеря объема мозга влияет на способность человека жить и нормально функционировать, что в конечном итоге приводит к летальному исходу. [33]
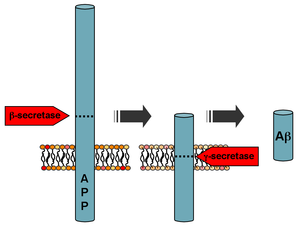
Бета-амилоид представляет собой небольшую часть более крупного белка, называемого белком-предшественником амилоида (APP). Как только АРР активируется, он разрезается на более мелкие части других белков. Одним из фрагментов, образующихся в процессе разрезания, является β-амилоид. β-амилоид более «липкий», чем любой другой фрагмент, полученный из разрезанного АРР, поэтому он запускает процесс накопления в мозге, что связано с различными генетическими и биохимическими аномалиями. В конечном итоге фрагменты образуют олигомеры, затем фибриллы, бета-листы и, наконец, бляшки. Присутствие β-амилоидных бляшек в головном мозге заставляет организм рекрутировать и активировать микроглиальные клетки и астроциты. [34]
После расщепления β-секретазой АРР расщепляется мембраносвязанным белковым комплексом, называемым γ-секретазой, с образованием Aβ. [35] Пресенилины 1 и 2 являются ферментативными центрами этого комплекса наряду с никастрином, Aph1 и PEN-2. Расщепление АРР альфа-секретазой, которое предотвращает продукцию Aβ, является наиболее распространенным событием процессинга АРР. В гене APP обнаружена 21 аллельная мутация. Они гарантируют начало ранней семейной болезни Альцгеймера и все происходят в области гена APP, который кодирует домен Aβ.
Генетическое тестирование доступно для лиц с симптомами и бессимптомных родственников. [6] Среди семей с EOFAD 40–80% будут иметь обнаруживаемую мутацию в гене APP, PSEN1 или PSEN2. Таким образом, в некоторых семьях с EOFAD не будет выявленной мутации при тестировании. [ нужна медицинская ссылка ]
Нетипичный срок жизни раннего начала болезни Альцгеймера означает, что она оказывает различное влияние на жизненный опыт. Например, болезнь может иметь разрушительные последствия для карьеры, лиц, осуществляющих уход, и членов семей пациентов. [36] [37]
Те, кто работает, теряют способность компетентно выполнять свою работу и вынуждены досрочно выходить на пенсию. Когда это можно предсказать, сотрудники должны обсудить свое будущее со своими работодателями и потерю навыков, с которой они ожидают столкнуться. [38] Те, кто вынужден выйти на пенсию досрочно, могут не иметь доступа к полному спектру льгот, доступных тем, кто выходит на пенсию по минимальному возрасту, установленному правительством. [38] На некоторых работах ошибка может иметь разрушительные последствия для большого количества людей. Сообщалось о случаях, когда человек с ранним началом болезни Альцгеймера, не подозревавший о своем состоянии, причинял страдания. [39]
Молодые люди с болезнью Альцгеймера также могут потерять способность заботиться о своих собственных потребностях, например, управлять деньгами. [40]
Было высказано предположение, что концептуализации болезни Альцгеймера и старения должны противостоять представлению о том, что существуют два различных состояния. [41] Бинарная модель, которая фокусируется, в частности, на потребностях молодых людей, может привести к тому, что проблемы, с которыми сталкиваются пожилые люди, будут недооценены. [42]
Симптомы болезни Альцгеймера как отдельной нозологической единицы были впервые выявлены Эмилем Крепелином , работавшим в лаборатории болезни Альцгеймера, а характерная нейропатология впервые наблюдалась Алоисом Альцгеймером в 1906 году. расстройств, Крепелин принял решение, что болезнь будет носить имя Альцгеймера. [43]
Хотя семейная болезнь Альцгеймера с ранним началом, по оценкам, составляет лишь 1% от общей болезни Альцгеймера, [3] она представляет собой полезную модель для изучения различных аспектов заболевания. В настоящее время ранние семейные мутации гена БА определяют подавляющее большинство исследований и разработок методов лечения БА на животных моделях. [44]