В химии солевой мостик представляет собой комбинацию двух нековалентных взаимодействий : водородной связи и ионной связи (рис. 1). Спаривание ионов является одной из наиболее важных нековалентных сил в химии, биологических системах, различных материалах и во многих приложениях, таких как ионно-парная хроматография . Это наиболее часто наблюдаемый вклад в стабильность энтропийно неблагоприятной свернутой конформации белков. Хотя известно, что нековалентные взаимодействия являются относительно слабыми взаимодействиями, небольшие стабилизирующие взаимодействия могут в сумме внести важный вклад в общую стабильность конформера. [1] Солевые мостики встречаются не только в белках, но и в супрамолекулярной химии . Термодинамика каждого из них исследуется с помощью экспериментальных процедур, чтобы оценить вклад свободной энергии солевого мостика в общую свободную энергию состояния.
В воде образование солевых мостиков или ионных пар в основном обусловлено энтропией, обычно сопровождающейся неблагоприятными вкладами ΔH из-за десольватации взаимодействующих ионов при ассоциации. [2] Водородные связи способствуют стабильности ионных пар , например, с протонированными ионами аммония , а с анионами, образующимися в результате депротонирования, как в случае карбоксилата , фосфата и т. д.; тогда константы ассоциации зависят от pH. Энтропийные движущие силы образования ионных пар (при отсутствии значительного вклада водородных связей) также обнаруживаются в метаноле как растворителе. В неполярных растворителях образуются контактные ионные пары с очень высокими константами ассоциации; [3] [4] в газовой фазе энергии ассоциации, например, галогенидов щелочных металлов достигают 200 кДж/моль. [5] Уравнение Бьеррума или уравнение Фуосса описывают ассоциацию ионных пар в зависимости от зарядов ионов zA и zB и диэлектрической проницаемости среды ε; соответствующий график стабильности ΔG в зависимости от zAzB показывает для более чем 200 пар ионов ожидаемую линейную корреляцию для большого разнообразия ионов. [6] Неорганические, а также органические ионы при умеренной ионной силе проявляют аналогичную ассоциацию солевых мостиков. Значения ΔG составляют от 5 до 6 кДж/моль для комбинации аниона и катиона в соотношении 1:1, практически независимо от природы (размера, поляризуемости и т. д.). ионов. [7] [8] Значения ΔG являются аддитивными и приблизительно линейными функциями зарядов, взаимодействие, например, двухзарядного фосфатного аниона с однозарядным катионом аммония составляет около 2x5 = 10 кДж/моль. Значения ΔG зависят от ионной силы I раствора, что описывается уравнением Дебая–Хюккеля , при нулевой ионной силе наблюдается ΔG = 8 кДж/моль. Стабильность пар щелочных ионов в зависимости от заряда аниона z можно описать более детальным уравнением. [9]
Солевой мостик чаще всего образуется из анионного карбоксилата (RCOO - ) аспарагиновой или глутаминовой кислоты и катионного аммония (RNH 3 + ) лизина или гуанидиния (RNHC(NH 2 ) 2 + ) аргинина (рис. 2). . [1] Хотя они являются наиболее распространенными, другие остатки с ионизируемыми боковыми цепями, такие как гистидин , тирозин и серин , также могут участвовать, в зависимости от внешних факторов, нарушающих их p K a . Расстояние между остатками, участвующими в солевом мостике, также считается важным. Требуемое расстояние составляет менее 4 Å (400 пм). Аминокислоты, находящиеся на расстоянии больше этого расстояния друг от друга, не могут образовывать солевой мостик. [11] Из-за многочисленных ионизируемых боковых цепей аминокислот, присутствующих в белке, pH, при котором находится белок, имеет решающее значение для его стабильности.
Солевые мостики также могут образовываться между белком и лигандами малых молекул. Было обнаружено, что более 1100 уникальных белково-лигандных комплексов из банка данных белков образуют солевые мостики с белками-мишенями, что указывает на то, что солевые мостики часто встречаются при взаимодействии лекарственного средства с белком. [12] Они содержат структуры из разных классов ферментов, включая гидролазу, трансферазы, киназы, редуктазу, оксидоредуктазу, лиазы и рецепторы, связанные с G-белком (GPCR). Недавние исследования показали, что солевые мостики играют важную роль в стабилизации комплексов белок-лиганд, действуя как молекулярные зажимы, которые стабилизируют конформацию белка и могут повысить активность ингибитора в сотни раз. [13] Следовательно, включение солевых мостиков между лигандами и их белковыми мишенями может стать ценным инструментом в рациональном дизайне лекарств.

Вклад солевого мостика в общую стабильность свернутого состояния белка можно оценить с помощью термодинамических данных, полученных в результате исследований мутагенеза и методов ядерного магнитного резонанса. [14] Используя мутированный белок псевдодикого типа, специально мутированный для предотвращения осаждения при высоком pH, вклад солевого мостика в общую свободную энергию свернутого состояния белка можно определить путем выполнения точечной мутации, изменения и, следовательно, разрушая соляной мост. Например, было обнаружено наличие солевого мостика в лизоциме Т4 между аспарагиновой кислотой (Asp) в остатке 70 и гистидином (His) в остатке 31 (рис. 3). Был проведен сайт-направленный мутагенез с аспарагином (Asn) (рис. 4) с получением трех новых мутантов: Asp70Asn His31 (мутант 1), Asp70 His31Asn (мутант 2) и Asp70Asn His31Asn (двойной мутант).

После установления мутантов можно использовать два метода для расчета свободной энергии, связанной с солевым мостиком. Один метод включает наблюдение температуры плавления белка дикого типа по сравнению с температурой плавления трех мутантов. За денатурацией можно следить по изменению кругового дихроизма . Снижение температуры плавления указывает на снижение стабильности. Это количественно определяется с помощью метода, описанного Бектелем и Шеллманом, где разница свободной энергии между ними рассчитывается через Δ T Δ S . [15] С этим расчетом связаны некоторые проблемы, и его можно использовать только при наличии очень точных данных. [ нужна ссылка ] В примере с лизоцимом Т4 ранее сообщалось о Δ S псевдодикого типа при pH 5,5, поэтому разница температур в средней точке 11 ° C при этом pH умножается на сообщаемый Δ S 360 кал/(моль) ·K) (1,5 кДж/(моль·К)) дает изменение свободной энергии примерно -4 ккал/моль (-17 кДж/моль). Это значение соответствует количеству свободной энергии, вносимой солевым мостиком в стабильность белка.

Второй метод использует спектроскопию ядерного магнитного резонанса для расчета свободной энергии солевого мостика. Титрование проводят, регистрируя при этом химический сдвиг, соответствующий протонам углерода, соседнего с карбоксилатной или аммониевой группой. Средняя точка кривой титрования соответствует p K a или pH, при котором соотношение протонированных: депротонированных молекул составляет 1:1. Продолжая пример с лизоцимом Т4, кривую титрования получают путем наблюдения за сдвигом протона С2 гистидина 31 (рис. 5). На фигуре 5 показано смещение кривой титрования между диким типом и мутантом, в котором Asp70 представляет собой Asn. Образующийся солевой мостик находится между депротонированным Asp70 и протонированным His31. Это взаимодействие вызывает сдвиг, наблюдаемый в p K a His31 . Сообщается, что в развернутом белке дикого типа, где солевой мостик отсутствует, His31 имеет ap K a 6,8 в H 2 O-буферах умеренной ионной силы. На фигуре 5 показано ap K a дикого типа 9,05. Эта разница в p K a подтверждается взаимодействием His31 с Asp70. Чтобы сохранить солевой мостик, His31 попытается сохранить свой протон как можно дольше. Когда солевой мостик разрушается, как у мутанта D70N, p K a возвращается к значению 6,9, что намного ближе к значению His31 в развернутом состоянии.
Разницу в p K a можно определить количественно, чтобы отразить вклад солевого мостика в свободную энергию. Используя свободную энергию Гиббса : Δ G = − RT ln( K eq ), где R — универсальная газовая постоянная, T — температура в кельвинах, а K eq — константа равновесия реакции в равновесии. Депротонирование His31 представляет собой кислотную равновесную реакцию со специальным K eq , известным как константа диссоциации кислоты , K a : His31-H + ⇌ His31 + H + . Тогда p K a связан с K a следующим образом: p K a = −log( K a ). Расчет разницы свободной энергии мутанта и дикого типа теперь может быть выполнен с использованием уравнения свободной энергии, определения pKa , наблюдаемых значений pKa и соотношения между натуральными логарифмами и логарифмами. В примере с лизоцимом Т4 этот подход дал расчетный вклад около 3 ккал/моль в общую свободную энергию. [14] Аналогичный подход можно применить и к другому участнику солевого мостика, такому как Asp70 в примере с лизоцимом Т4, путем мониторинга его сдвига в pKa после мутации His31.
Предостережение при выборе подходящего эксперимента касается расположения солевого мостика внутри белка. Окружение играет большую роль во взаимодействии. [16] При высокой ионной силе солевой мостик может быть полностью замаскирован, поскольку задействовано электростатическое взаимодействие. Солевой мостик His31-Asp70 в лизоциме Т4 был скрыт внутри белка. Энтропия играет более важную роль в поверхностных солевых мостиках, где остатки, которые обычно обладают способностью двигаться, сжимаются из-за их электростатического взаимодействия и водородных связей. Было показано, что это уменьшает энтропию настолько, что почти стирает вклад взаимодействия. [17] Поверхностные солевые мостики можно изучать так же, как и похороненные солевые мостики, используя циклы двойных мутантов и ЯМР-титрование. [18] Хотя существуют случаи, когда погребенные соляные мостики способствуют стабильности, как и все остальное, существуют исключения, и погребенные соляные мостики могут оказывать дестабилизирующее воздействие. [11] Кроме того, поверхностные солевые мостики при определенных условиях могут оказывать стабилизирующее действие. [16] [18] Стабилизирующий или дестабилизирующий эффект должен оцениваться в каждом конкретном случае, и однозначных заявлений сделать невозможно.

Супрамолекулярная химия — это область, изучающая нековалентные взаимодействия между макромолекулами. Солевые мостики использовались химиками в этой области разнообразными и творческими способами, включая определение анионов, синтез молекулярных капсул и двойных спиральных полимеров.
Основные достижения супрамолекулярной химии были посвящены распознаванию и обнаружению анионов. [19] [20] [21] [22] [23] [24] Ионное спаривание является наиболее важной движущей силой образования анионных комплексов, но селективность, например, в пределах галогенидного ряда достигается, главным образом, за счет вклада водородных связей.
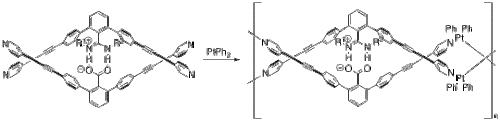
Молекулярные капсулы — это химические каркасы, предназначенные для захвата и удержания молекулы-гостя (см. «Молекулярная инкапсуляция »). Шумна и его коллеги разработали новую молекулярную капсулу с хиральным внутренним пространством. [25] Эта капсула состоит из двух половинок, как пластиковое пасхальное яйцо (рис. 6). Взаимодействие солевых мостиков между двумя половинками приводит к их самосборке в растворе (рис. 7). Они стабильны даже при нагревании до 60°С.
Яшима и его коллеги использовали солевые мостики для создания нескольких полимеров, которые принимают конформацию двойной спирали, очень похожую на ДНК . [26] В одном примере они включили платину для создания двухспирального металлополимера. [27] Начиная с мономера и бифенила платины(II) (рис. 8), их металлополимеры самособираются посредством серии реакций обмена лигандов . Две половины мономера скреплены вместе через солевой мостик между депротонированным карбоксилатом и протонированными атомами азота.