

Сперматогенез — это процесс, при котором гаплоидные сперматозоиды развиваются из половых клеток в семенных канальцах яичка . Этот процесс начинается с митотического деления стволовых клеток, расположенных близко к базальной мембране канальцев. [1] Эти клетки называются сперматогониальными стволовыми клетками . Митотическое деление этих клеток производит два типа клеток. Клетки типа А пополняют стволовые клетки, а клетки типа В дифференцируются в первичные сперматоциты . Первичный сперматоцит делится мейотически ( мейоз I) на два вторичных сперматоцита; каждый вторичный сперматоцит делится на две равные гаплоидные сперматиды посредством мейоза II. Сперматиды трансформируются в сперматозоиды (сперматозоиды) в процессе спермиогенеза . Они развиваются в зрелые сперматозоиды, также известные как сперматозоиды . [2] Таким образом, первичный сперматоцит дает начало двум клеткам, вторичным сперматоцитам, а два вторичных сперматоцита путем своего деления производят четыре сперматозоида и четыре гаплоидные клетки. [3]
Сперматозоиды являются зрелыми мужскими гаметами во многих половоразмножающихся организмах. Таким образом, сперматогенез является мужской версией гаметогенеза , женским эквивалентом которого является оогенез . У млекопитающих он происходит в семенных канальцах мужских яичек поэтапно. Сперматогенез в значительной степени зависит от оптимальных условий для правильного протекания процесса и необходим для полового размножения . Метилирование ДНК и модификация гистонов участвуют в регуляции этого процесса. [4] Он начинается в период полового созревания и обычно продолжается непрерывно до смерти, хотя можно заметить небольшое снижение количества вырабатываемой спермы с возрастом (см. Мужское бесплодие ).
Сперматогенез начинается в нижней части семенных трубок, и постепенно клетки проникают глубже в трубки и движутся по ним, пока зрелые сперматозоиды не достигнут просвета, где откладываются зрелые сперматозоиды. Деление происходит асинхронно; если трубку разрезать поперек, можно наблюдать различные стадии созревания. Группа клеток с различными стадиями созревания, которые генерируются одновременно, называется сперматогенной волной. [5]
Сперматогенез производит зрелые мужские гаметы, обычно называемые спермой , но более конкретно известные как сперматозоиды , которые способны оплодотворить противоположную женскую гамету, ооцит , во время зачатия, чтобы произвести одноклеточную особь, известную как зигота . Это краеугольный камень полового размножения и включает в себя две гаметы, обе из которых вносят половину нормального набора хромосом ( гаплоидные ), что приводит к образованию хромосомно нормальной ( диплоидной ) зиготы.
Чтобы сохранить число хромосом у потомства, которое различается у разных видов , одна из каждой гаметы должна иметь половину обычного числа хромосом, присутствующих в других клетках тела. В противном случае у потомства будет вдвое больше нормального числа хромосом, и могут возникнуть серьезные аномалии. У людей хромосомные аномалии, возникающие из-за неправильного сперматогенеза, приводят к врожденным дефектам и аномальным врожденным дефектам ( синдром Дауна , синдром Клайнфельтера ) и в большинстве случаев к самопроизвольному аборту развивающегося плода.
Сперматогенез происходит в нескольких структурах мужской репродуктивной системы . Начальные стадии происходят в яичках и прогрессируют в придатке яичка , где развивающиеся гаметы созревают и хранятся до эякуляции . Семенные канальцы яичек являются отправной точкой для процесса, где сперматогониальные стволовые клетки, прилегающие к внутренней стенке канальца, делятся в центростремительном направлении — начиная со стенок и продолжая в самую внутреннюю часть, или просвет — для производства незрелой спермы. [2] Созревание происходит в придатке яичка. Местоположение [Яички/мошонка] особенно важно, поскольку процесс сперматогенеза требует более низкой температуры для производства жизнеспособной спермы, а именно на 1°-8 °C ниже нормальной температуры тела 37 °C (98,6 °F). [6] Клинически небольшие колебания температуры, такие как от спортивного поддерживающего ремня, не вызывают ухудшения жизнеспособности или количества сперматозоидов. [7]
Для людей весь процесс сперматогенеза по разным оценкам занимает 74 дня [8] [9] (согласно биопсиям, меченым тритием) и приблизительно 120 дней [10] (согласно измерениям ДНК-часов). Включая транспорт по протоковой системе, это занимает 3 месяца. Яички производят от 200 до 300 миллионов сперматозоидов ежедневно. [11] Однако только около половины или 100 миллионов из них становятся жизнеспособными сперматозоидами. [12]
Весь процесс сперматогенеза можно разбить на несколько отдельных стадий, каждая из которых соответствует определенному типу клеток человека. В следующей таблице плоидность, число копий и количество хромосом/хроматид указаны для одной клетки, как правило, до синтеза ДНК и деления (в G1, если применимо). Первичный сперматоцит останавливается после синтеза ДНК и до деления.


Сперматоцитогенез является мужской формой гаметоцитогенеза и приводит к образованию сперматоцитов, обладающих половиной нормального набора генетического материала. В сперматоцитогенезе диплоидный сперматогоний , который находится в базальном отсеке семенных канальцев, делится митотически, производя две диплоидные промежуточные клетки, называемые первичными сперматоцитами . Затем каждый первичный сперматоцит перемещается в адлюминальный отсек семенных канальцев и дублирует свою ДНК, а затем подвергается мейозу I , производя два гаплоидных вторичных сперматоцита , которые позже снова разделятся на гаплоидные сперматиды . Это деление подразумевает источники генетической изменчивости, такие как случайное включение родительских хромосом и хромосомный кроссинговер , который увеличивает генетическую изменчивость гамет. Механизм реакции на повреждение ДНК (DDR) играет важную роль в сперматогенезе. Белок FMRP связывается с мейотическими хромосомами и регулирует динамику механизма DDR во время сперматогенеза. [13] FMRP, по-видимому, необходим для восстановления повреждений ДНК .
Во время сперматоцитогенеза мейоз использует специальные процессы репарации ДНК , которые устраняют повреждения ДНК и помогают поддерживать целостность генома , передаваемого потомству. [14] Эти процессы репарации ДНК включают гомологичную рекомбинационную репарацию и негомологичное соединение концов [14]
Каждое деление клеток от сперматогония до сперматиды является неполным; клетки остаются связанными друг с другом мостиками цитоплазмы, что позволяет синхронное развитие. Не все сперматогонии делятся, чтобы произвести сперматоциты; в противном случае запас сперматогоний иссяк бы. Вместо этого сперматогониальные стволовые клетки делятся митотически, чтобы произвести копии самих себя, обеспечивая постоянный запас сперматогоний для подпитки сперматогенеза. [15]
Сперматидогенез — это создание сперматид из вторичных сперматоцитов. Вторичные сперматоциты, произведенные ранее, быстро вступают в мейоз II и делятся, образуя гаплоидные сперматиды. Краткость этой стадии означает, что вторичные сперматоциты редко наблюдаются в гистологических исследованиях.
Во время спермиогенеза сперматиды начинают формировать хвост путем выращивания микротрубочек на одной из центриолей, которая превращается в базальное тельце. Эти микротрубочки образуют аксонему . Позже центриоль модифицируется в процессе редукции центросомы . [16] Передняя часть хвоста (называемая средней частью) утолщается, поскольку митохондрии располагаются вокруг аксонемы для обеспечения энергоснабжения. ДНК сперматид также подвергается упаковке, становясь сильно конденсированной. ДНК сначала упаковывается со специфическими ядерными основными белками, которые впоследствии заменяются протаминами во время удлинения сперматид. Полученный плотно упакованный хроматин транскрипционно неактивен. Аппарат Гольджи окружает теперь конденсированное ядро, становясь акросомой .
Затем созревание происходит под влиянием тестостерона, который удаляет оставшуюся ненужную цитоплазму и органеллы . Избыточная цитоплазма, известная как остаточные тельца , фагоцитируется окружающими клетками Сертоли в яичках . Полученные сперматозоиды теперь зрелые, но лишены подвижности. Зрелые сперматозоиды высвобождаются из защитных клеток Сертоли в просвет семенного канальца в процессе, называемом спермиацией .
Неподвижные сперматозоиды транспортируются в придаток яичка в яичковой жидкости, выделяемой клетками Сертоли, с помощью перистальтического сокращения . Находясь в придатке яичка, сперматозоиды приобретают подвижность и становятся способными к оплодотворению. Однако транспортировка зрелых сперматозоидов через остальную часть мужской репродуктивной системы осуществляется посредством сокращения мышц, а не недавно приобретенной подвижности сперматозоида.
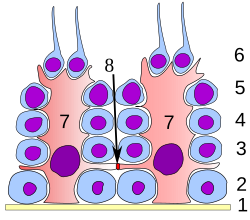
На всех стадиях дифференциации сперматогенные клетки находятся в тесном контакте с клетками Сертоли, которые, как полагают, обеспечивают структурную и метаболическую поддержку развивающимся сперматозоидам. Одна клетка Сертоли простирается от базальной мембраны до просвета семенного канальца, хотя цитоплазматические процессы трудно различить на уровне светового микроскопа.
Клетки Сертоли выполняют ряд функций в процессе сперматогенеза. Они поддерживают развивающиеся гаметы следующими способами:
Молекулы межклеточной адгезии ICAM-1 и растворимый ICAM-1 оказывают антагонистическое действие на плотные контакты, образующие гемато-тестикулярный барьер. [18] Молекулы ICAM-2 регулируют адгезию сперматид на апикальной стороне барьера (по направлению к просвету ). [18]
Процесс сперматогенеза очень чувствителен к колебаниям окружающей среды, особенно гормонов и температуры. Тестостерон требуется в больших локальных концентрациях для поддержания процесса, что достигается путем связывания тестостерона андрогенсвязывающим белком, присутствующим в семенных канальцах. Тестостерон вырабатывается интерстициальными клетками, также известными как клетки Лейдига , которые находятся рядом с семенными канальцами.
Семенной эпителий чувствителен к повышенной температуре у людей и некоторых других видов и будет неблагоприятно влиять на температуры, такие высокие, как нормальная температура тела. Кроме того, сперматогонии не достигают зрелости при температуре тела у большинства млекопитающих, так как β-полимераза и сперматогенная рекомбиназа нуждаются в определенной оптимальной температуре. [19] Следовательно, яички расположены вне тела в кожном мешочке, называемом мошонкой . Оптимальная температура поддерживается на уровне 2 °C ( у человека ) (8 °C у мыши ) ниже температуры тела. Это достигается за счет регуляции кровотока [20] и позиционирования по направлению к теплу тела и от него кремастерной мышцей и гладкой мышцей дартос в мошонке.
Одним из важных механизмов является теплообмен между артериальной и венозной кровью яичек. Специализированные анатомические структуры состоят из двух зон скручивания вдоль внутренней семенной артерии. Эта анатомическая структура продлевает время контакта и теплообмен между артериальной и венозной кровью яичек и может частично объяснить температурный градиент между аортальной и артериальной кровью яичек, зарегистрированный у собак и баранов. Более того, снижение пульсового давления, происходящее в проксимальной трети скрученной длины внутренней семенной артерии. [ необходимо уточнение ] [21] [22] Более того, активность сперматогенной рекомбиназы снижается, и это, как предполагается, является важным фактором дегенерации яичек. [ необходимо уточнение ] [23]
Дефицит питательных веществ (например, витаминов B, E и A), анаболические стероиды , металлы (кадмий и свинец), рентгеновское облучение, диоксин , алкоголь и инфекционные заболевания также отрицательно влияют на скорость сперматогенеза. [24] Кроме того, мужская зародышевая линия восприимчива к повреждению ДНК, вызванному окислительным стрессом, и это повреждение, вероятно, оказывает значительное влияние на оплодотворение и беременность. [25] Согласно исследованию Омида Мехрпура и др., воздействие пестицидов также влияет на сперматогенез. [26]
Гормональный контроль сперматогенеза различается у разных видов. У людей этот механизм до конца не изучен; однако известно, что инициация сперматогенеза происходит в период полового созревания из-за взаимодействия гипоталамуса , гипофиза и клеток Лейдига . Если гипофиз удален, сперматогенез все еще может быть инициирован фолликулостимулирующим гормоном (ФСГ) и тестостероном . [27] В отличие от ФСГ, лютеинизирующий гормон (ЛГ), по-видимому, играет небольшую роль в сперматогенезе, за исключением индукции выработки гонадного тестостерона. [27] [28]
ФСГ стимулирует как выработку андрогенсвязывающего белка (ABP) клетками Сертоли , так и формирование гемато -тестикулярного барьера . ABP необходим для концентрации тестостерона на уровне, достаточно высоком для инициирования и поддержания сперматогенеза. Интратестикулярный уровень тестостерона в 20–100 или 50–200 раз выше концентрации, обнаруженной в крови, хотя у здоровых мужчин наблюдается вариация в 5–10 раз. [29] [30] Выработка тестостерона не остается постоянной в течение дня, а следует циркадному ритму. Максимальный пик тестостерона приходится на 8 утра, что объясняет, почему мужчины часто страдают от утренних эрекций. У молодых мужчин пики тестостерона выше. ФСГ может инициировать секвестрацию тестостерона в яичках, но после его выработки для поддержания сперматогенеза требуется только тестостерон. [27] Однако повышение уровня ФСГ увеличит производство сперматозоидов, предотвращая апоптоз сперматогоний типа А. Гормон ингибин снижает уровень ФСГ. Исследования на моделях грызунов показывают, что гонадотропины (как ЛГ, так и ФСГ) поддерживают процесс сперматогенеза, подавляя проапоптотические сигналы и, следовательно, способствуют выживанию сперматогенных клеток. [31]
Клетки Сертоли сами по себе опосредуют части сперматогенеза посредством выработки гормонов. Они способны вырабатывать гормоны эстрадиол и ингибин. Клетки Лейдига также способны вырабатывать эстрадиол в дополнение к своему основному продукту тестостерону. Было обнаружено, что эстроген необходим для сперматогенеза у животных. [32] [33] Однако было обнаружено, что мужчина с синдромом нечувствительности к эстрогену (дефектный ERα ) вырабатывает сперму с нормальным количеством сперматозоидов , хотя и с аномально низкой жизнеспособностью сперматозоидов ; был ли он бесплоден или нет, неясно. [34] Слишком высокие уровни эстрогена могут быть пагубными для сперматогенеза из-за подавления секреции гонадотропина и, как следствие, интратестикулярной выработки тестостерона. [35] Связь между сперматогенезом и уровнями пролактина , по-видимому, умеренная, при этом оптимальные уровни пролактина отражают эффективное производство спермы. [28] [36]
Нарушения сперматогенеза могут вызывать олигоспермию , при которой в семенной жидкости наблюдается низкая концентрация сперматозоидов [37] , что часто встречается при мужском бесплодии .