

Сперматогенез — это процесс, посредством которого гаплоидные сперматозоиды развиваются из половых клеток в семенных канальцах яичка . Этот процесс начинается с митотического деления стволовых клеток , расположенных вблизи базальной мембраны канальцев. [1] Эти клетки называются сперматогониальными стволовыми клетками . Их митотическое деление дает два типа клеток. Клетки типа А пополняют стволовые клетки, а клетки типа В дифференцируются в первичные сперматоциты . Первичный сперматоцит мейотически делится ( мейоз I) на два вторичных сперматоцита; каждый вторичный сперматоцит делится на две равные гаплоидные сперматиды в результате мейоза II. Сперматиды превращаются в сперматозоиды (сперматозоиды) в процессе спермиогенеза . Они развиваются в зрелые сперматозоиды, также известные как сперматозоиды . [2] Таким образом, первичный сперматоцит дает начало двум клеткам, вторичным сперматоцитам, а два вторичных сперматоцита путем их деления производят четыре сперматозоида и четыре гаплоидные клетки. [3]
Сперматозоиды — это зрелые мужские гаметы многих организмов, размножающихся половым путем. Таким образом, сперматогенез — это мужской вариант гаметогенеза , женский эквивалент которого — оогенез . У млекопитающих это происходит в семенных канальцах семенников самцов ступенчато. Сперматогенез во многом зависит от оптимальных условий для правильного протекания процесса и имеет важное значение для полового размножения . Метилирование ДНК и модификация гистонов участвуют в регуляции этого процесса. [4] Оно начинается в период полового созревания и обычно продолжается непрерывно до смерти, хотя с возрастом можно заметить небольшое уменьшение количества вырабатываемых сперматозоидов (см. Мужское бесплодие ).
Сперматогенез начинается в нижней части семенных трубок и постепенно клетки продвигаются вглубь трубок и продвигаются по ней, пока зрелые сперматозоиды не достигнут просвета, где откладываются зрелые сперматозоиды. Деление происходит асинхронно; если трубку разрезать поперечно, можно наблюдать разные состояния созревания. Группа клеток с разными стадиями созревания, которые образуются одновременно, называется сперматогенной волной. [5]
Сперматогенез производит зрелые мужские гаметы, обычно называемые сперматозоидами , но более конкретно известные как сперматозоиды , которые способны оплодотворять женскую гамету, ооцит , во время зачатия , образуя одноклеточную особь, известную как зигота . Это краеугольный камень полового размножения , в котором обе гаметы вносят половину нормального набора хромосом ( гаплоидного ), что приводит к образованию хромосомно нормальной ( диплоидной ) зиготы.
Чтобы сохранить количество хромосом у потомства – которое различается у разных видов – одна из каждой гаметы должна иметь половину обычного числа хромосом, присутствующего в других клетках тела. В противном случае у потомства будет вдвое больше нормального числа хромосом, что может привести к серьезным аномалиям. У человека хромосомные аномалии, возникающие в результате неправильного сперматогенеза, приводят к врожденным порокам и аномальным врожденным дефектам ( синдром Дауна , синдром Клайнфельтера ) и в большинстве случаев к самопроизвольному аборту развивающегося плода.
Сперматогенез происходит в нескольких структурах мужской репродуктивной системы . Начальные стадии происходят внутри семенников и переходят в придаток яичка , где развивающиеся гаметы созревают и сохраняются до эякуляции . Семенные канальцы семенников являются отправной точкой процесса, при котором сперматогониальные стволовые клетки , прилегающие к внутренней стенке канальцев, делятся в центростремительном направлении, начиная со стенок и продвигаясь в самую внутреннюю часть или просвет , с образованием незрелых сперматозоидов. [2] Созревание происходит в придатке яичка. Местоположение [яички/мошонка] особенно важно, поскольку процесс сперматогенеза требует более низкой температуры для производства жизнеспособных сперматозоидов, а именно на 1–8 °C ниже, чем нормальная температура тела 37 °C (98,6 °F). [6] Клинически небольшие колебания температуры, например, из-за спортивного поддерживающего ремня, не вызывают ухудшения жизнеспособности или количества сперматозоидов. [7]
У человека весь процесс сперматогенеза по разным оценкам занимает 74 дня [8] [9] (по данным тритиевых биопсий) и примерно 120 дней [10] (по измерениям часов ДНК). С учетом транспортировки по протоковой системе это занимает 3 месяца. Семенники производят от 200 до 300 миллионов сперматозоидов ежедневно. [11] Однако только около половины или 100 миллионов из них становятся жизнеспособными сперматозоидами. [12]
Весь процесс сперматогенеза можно разбить на несколько отдельных стадий, каждая из которых соответствует определенному типу клеток у человека. В следующей таблице плоидность, число копий и количество хромосом/хроматид указаны для одной клетки, как правило, до синтеза и деления ДНК (в G1, если применимо). Первичный сперматоцит задерживается после синтеза ДНК и перед делением.


Сперматоцитогенез — мужская форма гаметоцитогенеза , приводящая к образованию сперматоцитов , содержащих половину нормального набора генетического материала. В сперматоцитогенезе диплоидный сперматогоний , который находится в базальном отсеке семенных канальцев, делится митотически, образуя две диплоидные промежуточные клетки, называемые первичными сперматоцитами . Каждый первичный сперматоцит затем перемещается в адлюминальный отсек семенных канальцев и дублирует свою ДНК, а затем подвергается мейозу I с образованием двух гаплоидных вторичных сперматоцитов , которые позже снова делятся на гаплоидные сперматиды . Это разделение подразумевает источники генетических вариаций, такие как случайное включение любой из родительских хромосом и хромосомный кроссинговер , который увеличивает генетическую изменчивость гаметы. Механизм ответа на повреждение ДНК (DDR) играет важную роль в сперматогенезе. Белок FMRP связывается с мейотическими хромосомами и регулирует динамику механизма DDR во время сперматогенеза. [13] FMRP, по-видимому, необходим для восстановления повреждений ДНК .
Каждое клеточное деление от сперматогония до сперматиды является неполным; клетки остаются соединенными друг с другом мостиками цитоплазмы, что обеспечивает синхронное развитие. Не все сперматогонии делятся с образованием сперматоцитов; в противном случае запасы сперматогониев иссякнут. Вместо этого сперматогониальные стволовые клетки делятся митотически, производя свои копии, обеспечивая постоянный приток сперматогониев для стимулирования сперматогенеза. [14]
Сперматидогенез – это образование сперматид из вторичных сперматоцитов. Вторичные сперматоциты, образовавшиеся ранее, быстро вступают в мейоз II и делятся, образуя гаплоидные сперматиды. Кратковременность этой стадии означает, что вторичные сперматоциты редко обнаруживаются при гистологических исследованиях.
Во время спермиогенеза сперматиды начинают формировать хвост путем выращивания микротрубочек на одной из центриолей, которая превращается в базальное тельце. Эти микротрубочки образуют аксонему . В дальнейшем центриоль модифицируется в процессе редукции центросомы . [15] Передняя часть хвоста (так называемая средняя часть) утолщается, поскольку митохондрии располагаются вокруг аксонемы для обеспечения энергоснабжения. ДНК сперматид также подвергается упаковке, становясь сильно конденсированной. ДНК сначала упаковывается специфическими основными ядерными белками, которые впоследствии заменяются протаминами во время элонгации сперматид. Образующийся плотно упакованный хроматин транскрипционно неактивен. Аппарат Гольджи окружает теперь конденсированное ядро, становясь акросомой .
Затем созревание происходит под воздействием тестостерона, который удаляет оставшуюся ненужную цитоплазму и органеллы . Избыточная цитоплазма, известная как остаточные тельца , фагоцитируется окружающими клетками Сертоли в семенниках . Полученные сперматозоиды уже созрели, но лишены подвижности. Зрелые сперматозоиды высвобождаются из защитных клеток Сертоли в просвет семенных канальцев в ходе процесса, называемого спермиацией .
Неподвижные сперматозоиды транспортируются к придатку яичка в тестикулярной жидкости , секретируемой клетками Сертоли, с помощью перистальтического сокращения . Находясь в придатке яичка, сперматозоиды приобретают подвижность и становятся способными к оплодотворению. Однако транспорт зрелых сперматозоидов через остальную часть мужской репродуктивной системы достигается за счет сокращения мышц, а не за счет недавно приобретенной подвижности сперматозоидов.
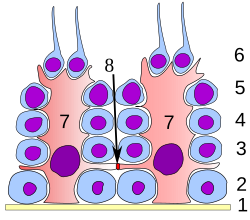
На всех стадиях дифференцировки сперматогенные клетки находятся в тесном контакте с клетками Сертоли, которые, как полагают, обеспечивают структурную и метаболическую поддержку развивающимся сперматозоидам. Единственная клетка Сертоли простирается от базальной мембраны до просвета семенных канальцев, хотя цитоплазматические отростки трудно различить на уровне световой микроскопии.
Клетки Сертоли выполняют ряд функций во время сперматогенеза: они поддерживают развивающиеся гаметы следующими способами:
Молекулы межклеточной адгезии ICAM-1 и растворимый ICAM-1 оказывают антагонистическое действие на плотные соединения , образующие гемато-тестикулярный барьер. [17] Молекулы ICAM-2 регулируют адгезию сперматид на апикальной стороне барьера (по направлению к просвету ). [17]
Процесс сперматогенеза весьма чувствителен к колебаниям окружающей среды, особенно гормонов и температуры. Тестостерон необходим в больших локальных концентрациях для поддержания этого процесса, что достигается за счет связывания тестостерона андрогенсвязывающим белком , присутствующим в семенных канальцах. Тестостерон вырабатывается интерстициальными клетками, также известными как клетки Лейдига , которые расположены рядом с семенными канальцами.
Семенной эпителий чувствителен к повышенной температуре у людей и некоторых других видов, и на него отрицательно влияют температуры, превышающие нормальную температуру тела. Кроме того, у большинства млекопитающих сперматогонии не достигают зрелости при температуре тела, поскольку β-полимераза и сперматогенная рекомбиназа нуждаются в определенной оптимальной температуре. [18] Следовательно, яички расположены вне тела в кожном мешочке, называемом мошонкой . Оптимальная температура поддерживается на уровне 2 °С ( человек ) (8 °С мышь ) ниже температуры тела. Это достигается за счет регуляции кровотока [19] и позиционирования кремастерных мышц и гладких мышц дартоса в мошонке по направлению к теплу тела и вдали от него .
Одним из важных механизмов является теплообмен между артериальным и венозным потоками крови яичек. Специализированные анатомические конструкции состоят из двух зон извилистости внутренней семенной артерии. Такое анатомическое расположение продлевает время контакта и теплообмена между артериальными и венозными кровотоками яичка и может частично объяснить температурный градиент между аортальной и артериальной кровью яичек, наблюдаемый у собак и баранов. Причем снижение пульсового давления происходит в проксимальной трети извитой длины внутренней семенной артерии. [ нужны разъяснения ] [20] [21] Более того, снижается активность сперматогенной рекомбиназы, и это считается важным фактором дегенерации яичек. [ необходимо разъяснение ] [22]
Дефицит диеты (например, витаминов B, E и A), анаболических стероидов , металлов (кадмия и свинца), рентгеновского облучения, диоксина , алкоголя и инфекционных заболеваний также отрицательно влияет на скорость сперматогенеза. [23] Кроме того, мужская зародышевая линия чувствительна к повреждению ДНК, вызванному окислительным стрессом, и это повреждение, вероятно, оказывает существенное влияние на оплодотворение и беременность. [24] Воздействие пестицидов также влияет на сперматогенез. [25]
Гормональный контроль сперматогенеза варьируется у разных видов. У людей этот механизм до конца не изучен; Однако известно, что инициация сперматогенеза происходит в период полового созревания за счет взаимодействия гипоталамуса , гипофиза и клеток Лейдига . Если гипофиз удален, сперматогенез все равно может быть инициирован фолликулостимулирующим гормоном (ФСГ) и тестостероном . [26] В отличие от ФСГ, лютеинизирующий гормон (ЛГ), по-видимому, играет небольшую роль в сперматогенезе, за исключением индукции выработки тестостерона гонадами. [26] [27]
ФСГ стимулирует как выработку андрогенсвязывающего белка (АБП) клетками Сертоли , так и образование гемато -тестикулярного барьера . АД необходим для концентрации тестостерона на достаточно высоком уровне, чтобы инициировать и поддерживать сперматогенез. Интратестикулярные уровни тестостерона в 20–100 или 50–200 раз выше, чем концентрация, обнаруженная в крови, хотя среди здоровых мужчин существуют различия в 5–10 раз. [28] [29] Производство тестостерона не остается постоянным в течение дня, а следует циркадному ритму. Максимальный пик тестостерона приходится на 8 часов утра, что объясняет, почему мужчины часто страдают от утренней эрекции. У молодых мужчин пики тестостерона выше. ФСГ может инициировать секвестрацию тестостерона в яичках, но после его выработки для поддержания сперматогенеза требуется только тестостерон. [26] Однако повышение уровня ФСГ увеличит выработку сперматозоидов за счет предотвращения апоптоза сперматогониев типа А. Гормон ингибин снижает уровень ФСГ. Исследования на моделях грызунов показывают, что гонадотропины (как ЛГ, так и ФСГ) поддерживают процесс сперматогенеза, подавляя проапоптотические сигналы и, следовательно, способствуют выживанию сперматогенных клеток. [30]
Сами клетки Сертоли опосредуют часть сперматогенеза посредством выработки гормонов. Они способны вырабатывать гормоны эстрадиол и ингибин. Клетки Лейдига также способны производить эстрадиол в дополнение к основному продукту – тестостерону. Было обнаружено, что эстроген необходим для сперматогенеза у животных. [31] [32] Однако у мужчины с синдромом нечувствительности к эстрогену (дефектный ERα ) было обнаружено, что он производит сперму с нормальным количеством сперматозоидов , хотя и с аномально низкой жизнеспособностью сперматозоидов ; неясно, был ли он бесплоден или нет. [33] Слишком высокие уровни эстрогена могут быть вредны для сперматогенеза из-за подавления секреции гонадотропинов и, как следствие, увеличения выработки интратестикулярного тестостерона. [34] Связь между сперматогенезом и уровнем пролактина, по-видимому, умеренная, при этом оптимальные уровни пролактина отражают эффективное производство спермы. [27] [35]
Нарушения сперматогенеза могут вызвать олигоспермию , которая представляет собой сперму с низкой концентрацией сперматозоидов [36] и является частым признаком мужского бесплодия .