
В стереохимии стереоизомерия , или пространственная изомерия , — это форма изомерии , при которой молекулы имеют одинаковую молекулярную формулу и последовательность связанных атомов (конституцию), но различаются трехмерной ориентацией своих атомов в пространстве. [1] [2] Это контрастирует со структурными изомерами , которые имеют одну и ту же молекулярную формулу, но связи или их порядок различаются. По определению, молекулы, являющиеся стереоизомерами друг друга, представляют собой один и тот же структурный изомер. [3]
Энантиомеры , также известные как оптические изомеры , представляют собой два стереоизомера, которые связаны друг с другом отражением: они представляют собой зеркальные изображения друг друга, которые не могут накладываться друг на друга. Человеческие руки являются макроскопическим аналогом этого. Каждый стереогенный центр в одном имеет противоположную конфигурацию в другом. Два соединения, являющиеся энантиомерами друг друга, имеют одинаковые физические свойства, за исключением направления, в котором они вращают поляризованный свет, и того, как они взаимодействуют с различными оптическими изомерами других соединений. В результате разные энантиомеры соединения могут иметь существенно разные биологические эффекты. Чистые энантиомеры также проявляют явление оптической активности и могут быть разделены только с использованием хирального агента. В природе присутствует только один энантиомер большинства хиральных биологических соединений, таких как аминокислоты (кроме глицина , который является ахиральным). Оптически активное соединение имеет две формы: форму D -(+) и форму L -(-).
Диастереомеры представляют собой стереоизомеры, не связанные между собой операцией отражения. [4] Они не являются зеркальным отражением друг друга. К ним относятся мезосоединения , цис - транс- изомеры , EZ-изомеры и неэнантиомерные оптические изомеры . Диастереомеры редко имеют одинаковые физические свойства. В примере, показанном ниже, мезоформа винной кислоты образует диастереомерную пару как с лево-, так и с декстровинной кислотой, которые образуют энантиомерную пару.
Обозначения D- и L- вышеприведенных изомеров не совпадают с более распространенными обозначениями d- и l- , что объясняет, почему они могут показаться перевернутыми тем, кто знаком только с последним соглашением об именах.
Проекцию Фишера можно использовать для различения молекул L и D. Хиральность (химия) . Например, по определению, в проекции Фишера предпоследний углерод D-сахара изображен с водородом слева и гидроксилом справа. L-сахара будут показаны с водородом справа и гидроксилом слева.
Другой относится к оптическому вращению , при взгляде на источник света вращение плоскости поляризации может быть либо вправо (правовращательное — d-поворотное, обозначаемое (+), по часовой стрелке), либо влево (левовращающее). - l-вращающийся, обозначаемый (-), против часовой стрелки) в зависимости от того, какой стереоизомер является доминирующим. Например, сахароза и камфора являются d-вращающими, тогда как холестерин L-вращающими.
Стереоизомерия двойных связей возникает потому, что вращение вокруг двойной связи ограничено, в результате чего заместители остаются неподвижными относительно друг друга. [5] Если два заместителя хотя бы на одном конце двойной связи одинаковы, то стереоизомер отсутствует и двойная связь не является стереоцентром, например, пропен, CH 3 CH=CH 2 , где два заместителя на одном конце оба являются Х. [6]
Традиционно стереохимию двойной связи описывали как цис (лат. на этой стороне) или транс (лат. поперек), в зависимости от относительного положения заместителей по обе стороны двойной связи. Простым примером цис - транс- изомерии являются 1,2-дизамещенные этены, подобные изомерам дихлорэтена (C 2 H 2 Cl 2 ), показанным ниже. [7]
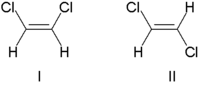
Молекула I представляет собой цис -1,2-дихлорэтен, а молекула II представляет собой транс -1,2-дихлорэтен. Из-за случайной двусмысленности ИЮПАК принял более строгую систему, в которой заместителям на каждом конце двойной связи назначается приоритет в зависимости от их атомного номера . Если высокоприоритетные заместители находятся по одну сторону связи, ей присваивается Z (нем. zusammen , вместе). Если они находятся на противоположных сторонах, то это Е (нем. entgegen , противоположный). [8] Поскольку хлор имеет больший атомный номер, чем водород, это группа с наивысшим приоритетом. [9] Используя это обозначение для названия молекул, изображенных выше, молекула I представляет собой (Z)-1,2-дихлорэтен, а молекула II представляет собой (E)-1,2-дихлорэтен. Это не тот случай, когда Z и цис или E и транс всегда взаимозаменяемы. Рассмотрим следующий фторметилпентен:
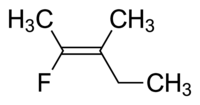
Правильное название для этой молекулы — либо транс -2-фтор-3-метилпент-2-ен, поскольку алкильные группы, образующие основную цепь (т.е. метил и этил), расположены поперек двойной связи друг от друга, либо (Z) -2-фтор-3-метилпент-2-ен, поскольку группы с наивысшим приоритетом на каждой стороне двойной связи находятся на одной и той же стороне двойной связи. Фтор — группа с наивысшим приоритетом на левой стороне двойной связи, а этил — группа с наивысшим приоритетом на правой стороне молекулы.
Термины цис и транс также используются для описания относительного положения двух заместителей в кольце; цис , если на одной стороне, иначе транс . [10] [11] [12]
Конформационная изомерия — это форма изомерии, которая описывает явление молекул с одинаковой структурной формулой, но разной формы из-за вращения вокруг одной или нескольких связей. [13] [14] [15] Различные конформации могут иметь разную энергию, обычно могут взаимопревращаться и очень редко поддаются изолированию. Например, существует множество конформаций циклогексана (циклогексан является важным промежуточным продуктом для синтеза нейлона-6,6), включая конформацию кресла , в которой четыре атома углерода образуют «место» кресла, один атом углерода «спинка» стула, а один атом углерода — «подставка для ног»; и конформация лодочки , конформация лодочки представляет собой максимум энергии на конформационном маршруте между двумя эквивалентными формами стула; однако оно не представляет собой переходное состояние этого процесса, поскольку существуют пути с более низкой энергией. Конформационная инверсия замещенных циклогексанов представляет собой очень быстрый процесс при комнатной температуре с периодом полураспада 0,00001 секунды. [16] [17]
Есть некоторые молекулы, которые можно выделить в нескольких конформациях из-за больших энергетических барьеров между различными конформациями. 2,2',6,6'-Тетразамещенные бифенилы могут относиться к этой последней категории.
Аномерия - это идентичность кольцевых структур с одинарной связью, где «цис» или «Z» и «транс» или «E» (геометрическая изомерия) должны обозначать замены в атоме углерода, которые также отображают идентичность хиральности; поэтому аномеры имеют атомы углерода, которые имеют геометрическую изомерию и оптическую изомерию ( энантиомерию ) на одном или нескольких атомах углерода кольца. [18] [19] [20] [21] Аномеры называются «альфа» или «аксиальные» и «бета» или «экваториальные» при замене циклической кольцевой структуры, которая имеет одинарные связи между атомами углерода кольца, например, гидроксильную группу, метилгидроксильную группу, метоксигруппу или другую пиранозную или фуранозную группу, которые представляют собой типичные замены одинарной связи, но не ограничиваются ими. [22] Осевая геометрическая изомерия будет перпендикулярна (90 градусов) к базовой плоскости, а экваториальная будет находиться на расстоянии 120 градусов от осевой связи или отклоняться на 30 градусов от базовой плоскости. [23]
Атропоизомеры представляют собой стереоизомеры, возникающие в результате затрудненного вращения вокруг одинарных связей , где барьер вращения стерической деформации достаточно высок, чтобы обеспечить изоляцию конформеров. [24] [25]
Правило Ле Бель-Вант-Гоффа гласит, что для структуры с n асимметричными атомами углерода возможно максимум 2 n различных стереоизомеров. Например, D -глюкоза представляет собой альдогексозу и имеет формулу C 6 H 12 O 6 . Четыре из шести атомов углерода стереогенны, что означает, что D -глюкоза является одним из 2 4 =16 возможных стереоизомеров. [26] [27]