Структурная биология , по определению Журнала структурной биологии , занимается структурным анализом живого материала (сформированного, состоящего из живых клеток и/или поддерживаемого и усовершенствованного живыми клетками) на каждом уровне организации. [1]
Ранние структурные биологи на протяжении 19 и начала 20 веков в основном могли изучать структуры только до предела остроты зрения невооруженным глазом и с помощью увеличительных очков и световых микроскопов. В 20 веке было разработано множество экспериментальных методов для изучения трехмерных структур биологических молекул. Наиболее известные методы — рентгеновская кристаллография , ядерный магнитный резонанс и электронная микроскопия . Благодаря открытию рентгеновских лучей и их применению к кристаллам белков структурная биология произвела революцию, поскольку теперь ученые могли получать трехмерные структуры биологических молекул в атомных деталях. [2] Аналогично, ЯМР-спектроскопия позволила получить информацию о структуре и динамике белка. [3] Наконец, в 21 веке в электронной микроскопии также произошла радикальная революция с развитием более когерентных источников электронов, коррекции аберраций для электронных микроскопов и программного обеспечения для реконструкции, которое позволило успешно реализовать криоэлектронную микроскопию с высоким разрешением, тем самым позволив исследование отдельных белков и молекулярных комплексов в трехмерном пространстве с ангстремным разрешением.
С развитием этих трех методов область структурной биологии расширилась и стала также отраслью молекулярной биологии , биохимии и биофизики , занимающейся молекулярной структурой биологических макромолекул (особенно белков , состоящих из аминокислот , РНК или ДНК , состоящих из состоят из нуклеотидов и мембран , состоящих из липидов ), как они приобретают имеющиеся у них структуры и как изменения в их структурах влияют на их функции. [4] Этот предмет представляет большой интерес для биологов, поскольку макромолекулы выполняют большинство функций клеток , и только свертываясь в определенные трехмерные формы, они способны выполнять эти функции. Эта архитектура, « третичная структура » молекул, сложным образом зависит от основного состава каждой молекулы, или « первичной структуры ». При более низком разрешении такие инструменты, как томография FIB-SEM, позволили лучше понять клетки и их органеллы в трех измерениях, а также то, как каждый иерархический уровень различных внеклеточных матриц способствует функционированию (например, в кости). В последние несколько лет также стало возможным прогнозировать высокоточные физические молекулярные модели , дополняющие экспериментальное изучение биологических структур. [5] Вычислительные методы, такие как моделирование молекулярной динамики, могут использоваться в сочетании со стратегиями определения эмпирической структуры для расширения и изучения структуры, конформации и функции белка. [6]


В 1912 году Макс фон Лауэ направил рентгеновские лучи на кристаллизованный сульфат меди, создав дифракционную картину . [7] Эти эксперименты привели к развитию рентгеновской кристаллографии и ее использованию при исследовании биологических структур. [5] В 1951 году Розалинда Франклин и Морис Уилкинс использовали рентгенограммы, чтобы получить первое изображение дезоксирибонуклеиновой кислоты (ДНК). Фрэнсис Крик и Джеймс Уотсон смоделировали двойную спиральную структуру ДНК, используя тот же метод в 1953 году, и получили Нобелевскую премию по медицине вместе с Уилкинсом в 1962 году. [8]
Кристаллы пепсина были первыми белками, кристаллизованными для использования в дифракции рентгеновских лучей Теодором Сведбергом , получившим в 1962 году Нобелевскую премию по химии. [9] Первая третичная структура белка , структура миоглобина , была опубликована в 1958 году Джоном Кендрю . [10] За это время моделирование белковых структур проводилось с использованием моделей из пробкового дерева или проволоки . [11] С изобретением программного обеспечения для моделирования, такого как CCP4, в конце 1970-х годов, [12] моделирование теперь выполняется с помощью компьютера. Недавние разработки в этой области включают создание рентгеновских лазеров на свободных электронах , позволяющих анализировать динамику и движение биологических молекул [13] , а также использование структурной биологии в помощь синтетической биологии . [14]
В конце 1930-х и начале 1940-х годов сочетание работ Исидора Раби , Феликса Блоха и Эдварда Миллса Перселла привело к развитию ядерного магнитного резонанса (ЯМР). В настоящее время ЯМР твердого тела широко используется в области структурной биологии для определения структуры и динамической природы белков ( ЯМР белков ). [15]
В 1990 году Ричард Хендерсон получил первое трехмерное изображение бактериородопсина с высоким разрешением с помощью криогенной электронной микроскопии (крио-ЭМ). [16] С тех пор крио-ЭМ становится все более популярным методом определения трехмерных структур биологических изображений с высоким разрешением. [17]
Совсем недавно были разработаны вычислительные методы для моделирования и изучения биологических структур. Например, молекулярная динамика (МД) обычно используется для анализа динамических движений биологических молекул. В 1975 году в журнале Nature было опубликовано первое моделирование процесса биологической складки с использованием МД. [18] Недавно предсказание структуры белка было значительно улучшено благодаря новому методу машинного обучения под названием AlphaFold. [19] Некоторые утверждают, что вычислительные подходы начинают лидировать в области исследований в области структурной биологии. [20]
Биомолекулы слишком малы, чтобы их можно было рассмотреть в деталях даже с помощью самых совершенных световых микроскопов . Методы, которые структурные биологи используют для определения их структуры, обычно включают измерения огромного количества идентичных молекул одновременно. Эти методы включают в себя:
Чаще всего исследователи используют их для изучения « нативных состояний » макромолекул. Но вариации этих методов также используются для наблюдения за возникающими или денатурированными молекулами, принимающими или возвращающими свое исходное состояние. См. сворачивание белка .
Третий подход, который структурные биологи используют для понимания структуры, — это биоинформатика , позволяющая искать закономерности среди разнообразных последовательностей , которые приводят к определенным формам. Исследователи часто могут вывести аспекты структуры интегральных мембранных белков на основе топологии мембраны , предсказанной анализом гидрофобности . См. предсказание структуры белка .
Структурные биологи внесли значительный вклад в понимание молекулярных компонентов и механизмов, лежащих в основе заболеваний человека. Например, криоЭМ и оцЯМР использовались для изучения агрегации амилоидных фибрилл, которые связаны с болезнью Альцгеймера , болезнью Паркинсона и диабетом II типа . [21] В дополнение к амилоидным белкам ученые использовали крио-ЭМ для создания моделей тау-нитей с высоким разрешением в мозгу пациентов с болезнью Альцгеймера, что может помочь в разработке более эффективных методов лечения в будущем. [22] Инструменты структурной биологии также можно использовать для объяснения взаимодействия между патогенами и хозяевами. Например, инструменты структурной биологии позволили вирусологам понять, как оболочка ВИЧ позволяет вирусу уклоняться от иммунных реакций человека. [23]
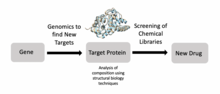
Структурная биология также является важным компонентом открытия лекарств . [24] Ученые могут идентифицировать цели с помощью геномики, изучать эти цели с помощью структурной биологии и разрабатывать лекарства, подходящие для этих целей. В частности, лиганд- ЯМР , масс-спектрометрия и рентгеновская кристаллография обычно используются в процессе открытия лекарств. Например, исследователи использовали структурную биологию, чтобы лучше понять Met , белок, кодируемый протоонкогеном, который является важной мишенью лекарств при раке . [25] Аналогичные исследования были проведены для целей лечения ВИЧ-инфекции для лечения людей со СПИДом . [24] Исследователи также разрабатывают новые противомикробные препараты для лечения микобактериальных инфекций, используя открытие лекарств, основанных на структуре. [24]
{{cite web}}: CS1 maint: bot: original URL status unknown (link)