Микотоксин Т-2 представляет собой трихотеценовый микотоксин . Это природный побочный продукт плесени Fusarium spp. грибок , токсичный для человека и животных. Клиническое состояние, которое он вызывает, представляет собой алиментарную токсическую алейкию и множество симптомов, связанных с такими разнообразными органами, как кожа, дыхательные пути и желудок. Проглатывание может произойти при употреблении в пищу заплесневелых цельных зерен . Т-2 может впитываться через кожу человека. [2] Хотя никаких значительных системных эффектов не ожидается после контакта с кожей в обычных сельскохозяйственных или жилых условиях, нельзя исключать локальное воздействие на кожу. Следовательно, контакт Т-2 с кожей должен быть ограничен.
Алиментарно-токсическая алейкия (АТА) — заболевание, вызываемое трихотеценами типа микотоксина Т-2, — унесло жизни многих тысяч граждан СССР в Оренбургской области в 1940-е годы. Сообщалось, что уровень смертности составил 10% от всего населения в этом районе. В 1970-х годах было высказано предположение, что причиной массового отравления стало употребление зараженной пищи. Из-за Второй мировой войны уборка зерновых задержалась, а продовольствия в России стало не хватать. Это привело к потреблению зерна, зараженного плесенью Fusarium , выделяющей микотоксин Т-2. [3]
В 1981 году госсекретарь США Александр Хейг и его преемник Джордж П. Шульц обвинили Советский Союз в использовании микотоксина Т-2 в качестве химического оружия, известного как « желтый дождь » в Лаосе (1975–81), Кампучии (1979–1981 гг.). 81) и Афганистане (1979–81), где оно, как утверждается, привело к тысячам жертв. [4] Хотя некоторые американские эксперты по химическому оружию утверждают, что идентифицировали образцы «желтого дождя» из Лаоса как трихотецены, другие эксперты полагают, что это воздействие произошло из-за естественного микотоксина Т-2 в загрязненных пищевых продуктах. [5] Другая альтернативная теория была разработана гарвардским биологом Мэтью Мезельсоном , который предположил, что «желтый дождь», обнаруженный в Юго-Восточной Азии, возник из экскрементов джунглевых пчел. [6] Первым подтверждением этой теории стало обнаружение высокого уровня пыльцы в собранных образцах, придающих веществу желтый цвет. Было также обнаружено, что джунглевые пчелы в этом районе летают коллективно в больших количествах на слишком большой высоте, чтобы их можно было легко увидеть, создавая ливни фекалий, которые можно было принять за брызги с самолетов. [7] Дальнейшее тестирование позже показало, что маслянистая жидкость на самом деле была наполненными пыльцой фекалиями джунглевых пчел. [6] Похожий случай был выявлен в Китае, и в этом случае причиной явления также стали пчелиные экскременты. [8] Несмотря на этот убедительный анализ, Соединенные Штаты не отказались от своих обвинений и заявляют, что проблема не решена полностью.
Микотоксин Т-2 также считается причиной синдрома войны в Персидском заливе . Американские войска страдали от симптомов, похожих на микотоксикоз, после того, как иракская ракета взорвалась в военном лагере США в Саудовской Аравии во время операции «Буря в пустыне» во время войны в Персидском заливе в 1991 году. Было показано, что Ирак исследовал трихотеценовые микотоксины, среди других веществ, и, таким образом, был способен владеть им и использовать его в химической войне . Тем не менее, большая часть ключевой информации об этих инцидентах остается засекреченной, в результате чего эти вопросы остаются нерешенными. [9]
Это соединение имеет тетрациклическую сесквитерпеноидную кольцевую систему 12,13-эпокситрихотена, что роднит его с трихотеценами. [10] Эти соединения, как правило, очень стабильны и не разлагаются во время хранения/измельчения и приготовления/обработки пищевых продуктов. Они также не разрушаются при высоких температурах. Это соединение имеет эпоксидное кольцо и несколько ацетильных и гидроксильных групп на боковых цепях. Эти особенности в основном ответственны за биологическую активность соединения и делают его высокотоксичным. Микотоксин Т-2 способен ингибировать синтез ДНК и РНК in vivo и in vitro [11] и может индуцировать апоптоз . [12] Однако in vivo это соединение быстро метаболизируется до микотоксина HT-2 (основного метаболита ). [13]
Токсичность токсина Т-2 обусловлена его 12,13-эпоксидным кольцом. [14] Эпоксиды в целом являются токсичными соединениями; они реагируют с нуклеофилами , а затем подвергаются дальнейшим ферментативным реакциям . Реакционная способность эпоксидов может привести к реакциям с эндогенными соединениями и клеточными компонентами, такими как основания ДНК и белки. [15] Эти реакции могли быть причиной замеченного действия и эффектов микотоксина Т-2. Токсическое соединение влияет на метаболизм мембранных фосфолипидов , приводит к повышению активности липидпероксидазы печени и оказывает ингибирующее действие на синтез ДНК и РНК . Кроме того, он может связываться с неотъемлемой частью 60-й субъединицы рибосомы, пептидилтрансферазой , тем самым ингибируя синтез белка . Считается, что эти эффекты являются объяснением того, что токсин Т-2 вызывает апоптоз (гибель клеток) в различных тканях, таких как иммунная система , ткани желудочно-кишечного тракта, а также ткани плода. Что касается апоптоза, было замечено, что уровень проапоптотического фактора Bas (Bcl-2-ассоциированный белок X) был повышен, а уровень Bcl-xl, антиапоптотического фактора, был снижен в хондоцитах человека (хрящевые ткани) . клетки). При воздействии микотоксина Т-2. Кроме того, был увеличен уровень Fas, антигена клеточной поверхности, связанного с апоптозом, и p53, белка, регулирующего клеточный цикл.
Микотоксин Т-2 естественным образом вырабатывается грибами Fusarium, наиболее важными видами которых являются: F. sporotrichioides , F. langsethiae , F. acuminatum и F. poae . Эти грибы встречаются в таких зернах, как ячмень , пшеница и овес . Производство этого соединения для исследовательских и коммерческих целей обычно осуществляется путем культивирования некоторых штаммов грибов, продуцирующих микотоксин Т-2, на чашках с агаром . На этих чашках с агаром грибы выглядят порошкообразными и могут выделять значительные количества микотоксина Т-2. Для выделения соединения обычно используют жидкостную хроматографию высокого давления (ВЭЖХ). [16]
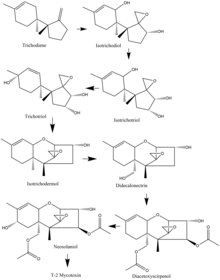
У видов Fusarium биосинтез микотоксина Т-2 часто начинается с триходиена, и многие виды имеют общий путь окисления и циклизации . Например, у видов F. sporotrichioides важные стадии окисления начинаются с триходиена и переходят к изотриходиолу. Отсюда одиннадцатый атом углерода окисляется с образованием изотрихотриола. Затем девятый углерод окисляется и образуется трихотриол, который затем циклизуется с образованием изотриходермола. После этого пятнадцатый углерод окисляется с образованием дидекалонектрина, что приводит к окислению четвертого углерода и образованию диацетоксисцирпенола. Предпоследний этап — окисление восьмого атома углерода с образованием неозоланиола, который затем подвергается небольшой модификации с образованием токсина Т-2. [17]
Люди и животные обычно подвергаются воздействию микотоксинов Т-2 через пищу. Некоторые зерна могут содержать токсин, что делает их угрозой для здоровья человека и экономическим бременем. [18] В отличие от большинства биологических токсинов, микотоксин Т-2 может всасываться через неповрежденную кожу. Соединение может доставляться через пищу, воду, капли, аэрозоли и дым из различных систем рассеивания. Это делает его потенциальным биологическим оружием , однако для получения смертельной дозы требуется большое количество этого соединения . Микотоксин Т-2 имеет ЛД 50 примерно 1 миллиграмм на килограмм массы тела.
По оценкам EFSA , среднее воздействие Т-2 в ЕС составляет от 12 до 43 нг/кг массы тела/день. [19] Этот диапазон ниже TDI в 100 нг/кг массы тела для суммы токсинов HT-2 и T-2, который используется EFSA.
Микотоксин Т-2 распределяется равномерно по всему организму, не отдавая предпочтение определенному органу или месту. У грызунов пик концентрации в плазме происходит примерно через тридцать минут после воздействия, а в одном исследовании период полураспада токсина Т-2 составил менее двадцати минут. В другом исследовании на свиньях распределение после четырехчасовой внутривенной инъекции составило 15–24% в желудочно-кишечном тракте и 4,7–5,2% в различных других тканях. [20]
После абсорбции и распределения в различных тканях микотоксин Т-2 проходит различные метаболические реакции, прежде чем выйти из организма. Исследования in vivo показали, что наиболее протекающими реакциями являются гидролиз сложного эфира и гидроксилирование изовалериловой группы. Также происходят деооксидирование и конъюгация глюкуронидов . Ht-2 является основным метаболитом. Предполагается, что в гидроксилировании участвует ферментный комплекс цитохрома p450. Триол Т-2 и тетраол Т-2, скорее всего, образуются посредством ацетилхолинэстеразы . Некоторые метаболические реакции микотоксина осуществляются микрофлорой кишечника. Образующиеся метаболиты в этих реакциях зависят от вида и pH. Однако расщепление сложного эфира осуществляется самим млекопитающим, а не микрофлорой. В эритроцитах микотоксин Т-2 метаболизируется до неозоланиола, а в лейкоцитах — до НТ-2 путем гидролиза, катализируемого карбоксилэстеразами.
После всасывания, распределения и метаболизма микотоксин Т-2 выводится довольно быстро, при этом 80–90% его выводится в течение 48 часов. [20] Основными методами выведения, по-видимому, являются моча и фекалии, [21] где выведение через желчь в значительной степени способствует выведению с фекалиями. [14] В выделениях также очень мало родительского микотоксина Т-2, а это означает, что большая часть исходного соединения метаболизируется заранее. [21]
Т-2 очень токсичен при вдыхании. Острые токсические симптомы включают рвоту, диарею, раздражение кожи, зуд, сыпь, волдыри, кровотечение и одышку . [22] Если человек подвергается воздействию Т-2 в течение длительного периода, развивается пищевая токсическая алейкия (АТА).
Сначала больной испытывает чувство жжения во рту, горле и желудке. Через несколько дней у человека разовьется острый гастроэнтерит , который продлится от 3 до 9 дней. В течение 9 недель костный мозг будет медленно деградировать. Также кожа начинает кровоточить и снижается общее количество лейкоцитов . Могут возникнуть проблемы с нервной системой.
В конечном итоге могут возникнуть следующие симптомы: высокая температура, петехиальные кровоизлияния , некроз мышц и кожи, бактериальная инфекция некротизированной ткани, увеличение лимфатических узлов . Существует вероятность удушья из-за отека гортани и стеноза голосовой щели . Недостаток кислорода является тогда причиной смерти. В противном случае больной умрет от бронхопневмонии и легочного кровотечения. [23]
Микотоксин Т-2 также токсичен для животных. Соединение известно своим летальным и сублетальным действием на сельскохозяйственных животных. Его часто обнаруживают в зараженных зерновых культурах, которыми кормят этих животных. [24] Большинство токсических эффектов свойственны людям и животным. После воздействия на эмбрионы рыб данио концентрации 20 мкмоль/л или выше уровень пороков развития и смертности увеличивался. Пороки развития включали деформации хвоста, сердечно-сосудистые дефекты и изменения в поведении на ранних этапах жизни. Это результат увеличения количества эпоксидов, вызывающих апоптоз клеток. [25] Другие исследования показали, что Т-2-токсин вызывает перекисное окисление липидов у крыс после его скармливания им. В результате воздействия токсина Т-2 у нескольких видов млекопитающих наблюдалось повышение уровня активных форм кислорода (АФК). Однако, несмотря на общее вредное воздействие токсина, в исследовании, проведенном на различных моделях культур клеток печени, полученных из кур, не было обнаружено никаких изменений в окислительно-восстановительном статусе клеток. [26]
Это соединение также снижает плодовитость овец и телок. Исследования показали, что высокая доза Т-2 задерживает овуляцию из -за задержки созревания фолликула . Это, возможно, замедляет последующую лютеинизацию , что делает невозможным зачатие самок животных.
Т-2 также оказывает влияние на плодовитость быков. В 1998 году было обнаружено, что заплесневелое сено влияет на качество спермы быков. Анализ заплесневелого сена показал наличие Т-2. Соединение уменьшало подвижность сперматозоидов и уровень тестостерона, а также увеличивало частоту морфологических аномалий в сперматозоидах.
Печень является еще одной мишенью для микотоксина. Это один из первых органов, через который проходит соединение после приема внутрь. Здесь он вызывает снижение экспрессии белков CYP1A у кроликов, свиней и крыс. Активность CYP3A снижается и у свиней. Эти ферменты помогают метаболизировать лекарства, которые проходят через печень. Снижение активности может привести к повышению содержания неметаболизированного препарата в плазме. Это может иметь опасные последствия для здоровья животного. [27]
Все упомянутые эффекты возникают при приеме Т-2 в высоких дозах. Животные способны метаболизировать это соединение с помощью ферментов семейства CYP3A, как и люди.
На данный момент специфической терапии отравлений микотоксином Т-2 не существует. [21] За воздействием микотоксина обычно следует стандартизированная обработка токсичных соединений с целью снижения воздействия токсина. Сюда входит использование активированного угля , который обладает высокой связывающей способностью: 0,48 мг микотоксина Т-2 на 1 мг угля. [21] При контакте с кожей используется мыло и вода, чтобы уменьшить кожное воздействие. [21] Считается , что антиоксиданты являются своего рода профилактикой и обладают полезными свойствами. [20]
В настоящее время микотоксины Т-2 не имеют других применений, кроме военных; однако есть некоторые возможные терапевтические применения. Благодаря своим способностям исследования показывают возможность использования микотоксина в качестве стимуляторов роста, антибиотиков , противовирусных средств , противолейкемических и противомалярийных средств . [20]
Желтый дождь – это экскременты лесных пчел. Она желтая из-за переваренной пыльцы, а дождь падает из роев пчел, находящихся слишком высоко, чтобы их можно было увидеть. Его теория оказывается совершенно верной. Собственные исследования правительства, до сих пор неопубликованные, доказывают, что источником являются пчелы, а не бомбы.