Существует три группы галогенидов индия : тригалогениды, моногалогениды и несколько промежуточных галогенидов . В моногалогенидах степень окисления индия равна +1, а их собственные названия: фторид индия (I), хлорид индия (I), бромид индия (I) и йодид индия (I).
Промежуточные галогениды содержат индий со степенями окисления +1, +2 и +3.
Во всех тригалогенидах степень окисления индия равна +3, а их собственные названия — фторид индия (III), хлорид индия (III), бромид индия (III) и иодид индия (III). Тригалогениды являются кислотами Льюиса . Трихлорид индия является отправной точкой в производстве триметилиндия , который используется в полупроводниковой промышленности.
InF 3 представляет собой белое твердое вещество , т. пл. 1170°С. В его структуре содержится 6-координатный индий.
InCl 3 представляет собой белое твердое вещество, т.пл. 586°С. Его получают окислением индия хлором. [1] Он изоструктурен AlCl 3 .
InBr 3 представляет собой бледно-желтое твердое вещество, т.пл. 435°С. Он изоструктурен AlCl 3 . Его готовят путем объединения элементов. [2] InBr 3 находит некоторое применение в органическом синтезе в качестве водостойкой кислоты Льюиса. [3]
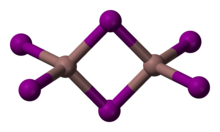
InI 3 представляет собой желтое твердое вещество. Его получают выпариванием раствора индия в HI. [4] Известны отдельные желтые и красные формы. Красная форма переходит в желтую при 57 °C. Структура красной формы не была определена с помощью рентгеновской кристаллографии , однако спектроскопические данные показывают, что индий может быть шестикоординатным. [5] Желтая форма состоит из In 2 I 6 с 4-мя координатными индиевыми центрами. Он используется в качестве «поглотителя йода» в процессе Cativa . [ нужна цитата ]
Известно удивительное количество промежуточных хлоридов и бромидов, но только один йодид и ни одного дифторида. Вместо очевидной степени окисления +2 эти соединения содержат индий в степенях окисления +1 и +3. Таким образом, дииодид описывается как In I In III X 4 . Спустя некоторое время было установлено существование соединений, содержащих анион In 2 Br.2-6были подтверждены, которые содержат связь индий-индий. Ранние работы по хлоридам и бромидам включали исследование бинарных фазовых диаграмм тригалогенидов и родственных им моногалогенидов. Многие из соединений изначально были ошибочно идентифицированы, поскольку многие из них неконгруэнтны и разлагаются перед плавлением. Существование и структура большинства ранее известных хлоридов и бромидов либо подтверждены рентгеновскими дифракционными исследованиями, либо ушли в историю. Возможно, самым неожиданным случаем ошибочной идентификации стал неожиданный результат: тщательное повторное исследование бинарной диаграммы состояния InCl/InCl 3 не обнаружило InCl 2 . [6]
Причиной такого обилия соединений является то, что индий образует 4- и 6-координатные анионы, содержащие индий(III), например, InBr.−4, ИнКл3-6а также анион В 2 Br2-6который неожиданно содержит связь индий-индий.
In 7 Cl 9 представляет собой твердое вещество желтого цвета, стабильное до 250 °C, формула которого составляет In I 6 (In III Cl 6 )Cl 3 [7]
In 7 Br 9 имеет структуру, аналогичную In 7 Cl 9 , и может быть сформулирован как In I 6 (In III Br 6 )Br 3 [8]
В 5 Бр 7 представляет собой твердое вещество бледно-желтого цвета. Формулируется В I 3 (В II 2 Br 6 )Br. Анион In II 2 Br 6 имеет затменную этаноподобную структуру с длиной связи металл-металл 270 пм. [9]
In 2 Cl 3 бесцветен и имеет формулу In I 3 In III Cl 6 [10]. Напротив, In 2 Br 3 содержит анион In 2 Br 6 , присутствующий в In 5 Br 7 , и формулируется In I 2 (In II 2 Br 6 ) со структурой, аналогичной Ga 2 Br 3 . [11]
В 4 Бр 7 почти бесцветен с бледно-зеленовато-желтым оттенком. Он светочувствителен (как TlCl и TlBr) и распадается на металлы InBr 2 и In. Это смешанная соль, содержащая InBr.−4и ИнБр3-6анионы, сбалансированные катионами In + . Его формулировка: In I 5 (In III Br 4 ) 2 (In III Br 6 ). Причины искажения решетки объясняются разрыхляющей комбинацией между дважды заполненными ненаправленными орбиталями индия 5s и соседними гибридными орбиталями брома 4p. [12]
В 5 Cl 9 формулируется как In I 3 In III 2 Cl 9 . В 2 кл .3-9анион имеет два 6-координатных атома индия с 3 мостиковыми атомами хлора, биооктаэдры с общими гранями, структуру, аналогичную Cr 2 Cl.2-9и Tl 2 Cl2-9. [13]
InBr 2 представляет собой зеленовато-белое кристаллическое твердое вещество, имеющее формулу In I In III Br 4 . Он имеет ту же структуру, что и GaCl 2 . InBr 2 растворим в ароматических растворителях, и были идентифицированы некоторые соединения, содержащие комплексы η 6 -арена In(I). (См. тактильность для объяснения связей в таких комплексах арен-ион металла). С некоторыми лигандами InBr 2 образует нейтральные комплексы, содержащие связь индий-индий. [14]
InI 2 представляет собой желтое твердое вещество, имеющее формулу In I In III I 4 .
Твердые моногалогениды InCl, InBr и InI нестабильны по отношению к воде, разлагаясь на металлы и частицы индия (III). Они занимают промежуточное положение между соединениями галлия (I), которые более реакционноспособны, и таллием (I), стабильным по отношению к воде. InI является наиболее стабильным. До сравнительно недавнего времени моногалогениды были научной диковинкой, однако с открытием того, что их можно использовать для получения кластерных и цепочечных соединений индия, они теперь привлекают гораздо больший интерес. [15]
InF известен только как нестабильное газообразное соединение.
Форма InCl при комнатной температуре имеет желтый цвет с кубической искаженной структурой NaCl. Красная высокотемпературная (>390 К) форма имеет структуру. [15]
InBr представляет собой красное кристаллическое вещество с температурой плавления 285 °C. Он имеет ту же структуру, что и , с орторомбической искаженной структурой каменной соли. Его можно получить из металлического индия и InBr 3 .
InI представляет собой кристаллическое твердое вещество темно-красного фиолетового цвета. Он имеет ту же структуру, что и . Его можно изготовить путем прямого соединения составляющих его элементов при высокой температуре. Альтернативно его можно получить из InI 3 и металлического индия в кипящем ксилоле. [16] Это наиболее стабильный из твердых моногалогенидов и растворим в некоторых органических растворителях. Растворы InI в смеси пиридин/м-ксилол устойчивы ниже 243 К. [15]
Тригалогениды представляют собой кислоты Льюиса и образуют соединения присоединения с лигандами. Для InF 3 известно несколько примеров, однако для других галогенидов известны аддитивные соединения с тетраэдрической, тригонально-бипирамидальной и октаэдрической координационной геометрией. Галогенид-ионы имеют примеры всех этих геометрий наряду с некоторыми анионами с октаэдрически координированными индием и мостиковыми атомами галогена, In 2 X3-9с тремя мостиковыми атомами галогена и In 2 X−7всего с одним. Кроме того, есть примеры индия с плоско-квадратной геометрией в ионе InX 5 2− . Плоская квадратная геометрия InCl2-5был первым обнаруженным элементом основной группы.
Соли InCl−4, ИнБр−4и ИнИ−4известны. Была получена соль LiInF 4 [17] [18] , однако она имеет необычную слоистую структуру с октаэдрически координированным индиевым центром. Соли InF 6 3− , InCl3-6и ИнБр3-6 [19] все были сделаны.
ИнКл2-5Было обнаружено, что ион имеет квадратно-пирамидальную форму в соли (NEt4) 2 InCl 5 , с той же структурой, что и (NEt 4 ) 2 TlCl 5 , но имеет тригонально-бипирамидальную форму в ацетонитриловом сольвате пентахлориндата тетрафенилфосфония. [20]
ИнБр2-5Ион также был обнаружен квадратно-пирамидальным, хотя и искаженным, в соли Bis(4-хлорпиридиния) [21] и тригонально-бипирамидальным [22] в Bi 37 InBr 48 .
В 2 X−7ионы содержат один мостиковый атом галогена. Из спектров невозможно определить, является ли мост изогнутым или линейным. Хлорид и бромид были обнаружены с помощью масс-спектрометрии электрораспылением. В 2 я−7ион получен в соли CsIn 2 I 7 . [5]
Цезиевые соли In 2 Cl3-9и в 2 комн.3-9оба содержат биядерные анионы с октаэдрически координированными атомами индия. [13]
In I X 2 − образуется при диспропорции иона In 2 X 6 2− . Соли, содержащие In I X2-3были созданы ионы, и их колебательные спектры были интерпретированы как показывающие, что они обладают симметрией C 3v , тригональной пирамидальной геометрией и структурами, подобными изоэлектронному Sn X−3ионы.
Получены соли хлорид-, бромид- и йодид-ионов (Bu 4 N) 2 In 2 X 6 . В неводных растворителях этот ион диспропорционируется с образованием In I X−2и В III X−4.
После открытия In 2 Br 6 2− в результате реакции дигалогенидов индия с нейтральными лигандами образовался ряд родственных нейтральных соединений, содержащих ядро In II 2 X 4 . [14] Некоторые химики называют эти аддукты, когда они используются в качестве отправной точки для синтеза кластерных соединений, «In 2 X 4 », например аддукт TMEDA . [23]