Триплетный кислород , 3 O 2 , относится к основному электронному состоянию молекулярного кислорода (дикислорода) с S = 1 . Молекулы триплетного кислорода содержат два неспаренных электрона, что делает триплетный кислород необычным примером стабильного и часто встречающегося дирадикала : [2] он более стабилен в виде триплета , чем синглета . Согласно теории молекулярных орбиталей , электронная конфигурация триплетного кислорода имеет два электрона, занимающих две π- молекулярные орбитали (МО) одинаковой энергии (то есть вырожденные МО ). В соответствии с правилами Хунда они остаются неспаренными и спин-параллельными, что и объясняет парамагнетизм молекулярного кислорода. Эти наполовину заполненные орбитали носят разрыхляющий характер, снижая общий порядок связей молекулы до 2 с максимального значения 3, которое могло бы возникнуть, когда эти разрыхляющие орбитали остаются полностью незанятыми, как в динитрогене . Символ молекулярного термина для триплетного кислорода - 3 Σ.−
г. [3]

Спины s = 1 ⁄ 2 двух электронов на вырожденных орбиталях дают в общей сложности 2 × 2 = 4 независимых спиновых состояния . Обменное взаимодействие разделяет их на синглетное состояние (суммарный спин S = 0) и набор из трех вырожденных триплетных состояний ( S = 1). В соответствии с правилами Хунда триплетные состояния энергетически более выгодны и соответствуют основному состоянию молекулы с общим электронным спином S = 1. Возбуждение до состояния S = 0 приводит к образованию гораздо более реакционноспособного, метастабильного синглетного кислорода . [4] [5]
Поскольку молекула в основном состоянии имеет ненулевой спиновый магнитный момент , кислород является парамагнитным ; т. е. его можно притянуть к полюсам магнита . Таким образом, структура Льюиса O=O со всеми электронами в парах неточно отражает природу связи в молекулярном кислороде. Однако альтернативная структура •O–O• также неадекватна, поскольку предполагает характер одинарной связи, а экспериментально определенная длина связи 121 пм [6] значительно короче, чем одинарная связь в перекиси водорода (HO–OH), которая имеет длина 147,5 вечера. [7] Это указывает на то, что триплетный кислород имеет более высокий порядок связи. Теория молекулярных орбиталей должна использоваться для правильного объяснения наблюдаемого парамагнетизма и короткой длины связи одновременно. В рамках теории молекулярных орбиталей связь кислород-кислород в триплете дикислорода лучше описать как одну полную σ-связь плюс две π-полусвязи, каждая полусвязь приходится на двухцентровую трехэлектронную (2c-3e) связь . чтобы дать чистый порядок облигаций, равный двум (1+2× 1/2 ), а также учитывает спиновое состояние ( S = 1). В случае триплетного дикислорода каждая связь 2c-3e состоит из двух электронов на связывающей орбитали π u и одного электрона на разрыхляющей орбитали π g , что дает чистый вклад в порядок связи 1/2 .
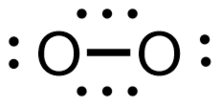
Обычные правила построения структур Льюиса должны быть изменены, чтобы учесть такие молекулы, как триплет дикислорода или оксид азота , которые содержат связи 2c-3e. В этом отношении нет единого мнения; Полинг предложил использовать три близко расположенные коллинеарные точки для обозначения трехэлектронной связи (см. иллюстрацию). [8]
Обычный экспериментальный способ наблюдать парамагнетизм дикислорода — охладить его до жидкой фазы. Если залить жидкий кислород между полюсами сильных магнитов, расположенных близко друг к другу, он может оказаться во взвешенном состоянии. Или магнит может притягивать струю жидкого кислорода по мере его наливания. Чистый магнитный момент полного спина электрона дает объяснение этим наблюдениям.
Необычная электронная конфигурация не позволяет молекулярному кислороду напрямую реагировать со многими другими молекулами, которые часто находятся в синглетном состоянии . Однако триплетный кислород легко вступает в реакцию с молекулами в дублетном состоянии с образованием нового радикала.
Сохранение спинового квантового числа потребовало бы триплетного переходного состояния в реакции триплетного кислорода с замкнутой оболочкой (молекула в синглетном состоянии). Требуемой дополнительной энергии достаточно, чтобы предотвратить прямую реакцию при температуре окружающей среды со всеми субстратами, кроме наиболее реакционноспособных, например, с белым фосфором . При более высоких температурах или в присутствии подходящих катализаторов реакция протекает легче. Например, для большинства легковоспламеняющихся веществ характерна температура самовоспламенения , при которой они горят на воздухе без внешнего пламени или искры.