

Элементарный фосфор может существовать в нескольких аллотропах , наиболее распространенными из которых являются белые и красные твердые вещества. Известны также сплошные фиолетовые и черные аллотропы. Газообразный фосфор существует в виде дифосфора и атомарного фосфора.
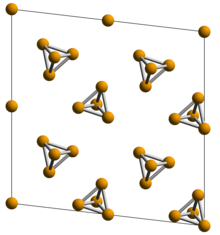
Белый фосфор , желтый фосфор или просто тетрафосфор ( P 4 ) существует в виде молекул фосфора, состоящих из четырех атомов в тетраэдрической структуре. Тетраэдрическое расположение приводит к деформации кольца и нестабильности . Молекула описывается как состоящая из шести одинарных связей фосфор-фосфор (связи P-P). Известны две кристаллические формы. Форма α определяется как стандартное состояние элемента, но на самом деле она метастабильна при стандартных условиях. [1] Он имеет объемно-центрированную кубическую кристаллическую структуру и обратимо превращается в β-форму при 195,2 К. Считается, что β-форма имеет гексагональную кристаллическую структуру. [2]
Белый фосфор представляет собой полупрозрачное воскообразное твердое вещество, которое под воздействием света быстро желтеет. По этой причине его еще называют желтым фосфором. Он светится зеленоватым светом в темноте (при воздействии кислорода), легко воспламеняется и пирофорен (самовоспламеняется) при контакте с воздухом. Он токсичен , вызывая серьезные повреждения печени при проглатывании и окаменевшую челюсть при хроническом проглатывании или вдыхании. Запах горения этой формы имеет характерный чесночный запах, а образцы обычно покрыты белой « пентаоксидом дифосфора », состоящим из тетраэдров P 4 O 10 с кислородом, внедренным между атомами фосфора и в их вершинах. Белый фосфор мало растворим в воде и может храниться под водой. Действительно, белый фосфор безопасен от самовоспламенения только при погружении в воду ; из-за этого непрореагировавший белый фосфор может оказаться опасным для любителей пляжного отдыха , которые могут собирать вымытые образцы, не подозревая об их истинной природе. [3] [4] P 4 растворим в бензоле , маслах , сероуглероде и дихлориде серы .
Белый аллотроп можно получить несколькими методами. В промышленном процессе фосфоритную руду нагревают в электрической или топливной печи в присутствии углерода и кремнезема . [5] Элементарный фосфор затем высвобождается в виде пара и может быть собран под действием фосфорной кислоты . Идеализированное уравнение этой карботермической реакции показано для фосфата кальция (хотя фосфоритная руда содержит значительные количества фторапатита ):
Белый фосфор имеет значительное давление паров при обычных температурах. Плотность пара указывает на то, что пар состоит из молекул P 4 при температуре примерно до 800 °C. Выше этой температуры происходит диссоциация на молекулы P 2 .
Он самопроизвольно воспламеняется на воздухе при температуре около 50 ° C (122 ° F) и при гораздо более низких температурах, если он мелкодисперсный (из-за снижения температуры плавления ). Фосфор реагирует с кислородом, образуя обычно два оксида в зависимости от количества доступного кислорода: P 4 O 6 ( триоксид фосфора ) при реакции с ограниченным запасом кислорода и P 4 O 10 при реакции с избытком кислорода. В редких случаях также образуются P 4 O 7 , P 4 O 8 и P 4 O 9 , но в небольших количествах. В результате сгорания образуется оксид фосфора (V):
Благодаря этому свойству белый фосфор используется в качестве оружия .
Хотя белый фосфор переходит в термодинамически более стабильный красный аллотроп, образования кубической молекулы Р 8 в конденсированной фазе не наблюдается. Аналоги этой гипотетической молекулы были получены из фосфаалкинов . [6] Белый фосфор в газообразном состоянии и в виде воскообразного твердого вещества состоит из реакционноспособных молекул P 4 .


Красный фосфор может образоваться при нагревании белого фосфора до 300 °C (572 °F) в отсутствие воздуха или при воздействии на белый фосфор солнечного света . Красный фосфор существует в виде аморфной сетки. При дальнейшем нагревании аморфный красный фосфор кристаллизуется. Объемный красный фосфор не воспламеняется на воздухе при температуре ниже 240 °C (464 °F), тогда как кусочки белого фосфора воспламеняются при температуре около 30 °C (86 °F).
В стандартных условиях он более стабилен, чем белый фосфор, но менее стабилен, чем термодинамически стабильный черный фосфор. Стандартная энтальпия образования красного фосфора составляет -17,6 кДж/моль. [1] Красный фосфор кинетически наиболее стабилен.
Впервые оно было представлено Антоном фон Шрёттером перед Венской академией наук 9 декабря 1847 года, хотя другие, несомненно, имели это вещество в своих руках раньше, например Берцелиус. [7]
Красный фосфор можно использовать в качестве очень эффективного антипирена , особенно в термопластах (например, полиамиде ) и термореактивных материалах (например, эпоксидных смолах или полиуретанах ). Огнезащитный эффект основан на образовании полифосфорной кислоты . Вместе с органическим полимерным материалом эти кислоты образуют обугливание, препятствующее распространению пламени. Риски безопасности, связанные с образованием фосфина и чувствительностью красного фосфора к трению , можно эффективно минимизировать за счет стабилизации и микрокапсулирования . Для облегчения обращения красный фосфор часто используется в виде дисперсий или маточных смесей в различных системах-носителях. Однако в электронных/электрических системах огнезащитный состав на основе красного фосфора фактически запрещен крупными OEM-производителями из-за его склонности вызывать преждевременные выходы из строя. [8] Одна из постоянных проблем заключается в том, что красный фосфор в эпоксидных формовочных компаундах вызывает повышенный ток утечки в полупроводниковых устройствах. [9] Другой проблемой было ускорение реакций гидролиза в изоляционном материале ПБТ . [10]
Красный фосфор также может использоваться при незаконном производстве метамфетамина и крокодила .
Красный фосфор можно использовать в качестве элементарного фотокатализатора образования водорода из воды. [11] Они демонстрируют устойчивую скорость выделения водорода 633 мкмоль / (ч⋅г) за счет образования мелкоразмерного волокнистого фосфора. [12]

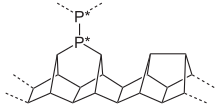
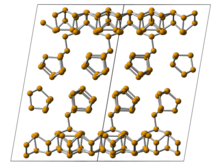
Моноклинный фосфор , или фиолетовый фосфор , также известен как металлический фосфор Хитторфа . [13] [14] В 1865 году Иоганн Вильгельм Хитторф нагрел красный фосфор в запечатанной трубке при температуре 530 °C. Верхняя часть трубки поддерживалась при температуре 444°С. В результате сублимировались блестящие непрозрачные моноклинные или ромбоэдрические кристаллы. Фиолетовый фосфор также можно получить растворением белого фосфора в расплавленном свинце в запечатанной трубке при температуре 500 ° C в течение 18 часов. При медленном охлаждении аллотроп Хитторфа кристаллизуется . Кристаллы можно обнаружить, растворив свинец в разбавленной азотной кислоте с последующим кипячением в концентрированной соляной кислоте . [15] Кроме того, существует волокнистая форма с аналогичными фосфорными клетками. Решетчатая структура фиолетового фосфора была представлена Турном и Кребсом в 1969 году. [16] Мнимые частоты, указывающие на иррациональность или нестабильность структуры, были получены для описанной фиолетовой структуры в 1969 году. [17] Монокристалл фиолетового фосфора был также производится. Методом монокристаллической рентгеновской дифракции установлено, что структура решетки фиолетового фосфора является моноклинной с пространственной группой P 2/ n (13) ( a = 9,210, b = 9,128, c = 21,893 Å, β = 97,776°, CSD-1935087). Оптическая запрещенная зона фиолетового фосфора, измеренная с помощью спектроскопии диффузного отражения, составила около 1,7 эВ. Температура термического разложения была на 52 °C выше, чем у его аналога из черного фосфора. Фиолетовый фосфорен легко получить как механическим, так и растворным эксфолиированием.
Фиолетовый фосфор не воспламеняется на воздухе до нагревания до 300 °С и нерастворим во всех растворителях. Он не подвергается воздействию щелочей и лишь медленно реагирует с галогенами . Его можно окислить азотной кислотой до фосфорной кислоты .
Если его нагреть в атмосфере инертного газа, например азота или углекислого газа , он сублимируется , а пары конденсируются в виде белого фосфора. Если его нагреть в вакууме и быстро конденсировать пары, получится фиолетовый фосфор. По-видимому, фиолетовый фосфор представляет собой полимер с высокой относительной молекулярной массой, который при нагревании распадается на молекулы Р 2 . При охлаждении они обычно димеризуются с образованием молекул P 4 (т.е. белого фосфора), но в вакууме они снова соединяются, образуя полимерный фиолетовый аллотроп.


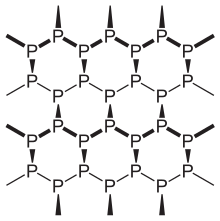
Черный фосфор представляет собой термодинамически стабильную форму фосфора при комнатной температуре и давлении с теплотой образования -39,3 кДж/моль (по отношению к белому фосфору, который определяется как стандартное состояние). [1] Впервые он был синтезирован путем нагрева белого фосфора под высоким давлением (12 000 атмосфер) в 1914 году. Как двумерный материал, по внешнему виду, свойствам и структуре черный фосфор очень похож на графит : он одновременно черный и чешуйчатый, является проводником. электричества и сморщенных слоев связанных атомов. [18]
Черный фосфор имеет орторомбическую складчатую сотовую структуру и является наименее реакционноспособным аллотропом из-за его решетки из взаимосвязанных шестичленных колец, где каждый атом связан с тремя другими атомами. [19] [20] В этой структуре каждый атом фосфора имеет пять электронов на внешней оболочке. [21] Черный и красный фосфор также могут иметь кубическую кристаллическую решетку. [22] Первый синтез кристаллов черного фосфора под высоким давлением был осуществлен лауреатом Нобелевской премии Перси Уильямсом Бриджменом в 1914 году . [23] Соли металлов катализируют синтез черного фосфора. [24]
Датчики на основе черного фосфора обладают рядом превосходящих качеств по сравнению с традиционными материалами, используемыми в пьезоэлектрических или резистивных датчиках. Черный фосфор, характеризующийся своей уникальной сотовой решетчатой структурой, обеспечивает исключительную подвижность носителей. Это свойство обеспечивает его высокую чувствительность и механическую устойчивость, что делает его интересным кандидатом на роль сенсорной технологии . [25] [26]
Сходство с графитом также включает возможность расслаивания (расслоения) скотча, в результате чего получается фосфорен , графеноподобный 2D-материал с превосходными свойствами переноса заряда, свойствами теплопереноса и оптическими свойствами. Отличительные особенности, представляющие научный интерес, включают зависимость ширины запрещенной зоны, которой нет в графене. [27] Это, в сочетании с высоким коэффициентом включения/выключения ~10 5 , делает фосфорен многообещающим кандидатом для полевых транзисторов (FET). [28] Перестраиваемая запрещенная зона также предполагает перспективное применение в фотодетекторах среднего инфракрасного диапазона и светодиодах. [29] [30] Расслоенный черный фосфор сублимируется при 400 °C в вакууме. [31] Он постепенно окисляется под воздействием воды в присутствии кислорода, что вызывает беспокойство при рассмотрении его, например, в качестве материала для изготовления транзисторов. [32] [33] Расслаивающийся черный фосфор является новым анодным материалом в аккумуляторных батареях, демонстрирующим высокую стабильность и способность хранить литий . [34]
Кольцевой фосфор был теоретически предсказан в 2007 году. [35] Кольцевой фосфор был самоорганизован внутри вакуумированных многостенных углеродных нанотрубок с внутренним диаметром 5–8 нм с использованием метода паровой инкапсуляции. Внутри многостенной углеродной нанотрубки с внутренним диаметром 5,90 нм в атомном масштабе наблюдалось кольцо диаметром 5,30 нм, состоящее из 23 звеньев P 8 и 23 P 2 с общим количеством атомов P 230. Расстояние между соседними кольцами составляет 6,4 Å. [36]
Молекула P 6 в форме кольца не стабильна изолированно.
Однослойный синий фосфор впервые был получен в 2016 году методом молекулярно-лучевой эпитаксии из черного фосфора в качестве прекурсора. [37]


Аллотроп дифосфора ( Р 2 ) обычно можно получить только в экстремальных условиях (например, из Р 4 при 1100 К). В 2006 году двухатомная молекула была получена в гомогенном растворе при нормальных условиях с использованием комплексов переходных металлов (например, вольфрама и ниобия ). [38]
Дифосфор — это газообразная форма фосфора , термодинамически стабильная форма при температуре от 1200 до 2000 °C. Диссоциация тетрафосфора ( P 4 ) начинается при более низкой температуре: процентное содержание P 2 при 800 °C составляет ≈ 1%. При температуре выше примерно 2000°С молекула дифосфора начинает диссоциировать на атомарный фосфор.
Полимеры наностержней P 12 были выделены из комплексов CuI-P с помощью низкотемпературной обработки. [39]
Было показано, что красный/коричневый фосфор стабилен на воздухе в течение нескольких недель и имеет свойства, отличные от свойств красного фосфора. Электронная микроскопия показала, что красный/коричневый фосфор образует длинные параллельные наностержни диаметром от 3,4 до 4,7 Å. [39]
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка )