
Фаза S ( фаза синтеза ) — это фаза клеточного цикла , в которой реплицируется ДНК , происходящая между фазой G1 и фазой G2 . [1] Поскольку точное дублирование генома имеет решающее значение для успешного деления клеток, процессы, происходящие во время S-фазы, жестко регулируются и широко консервативны.
Вход в S-фазу контролируется точкой ограничения G1 (R), которая передает клеткам оставшуюся часть клеточного цикла, если имеется достаточное количество питательных веществ и сигналов роста. [2] Этот переход по существу необратим; после прохождения точки ограничения клетка перейдет через S-фазу, даже если условия окружающей среды станут неблагоприятными. [2]
Соответственно, вход в S-фазу контролируется молекулярными путями, которые способствуют быстрому однонаправленному сдвигу состояния клетки. Например, у дрожжей рост клеток индуцирует накопление циклина Cln3 , который образует комплекс с циклин-зависимой киназой CDK2. [3] Комплекс Cln3-CDK2 способствует транскрипции генов S-фазы путем инактивации репрессора транскрипции Whi5 . [3] Поскольку активация генов S-фазы приводит к дальнейшему подавлению Whi5 , этот путь создает петлю положительной обратной связи, которая полностью заставляет клетки экспрессировать гены S-фазы. [3]
Удивительно похожая схема регуляции существует в клетках млекопитающих. [3] Митогенные сигналы, полученные на протяжении фазы G1, вызывают постепенное накопление циклина D, который образует комплекс с CDK4/6. [3] Активный комплекс циклин D-CDK4/6 индуцирует высвобождение транскрипционного фактора E2F , который, в свою очередь, инициирует экспрессию генов S-фазы. [3] Несколько генов-мишеней E2F способствуют дальнейшему высвобождению E2F, создавая петлю положительной обратной связи, аналогичную той, которая обнаружена у дрожжей. [3]
На протяжении фазы M и фазы G1 клетки собирают неактивные пререпликационные комплексы (пре-RC) в точках начала репликации, распределенных по всему геному. [4] Во время S-фазы клетка преобразует пре-РК в активные вилки репликации, чтобы инициировать репликацию ДНК. [4] Этот процесс зависит от киназной активности Cdc7 и различных CDK S-фазы, оба из которых активируются при входе в S-фазу. [4]
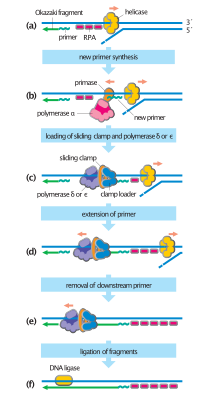
Активация pre-RC — тщательно регулируемый и очень последовательный процесс. После того, как Cdc7 и CDK S-фазы фосфорилируют свои соответствующие субстраты, второй набор репликативных факторов связывается с пре-RC. [4] Стабильная ассоциация побуждает хеликазу MCM раскручивать небольшой участок родительской ДНК на две нити оцДНК, что, в свою очередь, рекрутирует белок репликации А ( RPA ), белок, связывающий оцДНК. [4] Рекрутирование RPA запускает репликационную вилку для загрузки репликативных ДНК- полимераз и скользящих зажимов PCNA . [4] Загрузка этих факторов завершает активную репликационную вилку и инициирует синтез новой ДНК.
Полная сборка и активация вилки репликации происходит только на небольшом подмножестве источников репликации. Все эукариоты обладают гораздо большим количеством точек начала репликации, чем это необходимо для одного цикла репликации ДНК. [5] Избыточные источники могут повысить гибкость репликации ДНК, позволяя клеткам контролировать скорость синтеза ДНК и реагировать на репликационный стресс. [5]
Поскольку для правильного функционирования новая ДНК должна быть упакована в нуклеосомы , параллельно с репликацией ДНК происходит синтез канонических (нонвариантных) белков -гистонов . Во время ранней S-фазы комплекс циклин E-Cdk2 фосфорилирует NPAT , ядерный коактиватор транскрипции гистонов. [6] NPAT активируется путем фосфорилирования и привлекает комплекс ремоделирования хроматина Tip60 к промоторам гистоновых генов. [6] Активность Tip60 удаляет ингибирующие структуры хроматина и приводит к увеличению скорости транскрипции в три-десять раз. [1] [6]
Помимо увеличения транскрипции гистоновых генов, вход в S-фазу также регулирует выработку гистонов на уровне РНК. Вместо полиаденилированных хвостов канонические транскрипты гистонов обладают консервативным мотивом 3'- стебельной петли , который избирательно связывается с белком, связывающим стебельчатую петлю ( SLBP ). [7] Связывание SLBP необходимо для эффективной обработки, экспорта и трансляции мРНК гистонов, что позволяет ему функционировать как высокочувствительный биохимический «переключатель». [7] Во время S-фазы накопление SLBP действует вместе с NPAT, резко повышая эффективность производства гистонов. [7] Однако, как только S-фаза заканчивается, как SLBP, так и связанная РНК быстро разрушаются. [8] Это немедленно останавливает выработку гистонов и предотвращает токсичное накопление свободных гистонов. [9]

Свободные гистоны, вырабатываемые клеткой во время S-фазы, быстро включаются в новые нуклеосомы. Этот процесс тесно связан с репликационной вилкой, происходящей непосредственно «спереди» и «позади» репликационного комплекса. Транслокация хеликазы MCM вдоль ведущей цепи разрушает родительские октамеры нуклеосомы, что приводит к высвобождению субъединиц H3-H4 и H2A-H2B. [10] Повторная сборка нуклеосом за репликационной вилкой опосредуется факторами сборки хроматина (CAF), которые слабо связаны с белками репликации. [4] [11] Хотя это и не до конца понятно, повторная сборка, похоже, не использует полуконсервативную схему, наблюдаемую при репликации ДНК. [11] Эксперименты по маркировке показывают, что дупликация нуклеосом преимущественно консервативна. [11] [10] Отцовская коровая нуклеосома H3-H4 остается полностью отделенной от вновь синтезированного H3-H4, что приводит к образованию нуклеосом, которые содержат либо исключительно старые H3-H4, либо исключительно новые H3-H4. [10] [11] «Старые» и «новые» гистоны назначаются каждой дочерней цепи полуслучайно, что приводит к равному разделению регуляторных модификаций. [10]
Сразу после деления каждая дочерняя хроматида обладает только половиной эпигенетических модификаций, присутствующих в отцовской хроматиде. [10] Клетка должна использовать этот частичный набор инструкций для восстановления функциональных доменов хроматина перед вступлением в митоз.
Для больших геномных регионов наследование старых нуклеосом H3-H4 достаточно для точного восстановления доменов хроматина. [10] Репрессивный комплекс Polycomb 2 ( PRC2 ) и несколько других комплексов, модифицирующих гистоны, могут «копировать» модификации, присутствующие в старых гистонах, на новые. [10] Этот процесс усиливает эпигенетические метки и противодействует разбавляющему эффекту дупликации нуклеосом. [10]
Однако для небольших доменов, приближающихся к размеру отдельных генов, старые нуклеосомы распределены слишком тонко для точного распространения модификаций гистонов. [10] В этих регионах структура хроматина, вероятно, контролируется включением вариантов гистонов во время повторной сборки нуклеосом. [10] Тесная корреляция, наблюдаемая между H3.3/H2A.Z и транскрипционно активными областями, подтверждает этот предложенный механизм. [10] К сожалению, причинно-следственная связь еще не доказана. [10]
Во время S-фазы клетка постоянно проверяет свой геном на наличие аномалий. Обнаружение повреждения ДНК вызывает активацию трех канонических «путей контрольных точек» S-фазы, которые задерживают или останавливают дальнейшее развитие клеточного цикла: [12]
В дополнение к этим каноническим контрольным точкам, недавние данные свидетельствуют о том, что нарушения в поставках гистонов и сборке нуклеосом также могут изменять прогрессию S-фазы. [14] Истощение свободных гистонов в клетках дрозофилы резко продлевает S-фазу и вызывает необратимую остановку G2-фазы. [14] Этот уникальный фенотип ареста не связан с активацией канонических путей повреждения ДНК, что указывает на то, что сборка нуклеосом и поставка гистонов могут быть тщательно изучены с помощью новой контрольной точки S-фазы. [14]