Неомицин — аминогликозидный антибиотик , проявляющий бактерицидную активность против грамотрицательных аэробных палочек и некоторых анаэробных палочек, у которых резистентность еще не возникла. Обычно он не эффективен против грамположительных палочек и анаэробных грамотрицательных палочек. Неомицин выпускается в пероральных и местных формах, включая кремы, мази и глазные капли. Неомицин относится к классу аминогликозидов антибиотиков, которые содержат два или более аминосахара , соединенных гликозидными связями .
Неомицин был открыт в 1949 году микробиологом Селманом Ваксманом и его студентом Хьюбертом Лешевалье в Ратгерском университете . Неомицин получил одобрение для медицинского применения в 1952 году. [1] Ратгерский университет получил патент на неомицин в 1957 году. [2]
Неомицин был открыт в 1949 году микробиологом Селманом Ваксманом и его студентом Хьюбертом Лешевалье в Ратгерском университете . Он вырабатывается естественным образом бактерией Streptomyces fradiae . [3] Синтез требует определенных питательных условий в стационарных или погруженных аэробных условиях. Затем соединение выделяют и очищают от бактерии. [4]
Неомицин обычно применяется в качестве местного препарата, такого как Неоспорин ( неомицин/полимиксин В/бацитрацин ). Антибиотик также можно вводить перорально, в этом случае его обычно комбинируют с другими антибиотиками. Неомицин не всасывается из желудочно-кишечного тракта и использовался в качестве профилактической меры при печеночной энцефалопатии и гиперхолестеринемии . Убивая бактерии в желудочно-кишечном тракте, Неомицин поддерживает низкий уровень аммиака и предотвращает печеночную энцефалопатию, особенно перед желудочно-кишечной хирургией . [ необходима цитата ]
Ваксман и Лешевалье изначально отметили, что неомицин был активен против бактерий, устойчивых к стрептомицину, а также против Mycobacterium tuberculosis , возбудителя туберкулеза . [5] Неомицин также использовался для лечения избыточного бактериального роста в тонком кишечнике . Неомицин не вводят инъекционно, так как он чрезвычайно нефротоксичен (повреждает функцию почек) даже по сравнению с другими аминогликозидами . Исключением является случай, когда неомицин в небольших количествах включен в качестве консерванта в некоторые вакцины — обычно 25 мкг на дозу. [6]
Подобно другим аминогликозидам, неомицин обладает превосходной активностью против грамотрицательных бактерий и частично эффективен против грамположительных бактерий . Он относительно токсичен для людей, а аллергические реакции отмечаются как распространенная нежелательная реакция (см.: гиперчувствительность ). [7] Врачи иногда рекомендуют использовать мази с антибиотиками без неомицина, такие как Полиспорин . [8] Ниже представлены данные о чувствительности к минимальной ингибирующей концентрации (МИК) для нескольких грамотрицательных бактерий, имеющих медицинское значение. [9]
В 2005–2006 годах неомицин был пятым по распространенности аллергеном в результатах патч-теста (10,0%). [10] В 2010 году он был назван аллергеном года. [11] Неомицин также является известным антагонистом ГАМК- гамма -аминомасляной кислоты и может вызывать судороги и психозы. [12] Как и другие аминогликозиды, неомицин, как было показано, является ототоксичным , вызывая шум в ушах , потерю слуха и вестибулярные проблемы у небольшого числа пациентов. Неомицин влияет на улитку, которая находится во внутреннем ухе. [13] Потеря слуха вызвана гибелью волосковых клеток уха, которая происходит в ответ на лечение неомицином. [13] Пациентам с существующим шумом в ушах или сенсоневральной потерей слуха рекомендуется поговорить с врачом о рисках и побочных эффектах перед приемом этого лекарства. [ необходима ссылка ]
Антибактериальная активность неомицина обусловлена его связыванием с 30S субъединицей прокариотической рибосомы , где он ингибирует прокариотическую трансляцию мРНК. [14]
Неомицин также проявляет высокую связывающую способность с фосфатидилинозитол-4,5-бисфосфатом (PIP2), фосфолипидным компонентом клеточных мембран. [15]
Устойчивость к неомицину обеспечивается одним из двух генов канамицинкиназы . [16] Гены, обеспечивающие устойчивость к неомицину, обычно включаются в ДНК- плазмиды, используемые для создания стабильных линий клеток млекопитающих, экспрессирующих клонированные белки в культуре. Многие коммерчески доступные плазмиды экспрессии белка содержат ген неорезистентности в качестве селективного маркера . В настоящее время проводятся исследования, чтобы понять, обладают ли производные неомицина тем же антибиотическим действием, оставаясь при этом эффективными против бактерий, устойчивых к неомицину. [17]
Неомицин был впервые выделен из Streptomyces fradiae и Streptomyces albogriseus в 1949 году (NBRC 12773). [18] Неомицин представляет собой смесь неомицина B (фрамицетина) и его эпимера неомицина C, причем последний компонент составляет около 5–15% смеси. Это основное соединение, которое наиболее активно при щелочной реакции. [5] Он также термостабилен и растворим в воде (хотя нерастворим в органических растворителях). [5] Неомицин обладает хорошей активностью против грамположительных и грамотрицательных бактерий , но является ототоксикантом . Таким образом, его использование ограничивается пероральным лечением кишечных инфекций. [19]
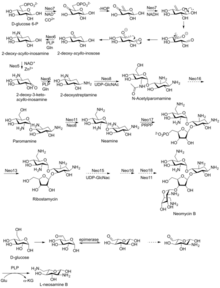
Неомицин B состоит из четырех связанных фрагментов: D -неозамина, 2-дезоксистрептамина (2-DOS), D -рибозы и L -неозамина. [ необходима цитата ]
Неомицин А, также называемый неамином, содержит D -неозамин и 2-дезоксистрептамин. Шесть генов отвечают за биосинтез неамина: ген DOIS (btrC, neo7); ген аминотрансферазы L-глутамин:DOI (btrS, neo6); предполагаемый ген гликозилтрансферазы (btrM, neo8); предполагаемый ген аминотрансферазы (похожий на глутамат-1-полуальдегид 2,1-аминомутазу) (btrB, neo18); предполагаемый ген алкогольдегидрогеназы (btrE, neo5); и еще один предполагаемый ген дегидрогеназы (похожий на хлориндегидрогеназу и родственные флавопротеины) (btrQ, neo11). [20] Деацетилаза, действующая для удаления ацетильной группы на N-ацетилглюкозаминовых фрагментах аминогликозидных промежуточных продуктов (Neo16), еще предстоит выяснить (последовательность, похожая на BtrD). [21]
Далее следует присоединение D -рибозы посредством рибозилирования неамина с использованием 5-фосфорибозил-1-дифосфата (PRPP) в качестве донора рибозила (BtrL, BtrP); [22] ген гликозилтрансферазы (потенциальные гомологи RibF, LivF, Parf) (Neo15). [23]
Неозамин B ( L -неозамин B), скорее всего, биосинтезируется таким же образом, как и неозамин C ( D -ниозамин) в биосинтезе неамина, но с дополнительным этапом эпимеризации , необходимым для учета присутствия эпимерного неозамина B в неомицине B. [24]
Неомицин B и C — это молекулы из 23 атомов углерода с четырехкольцевой структурой. Три из колец шестичленные, а одно — пятичленное. [25] Неомицин B и Неомицин C являются стереоизомерами друг друга и отличаются только одним стереоцентром, один из которых дает R-конформацию, а другой — S-конформацию. [25] Неомицин C может подвергаться ферментативному синтезу из рибостамицина. [26]
Неомицин стандартного качества состоит из нескольких родственных соединений, включая неомицин A (неамин), неомицин B (фрамицетин), неомицин C и несколько второстепенных соединений, содержащихся в гораздо меньших количествах. Неомицин B является наиболее активным компонентом неомицина, за которым следуют неомицин C и неомицин A. Неомицин A является неактивным продуктом распада изомеров C и B. [27] Количества этих компонентов в неомицине варьируются от партии к партии в зависимости от производителя и производственного процесса. [28]
Аминогликозиды, такие как неомицин, известны своей способностью связываться с дуплексной РНК с высокой аффинностью. [29] Константа ассоциации неомицина с РНК A-сайта находится в диапазоне 10 9 M −1 . [30] Однако, спустя более 50 лет после его открытия, его ДНК-связывающие свойства все еще были неизвестны. Было показано, что неомицин вызывает термическую стабилизацию триплексной ДНК, при этом оказывая незначительное или почти не оказывая влияния на стабилизацию дуплекса B-ДНК. [31] Было также показано, что неомицин связывается со структурами, которые принимают структуру A-формы, триплексная ДНК является одной из них. Неомицин также включает образование гибридного триплекса ДНК:РНК. [32]