Фторборная кислота или тетрафторборная кислота (архаично, фторборная кислота ) — неорганическое соединение с упрощенной химической формулой H + [ B F 4 ] − . В отличие от других сильных кислот, таких как H 2 SO 4 или HClO 4 , чистой (не содержащей растворителя) тетрафторборной кислоты (точнее, чистого тетрафторбората водорода H[BF 4 ] ) не существует. Термин «фторборная кислота» относится к ряду химических соединений, в зависимости от растворителя. Н + в упрощенной формуле фторборной кислоты представляет собой сольватированный протон . Растворителем может быть любое подходящее основание Льюиса . Например, если растворителем является вода, фторборную кислоту можно представить формулой [H 3 O] + [BF 4 ] - (тетрафторборат оксония), хотя более реалистично, что несколько молекул воды сольватируют протон: [H(H 2 O ) п ] + [BF 4 ] - . Сольват этилового эфира также имеется в продаже, где фторборная кислота может быть представлена формулой [H((CH 3 CH 2 ) 2 O) n ] + [BF 4 ] - , где n, скорее всего, равно 2.
В основном его производят как предшественник других фторборатных солей. [3] Это сильная кислота . Фторборная кислота вызывает коррозию и повреждает кожу. Он доступен коммерчески в виде раствора в воде и других растворителях , таких как диэтиловый эфир . Это сильная кислота со слабокоординирующим неокисляющим сопряженным основанием. [2] Структурно она похожа на хлорную кислоту , но не имеет опасностей, связанных с окислителями .
Чистый H[BF 4 ] был описан как «несуществующее соединение», поскольку ожидается, что достаточно «голый» протон будет отрывать фторид от иона тетрафторбората с образованием фторида водорода и трифторида бора :
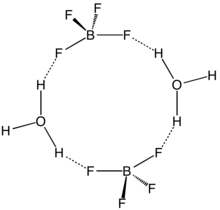
То же самое справедливо и для суперкислот, известных по упрощенным формулам H[PF 6 ] и H[SbF 6 ] . [4] [5] Однако раствор BF 3 в HF является очень кислым, имеет приблизительный вид [H 2 F] + [BF 4 ] - (тетрафторборат фторония) и функцию кислотности Гаммета -16,6 при 7 моль. % BF 3 , легко квалифицируемый как суперкислота. [6] Хотя не содержащий растворителя H[BF 4 ] не был выделен, его сольваты хорошо охарактеризованы. Эти соли состоят из протонированного растворителя в качестве катиона, например, H 3 O + и H 5 O.+2, а тетраэдрический BF−4анион. Анион и катионы имеют прочные водородные связи. [7]
Водные растворы H[BF 4 ] получают растворением борной кислоты в водной плавиковой кислоте . [8] [9] Три эквивалента HF реагируют с образованием промежуточного трифторида бора, а четвертый дает фторборную кислоту:
Безводные растворы можно приготовить обработкой водного раствора фторборной кислоты уксусным ангидридом . [10]
Кислотность фторборной кислоты осложняется тем, что ее название относится к ряду различных соединений, например, [H(CH 3 CH 2 ) 2 O] + [BF 4 ] − (тетрафторборат диметилоксония), [H 3 O] + [BF 4 ] − (тетрафторборат оксония) и HF·BF 3 ( аддукт фтороводород - трифторид бора 1:1) – каждый с разной кислотностью. Водное значение p K a указано как -0,44. [3] Титрование [ N((CH 2 ) 3 CH 3 ) 4 ] + [BF 4 ] - (тетрафторборат тетрабутиламмония) в растворе ацетонитрила показывает, что H[BF 4 ] , т.е. HF·BF 3 , имеет ap K a 1,6 в этом растворителе. Таким образом, его кислотность сравнима с кислотностью фторсульфоновой кислоты . [2]
Фторборная кислота является основным предшественником фторборатных солей, которые обычно получают путем обработки оксидов металлов фторборной кислотой. Неорганические соли являются промежуточными продуктами при производстве огнезащитных материалов и глазурных фритт , а также при электролитическом получении бора . H[BF 4 ] также используется при травлении алюминия и кислотном травлении.
H[BF 4 ] используется в качестве катализатора алкилирования и полимеризации . В реакциях защиты углеводов эфирная фторборная кислота является эффективным и экономичным катализатором реакций трансацетилирования и изопропилидирования. Растворы ацетонитрила расщепляют ацетали и некоторые простые эфиры . Многие реакционноспособные катионы были получены с использованием фторборной кислоты, например тетрафторборат тропилия ( C 7 H 7 + [BF 4 ] - ), тетрафторборат трифенилкарбения ( Ph 3 C] + [BF 4 ] - ), тетрафторборат триэтилоксония ( Et 3 O] + [ BF 4 ] - ) и тетрафторборат бензолдиазония ( [PhN 2 ] + [BF 4 ] - ).
Растворы H[BF 4 ] используются при гальванопокрытии олова и оловянных сплавов. В этом применении метансульфоновая кислота заменяет использование H[BF 4 ] . [11] Фторборная кислота также используется для высокоскоростной гальваники меди в фторборатных ваннах. [12]
H[BF 4 ] токсичен и поражает кожу и глаза. Он атакует стекло. [3] Он гидролизуется, выделяя едкий, летучий фторид водорода . [11]
Известен ряд фторборных кислот в водных растворах. Ряд можно представить следующим образом: [13]
{{cite book}}: CS1 maint: отсутствует местоположение издателя ( ссылка )