
В органической химии хелетропные реакции , также известные как хелотропные реакции , [2] представляют собой тип перициклической реакции ( химическая реакция , которая включает переходное состояние с циклическим массивом атомов и связанным с ним циклическим массивом взаимодействующих орбиталей ). [1] В частности, хелетропные реакции представляют собой подкласс циклоприсоединения . Ключевой отличительной особенностью хелетропных реакций является то, что в одном из реагентов обе новые связи образуются с одним и тем же атомом. [3]
В перициклическом переходном состоянии небольшая молекула отдает два электрона кольцу. Процесс реакции можно показать, используя две разные геометрии: малая молекула может приближаться линейным или нелинейным образом. В линейном подходе электроны на орбитали малой молекулы направлены прямо на π-систему. При нелинейном подходе орбита приближается под углом перекоса. Способность π-системы вращаться по мере приближения небольшой молекулы имеет решающее значение для образования новых связей. Направление вращения будет разным в зависимости от того, сколько π-электронов находится в системе. Ниже показана схема сближения двухэлектронного фрагмента с четырехэлектронной π-системой с использованием граничных молекулярных орбиталей. Вращение будет дисротационным, если маленькая молекула приближается линейно, и конротационным, если молекула приближается нелинейно. Диссротаторный и конротаторный — это сложные термины, обозначающие вращение связей в π-системе. Диссротаторный означает противоположные направления, а конротаторный означает одно и то же направление. Это также изображено на схеме ниже.
Используя правило Хюккеля, можно определить, является ли π-система ароматической или антиароматической. Если ароматические, линейные подходы используют вращательное движение, а нелинейные подходы используют вращательное движение. Противоположное дело обстоит с антиароматической системой. Линейные подходы будут иметь вращательное движение, а нелинейные подходы будут иметь вращательное движение. [1]
В 1995 году Суарес и Сордо показали, что диоксид серы при реакции с бутадиеном и изопреном дает два разных продукта в зависимости от механизма. Это было показано экспериментально и с помощью расчетов ab initio . Возможны как кинетический, так и термодинамический продукт, но термодинамический продукт более предпочтителен. Кинетический продукт возникает в результате реакции Дильса-Альдера , тогда как хелетропная реакция дает более термодинамически стабильный продукт. Хелетропный путь предпочтителен, поскольку он приводит к образованию более стабильного пятичленного кольцевого аддукта. На схеме ниже показана разница между двумя продуктами: путь справа показывает более стабильный термодинамический продукт, а путь слева показывает кинетический продукт. [4]
Хелетропные реакции 1,3-диенов с диоксидом серы широко исследованы с точки зрения кинетики (общие реакции см. выше).
При первом количественном измерении кинетических параметров этой реакции в исследовании 1976 года Айзекса и Лайлы была измерена скорость присоединения диоксида серы к производным бутадиена. Скорость добавления контролировали в бензоле при 30 °C с начальным двадцатикратным избытком диоксида серы, что позволяет получить приближение псевдопервого порядка. Исчезновение SO 2 отслеживали спектрофотометрически при 320 нм. Реакция имела кинетику псевдопервого порядка. Некоторые интересные результаты заключались в том, что электроноакцепторные группы диена снижали скорость реакции. Кроме того, на скорость реакции существенно влияли стерические эффекты 2-заместителей: более объемные группы увеличивали скорость реакции. Авторы объясняют это тенденцией объемных групп отдавать предпочтение цисоидной конформации диена, которая необходима для реакции (см. таблицу ниже). Кроме того, скорости при четырех температурах были измерены для семи диенов, что позволило рассчитать энтальпию активации (ΔH ‡ ) и энтропию активации (ΔS ‡ ) для этих реакций с помощью уравнения Аррениуса . [5]
Совсем недавно в исследовании 2002 года Монната, Фогеля и Сордо была измерена кинетика присоединения диоксида серы к 1,2-диметилиденциклоалканам. Интересный момент, представленный в этой статье, заключается в том, что реакция 1,2-диметилиденциклогексана с диоксидом серы может давать два разных продукта в зависимости от условий реакции. В результате реакции образуется соответствующий сульфин посредством гетеро-реакции Дильса-Альдера под кинетическим контролем (≤ -60 ° C), но под термодинамическим контролем (≥ -40 ° C) в результате реакции образуется соответствующий сульфолен посредством хелетропной реакции. Энтальпия активации гетеро-реакции Дильса–Альдера примерно на 8 кДж/моль меньше, чем соответствующей хелетропной реакции. Сульфолен примерно на 40 кДж/моль более стабилен, чем изометрический сульфин в растворе CH 2 Cl 2 /SO 2 . [6]
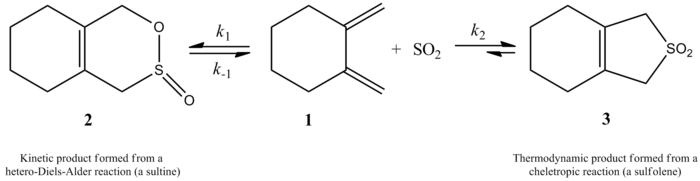
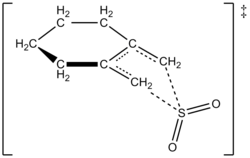
Авторам удалось экспериментально определить закон скорости реакции 1,2-диметилиденциклогексана с диоксидом серы при 261,2 К с образованием соответствующего сульфолена. Реакция имела первый порядок по 1,2-диметилиденциклогексану и второй порядок по диоксиду серы (см. ниже). Это подтвердило предсказание, основанное на квантовых расчетах ab initio высокого уровня . Используя вычислительные методы, авторы предложили переходную структуру хелетропной реакции 1,2-диметилиденциклогексана с диоксидом серы (см. рисунок справа). [6] Реакция второго порядка по диоксиду серы, поскольку другая молекула диоксида серы, вероятно, связывается с переходным состоянием, помогая его стабилизировать. [7] Аналогичные результаты были получены в исследовании 1995 года Суареса, Сордо и Сордо, в котором использовались расчеты ab initio для изучения кинетического и термодинамического контроля реакции диоксида серы с 1,3-диенами. [4]
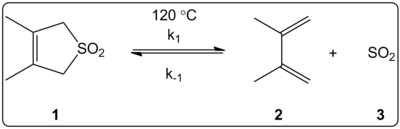
Влияние растворителя хелетропной реакции 3,4-диметил-2,5-дигидротиофен-1,1-диоксида (показано справа) кинетически исследовано в 14 растворителях. Установлено, что константы скорости прямой и обратной реакции, а также константы равновесия линейно коррелируют со шкалой полярности растворителя ET ( 30).
Реакции проводились при 120°C и изучались методом 1H-ЯМР-спектроскопии реакционной смеси. Было обнаружено , что прямая скорость k 1 уменьшается в 4,5 раза при переходе от циклогексана к метанолу . Установлено, что обратная скорость k -1 увеличивается в 53 раза при переходе от циклогексана к метанолу , а константа равновесия K eq уменьшается в 140 раз. Предполагается, что в процессе активации происходит смена полярности: Об этом свидетельствуют корреляции между равновесными и кинетическими данными. Авторы отмечают, что на реакцию, по-видимому, влияет полярность растворителя, что можно объяснить изменением дипольных моментов при переходе от реагента к переходному состоянию к продукту. Авторы также утверждают, что на хелетропную реакцию, по-видимому, не влияют ни кислотность, ни основность растворителя.
Результаты этого исследования позволяют авторам ожидать следующего поведения:
1. Изменение полярности растворителя будет влиять на скорость меньше, чем равновесное.
2. Константы скорости будут характеризоваться противоположным влиянием на полярность: k 1 будет несколько уменьшаться с увеличением E T (30), а k -1 будет увеличиваться в тех же условиях.
3. Влияние на k −1 будет больше, чем на k1 . [8]
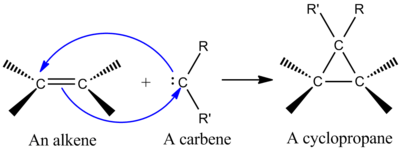
Одной из наиболее важных с синтетической точки зрения хелетропных реакций является присоединение синглетного карбена к алкену с образованием циклопропана (см. рисунок слева). [1] Карбен – это нейтральная молекула, содержащая двухвалентный углерод с шестью электронами в валентной оболочке. В связи с этим карбены являются высокореактивными электрофилами и образуются в качестве промежуточных продуктов реакции. [9] Синглетный карбен содержит пустую p- орбиталь и гибридную орбиталь примерно sp 2 с двумя электронами. Синглетные карбены стереоспецифично присоединяются к алкенам, и стереохимия алкенов сохраняется в циклопропановом продукте. [1] Механизм присоединения карбена к алкену представляет собой согласованное [2+1] циклоприсоединение (см. рисунок). Карбены, полученные из хлороформа или бромоформа, можно использовать для присоединения CX 2 к алкену с образованием дигалоциклопропана, тогда как реагент Симмонса-Смита добавляет CH 2 . [10]

Взаимодействие заполненной карбеновой орбитали с π-системой алкена создает четырехэлектронную систему и способствует нелинейному подходу. Также выгодно смешивать пустую p -орбиталь карбена с заполненной π-орбиталью алкена. Благоприятное смешивание происходит за счет нелинейного подхода (см. рисунок справа). Однако, хотя теория явно отдает предпочтение нелинейному подходу, нет очевидных экспериментальных последствий для линейного или нелинейного подхода. [1]