Математические модели могут прогнозировать развитие инфекционных заболеваний , показывать вероятный исход эпидемии ( в том числе среди растений ) и помогать информировать общественное здравоохранение и меры по охране растений. Модели используют базовые предположения или собранную статистику вместе с математическими вычислениями для поиска параметров различных инфекционных заболеваний и используют эти параметры для расчета эффектов различных вмешательств, таких как программы массовой вакцинации . Моделирование может помочь решить, каких вмешательств следует избегать, а какие опробовать, или предсказать будущие модели роста и т. д.
Моделирование инфекционных заболеваний — это инструмент, который использовался для изучения механизмов распространения заболеваний, для прогнозирования будущего развития вспышки и оценки стратегий борьбы с эпидемией. [1]
Первым ученым, который систематически пытался количественно оценить причины смерти, был Джон Граун в своей книге « Естественные и политические наблюдения над счетами смертности» в 1662 году. Счета, которые он изучал, представляли собой списки чисел и причин смертей, публикуемые еженедельно. Анализ причин смерти Граунта считается началом «теории конкурирующих рисков», которая, по мнению Дейли и Гани [1], является «теорией, которая в настоящее время прочно утвердилась среди современных эпидемиологов».
Самый ранний отчет о математическом моделировании распространения болезней был выполнен в 1760 году Даниэлем Бернулли . Получив медицинское образование, Бернулли создал математическую модель, защищающую практику прививок от оспы . [2] Расчеты по этой модели показали, что всеобщая прививка против оспы увеличит продолжительность жизни с 26 лет 7 месяцев до 29 лет 9 месяцев. [3] Работа Даниэля Бернулли предшествовала современному пониманию теории микробов . [4]
В начале 20 века Уильям Хамер [5] и Рональд Росс [6] применили закон действия масс для объяснения поведения эпидемий.
В 1920-е годы появились секционные модели. Эпидемическая модель Кермака -Маккендрика (1927 г.) и эпидемическая модель Рида-Фроста (1928 г.) описывают взаимоотношения между восприимчивыми , инфицированными и иммунными людьми в популяции. Эпидемическая модель Кермака-Маккендрика успешно предсказала поведение вспышек, очень похожее на то, которое наблюдалось во многих зарегистрированных эпидемиях. [7]
В последнее время агентные модели (ABM) стали использоваться взамен более простых секционных моделей . [8] Например, эпидемиологические ПРО использовались для информирования о мерах общественного здравоохранения (нефармацевтических) против распространения SARS-CoV-2 . [9] Эпидемиологические ПРО, несмотря на их сложность и требующие высокой вычислительной мощности, подвергались критике за упрощение и нереалистичность предположений. [10] [11] Тем не менее, они могут быть полезны при принятии решений относительно мер по смягчению и подавлению в случаях, когда ПРО точно откалиброваны. [12]
Модели хороши настолько, насколько хороши предположения, на которых они основаны. Если модель делает прогнозы, которые не соответствуют наблюдаемым результатам, а математические расчеты верны, первоначальные предположения должны измениться, чтобы модель стала полезной. [13]
«Стохастический» означает наличие или наличие случайной величины. Стохастическая модель — это инструмент для оценки распределения вероятностей потенциальных результатов, допускающий случайные изменения одного или нескольких входных данных с течением времени. Стохастические модели зависят от случайных изменений риска заражения, заболевания и динамики других заболеваний. Статистическое распространение заболевания на уровне агента в небольших или больших популяциях можно определить стохастическими методами. [14] [15] [16]
При работе с большими популяциями, как в случае с туберкулезом, часто используются детерминированные или фрагментарные математические модели. В детерминированной модели отдельные лица в популяции распределяются по разным подгруппам или сегментам, каждая из которых представляет определенную стадию эпидемии. [17]
Скорости перехода из одного класса в другой математически выражаются в виде производных, поэтому модель формулируется с использованием дифференциальных уравнений. При построении таких моделей необходимо исходить из того, что численность населения в каком-либо компартменте дифференцируема во времени и что эпидемический процесс носит детерминированный характер. Другими словами, изменения в численности населения компартмента можно рассчитать, используя только историю, которая использовалась для разработки модели. [7]
Распространенное объяснение роста эпидемий состоит в том, что 1 человек заражает 2, эти 2 заражают 4 и так далее и так далее, причем число инфицированных удваивается каждое поколение. Это аналогично игре в метки , где 1 человек отмечает 2, эти 2 отмечают 4 других, которых никогда не отмечали, и так далее. По ходу игры она становится все более безумной, поскольку помеченные пробегают мимо ранее помеченных, чтобы выследить тех, кого никогда не помечали. Таким образом, эта модель эпидемии приводит к кривой, которая растет в геометрической прогрессии, пока не упадет до нуля, поскольку все население инфицировано. т.е. нет коллективного иммунитета и нет пика и постепенного снижения, как это наблюдается в действительности. [18]
Эпидемии можно моделировать как болезни, распространяющиеся через сети контактов между людьми. Такую сеть можно математически представить в виде графа , и она называется контактной сетью. [19] Каждый узел в контактной сети представляет собой человека, и каждое звено (ребро) между парой узлов представляет собой контакт между ними. Связи в контактных сетях могут использоваться для передачи заболевания между людьми, и каждое заболевание имеет свою собственную динамику поверх своей контактной сети. Сочетание динамики заболевания под влиянием вмешательств, если таковые имеются, в контактной сети можно смоделировать с помощью другой сети, известной как сеть передачи. В сети передачи за передачу заболевания отвечают все звенья. Если такая сеть является локально древовидной сетью, то есть любая локальная окрестность в такой сети принимает форму дерева , то базовое воспроизведение можно записать через среднюю степень избытка передающей сети так, что:
где – средняя степень (средняя степень) сети, а – второй момент распределения степени сети передачи . Однако не всегда легко найти сеть передачи вне контактной сети и динамики заболевания. [20] Например, если сеть контактов может быть аппроксимирована графиком Эрдеша-Реньи с распределением степеней Пуассона , а параметры распространения заболевания такие, как определено в приведенном выше примере, то есть скорость передачи на человека и болезнь имеет средний период заражения , то базовое число воспроизводства равно [21] [22], поскольку для распределения Пуассона.
Базовое число воспроизводства (обозначается R 0 ) является мерой того, насколько переносима болезнь. Это среднее число людей, которых заразит один заразный человек за время заражения. Это количество определяет, будет ли инфекция расти субэкспоненциально , исчезнет или останется постоянной: если R 0 > 1, то каждый человек в среднем заражает более одного человека, поэтому болезнь будет распространяться; если R 0 < 1, то каждый человек в среднем заражает менее одного человека, поэтому болезнь вымирает; а если R 0 = 1, то каждый человек заразит в среднем ровно одного человека, поэтому болезнь станет эндемической: она распространится по всей популяции, но не увеличится и не уменьшится. [23]
Инфекционное заболевание считается эндемичным , если оно может поддерживаться в популяции без необходимости внешних воздействий. Это означает, что в среднем каждый зараженный человек заражает ровно одного другого человека (если больше, то число инфицированных вырастет субэкспоненциально , и возникнет эпидемия , меньше – и болезнь вымрет). Говоря математическим языком, это:
Базовый коэффициент воспроизводства ( R 0 ) болезни, предполагая, что все восприимчивы, умноженный на долю населения, которая действительно восприимчива ( S ), должен быть равен единице (поскольку те, кто не восприимчив, не учитываются в наших расчетах, поскольку они не могут заразиться болезнью). Обратите внимание: это соотношение означает, что для того, чтобы болезнь находилась в устойчивом эндемическом состоянии , чем выше базовый коэффициент воспроизводства, тем ниже должна быть доля восприимчивого населения, и наоборот. Это выражение имеет ограничения, касающиеся доли восприимчивости, например, R 0 равно 0,5, что означает, что S должно быть равно 2, однако эта доля превышает размер популяции. [ нужна цитата ]
Предположим, что распределение по возрасту прямоугольное, а возраст заражения имеет одинаковое распределение для каждого года рождения. Пусть средний возраст заражения равен A , например, когда люди моложе A восприимчивы, а люди старше A имеют иммунитет (или заразны). Тогда можно с помощью простого аргумента показать, что доля восприимчивого населения определяется выражением:
Мы еще раз повторяем, что L — это возраст, в котором в этой модели предполагается, что каждый человек умирает. Но математическое определение эндемического устойчивого состояния можно переформулировать следующим образом:
Следовательно, в силу транзитивного свойства :
Это обеспечивает простой способ оценки параметра R 0 с использованием легкодоступных данных.
Для населения с экспоненциальным возрастным распределением
Это позволяет определить базовое репродуктивное число заболевания с учетом A и L при любом типе распределения населения.
Компартментальные модели сформулированы как цепи Маркова . [24] Классической моделью в эпидемиологии является модель SIR, которую можно использовать как простую модель для моделирования эпидемий. Также используются несколько других типов секционных моделей.


В 1927 году У. О. Кермак и А. Г. Маккендрик создали модель, в которой они рассматривали фиксированную популяцию только с тремя компартментами: восприимчивая, ; зараженный, ; и выздоровел, . Отсеки, используемые в этой модели, состоят из трех классов: [25]
Существует множество модификаций модели SIR, в том числе те, которые включают рождения и смерти, где при выздоровлении иммунитет отсутствует (модель SIS), где иммунитет сохраняется лишь в течение короткого периода времени (SIRS), где имеется латентный период заболевание, при котором человек не заразен ( SEIS и SEIR ) и при котором дети могут рождаться с иммунитетом (MSIR). [ нужна цитата ]
Математические модели должны интегрировать растущий объем данных, генерируемых о взаимодействии хозяина и патогена . Этой проблеме посвящены многие теоретические исследования динамики популяций , структуры и эволюции инфекционных болезней растений и животных, в том числе человека. [26]
Темы исследований включают в себя:
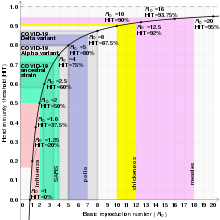
Если доля населения, обладающего иммунитетом, превышает уровень коллективного иммунитета к заболеванию, то болезнь больше не может персистировать в популяции и ее передача прекращается. [27] Таким образом, болезнь может быть устранена из популяции, если достаточное количество людей имеют иммунитет благодаря вакцинации или восстановлению после предыдущего заражения болезнью. Например, ликвидация оспы (последний дикий случай произошел в 1977 г.) и сертификация ликвидации местной передачи 2 из 3 типов дикого полиовируса (тип 2 в 2015 г., после последнего зарегистрированного случая в 1999 г., и тип 3 в 2019 г.). , после последнего зарегистрированного случая в 2012 году). [28]
Уровень коллективного иммунитета будем обозначать q . Напомним , что для стабильного состояния :
По очереди,
что примерно равно: [ нужна ссылка ]
S будет равно (1 − q ), поскольку q — это доля населения, обладающего иммунитетом, а q + S должно равняться единице (поскольку в этой упрощенной модели все либо восприимчивы, либо невосприимчивы). Затем:
Помните, что это пороговый уровень. Смерть от передачи произойдет только в том случае, если доля иммунных лиц превысит этот уровень из-за программы массовой вакцинации.
Мы только что рассчитали критический порог иммунизации (обозначенный q c ). Это минимальная доля населения, которая должна быть иммунизирована при рождении (или незадолго до рождения), чтобы инфекция в популяции вымерла.
Потому что доля окончательной численности популяции p , которая никогда не инфицирована, может быть определена как:
Следовательно,
Решая для , получаем:
Если используемая вакцина недостаточно эффективна или требуемый охват не может быть достигнут, программа может не превысить q c . Такая программа защитит привитых от болезней, но может изменить динамику передачи. [ нужна цитата ]
Предположим, что часть населения q (где q < q c ) при рождении иммунизирована против инфекции с R 0 > 1. Программа вакцинации меняет R 0 на R q , где
Это изменение происходит просто потому, что сейчас среди населения меньше восприимчивых людей, которые могут заразиться. R q — это просто R 0 минус те, кто обычно был бы заражен, но не может быть заражен сейчас, поскольку у них есть иммунитет.
Вследствие этого более низкого базового репродуктивного числа средний возраст заражения A также изменится на некоторое новое значение A q у тех, кто остался непривитым.
Вспомним отношение, связывающее R 0 , A и L . Если предположить , что продолжительность жизни не изменилась, то теперь :
Но R 0 = L / A , так что:
Таким образом, программа вакцинации может повысить средний возраст заражения, а у непривитых лиц будет наблюдаться снижение силы заражения из-за присутствия вакцинированной группы. Что касается заболевания, которое приводит к большей клинической тяжести у пожилых людей, непривитая часть населения может заболеть заболеванием относительно позже в жизни, чем это произошло бы в отсутствие вакцины.
Если программа вакцинации приведет к тому, что доля иммунных лиц в популяции превысит критический порог в течение значительного периода времени, передача инфекционного заболевания в этой популяции прекратится. Если элиминация происходит повсюду одновременно, то это может привести к ликвидации . [ нужна цитата ]
Преимущество моделей заключается в одновременном изучении нескольких результатов вместо того, чтобы делать единый прогноз. Модели продемонстрировали широкую степень надежности при прошлых пандемиях, таких как SARS , SARS-CoV-2 , [29] Свиной грипп , MERS и Эбола . [30]
{{cite journal}}: Требуется цитировать журнал |journal=( помощь ){{cite journal}}: CS1 maint: DOI inactive as of April 2024 (link){{cite book}}: CS1 maint: location (link)