Органическая фотохимия включает в себя органические реакции , вызываемые действием света. [1] [2] Поглощение ультрафиолетового света органическими молекулами часто приводит к реакциям. Раньше использовался солнечный свет, а в наше время используются ультрафиолетовые лампы. Органическая фотохимия оказалась очень полезным синтетическим инструментом. Сложные органические продукты можно получить просто.
Ранние примеры часто обнаруживались путем наблюдения за осадками или изменениями цвета образцов, подвергшихся воздействию солнечного света. Первый зарегистрированный случай был описан Чамицианом, когда солнечный свет превращал сантонин в желтый фотопродукт: [3]

Ранним примером осадка была фотодимеризация антрацена , охарактеризованная Юлием Федоровичем Фриче и подтвержденная Эльбсом. [4] Подобные наблюдения были сосредоточены на димеризации коричной кислоты в труксиловую кислоту . В настоящее время известны многие фотодимеры, например димер пиримидина , тиофосген , диамантан .
Другой пример был обнаружен Эгбертом Хавингой в 1956 году. [5] Любопытным результатом была активация при фотолизе мета-нитрогруппой в отличие от обычной активации орто- и пара-группами.
Органическая фотохимия продвинулась вперед с разработкой правил Вудворда-Гоффмана . [6] [7] Показательно, что эти правила помогают рационализировать фотохимически обусловленное электроциклическое замыкание кольца гекса-2,4-диена, которое происходит дисротационным образом.
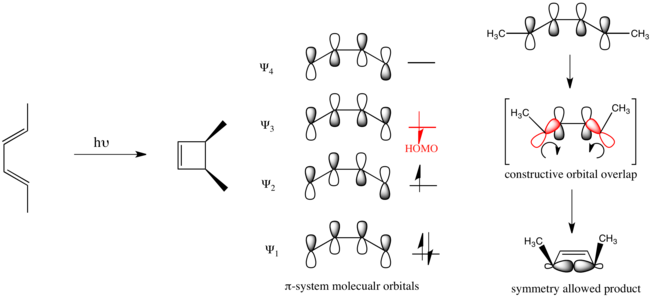
Органические реакции, подчиняющиеся этим правилам, называются разрешенными по симметрии. Реакции, идущие противоположным путем, запрещены по симметрии и требуют значительно больше энергии, чтобы протекать, если они вообще происходят.
Органические фотохимические реакции объясняются с точки зрения соответствующих возбужденных состояний . [8] [9]
Параллельно со структурными исследованиями, описанными выше, оценивалась роль спиновой множественности – синглетной или триплетной – на реакционную способность. Подчеркнута важность триплетно-возбужденных видов. Триплеты, как правило, живут дольше, чем синглеты, и имеют более низкую энергию, чем синглет той же конфигурации. Триплеты могут возникать в результате (А) преобразования первоначально образовавшихся синглетов или (Б) взаимодействия с триплетом с более высокой энергией (сенсибилизация).
Возможно гашение триплетных реакций. [10]
Обычные органические фотохимические реакции включают: тип Норриша I , тип Норриша II , рацемизацию оптически активных бифенилов, циклогексадиеноновую перегруппировку типа А, циклогексеноновую перегруппировку типа B, ди- π -метановую перегруппировку , бициклотип B. перегруппировка ]гексанона в фенолы, фотохимические электроциклические процессы, перегруппировка эпоксикетонов в бета-дикетоны, раскрытие цикла циклопропилкетонов, гетеролиз 3,5-диметоксилбензильных производных и фотохимические циклизации диенов.

Реагенты фотореакций могут быть как газообразными, так и жидкими. [11] Как правило, необходимо подносить реагенты близко к источнику света, чтобы получить максимально возможную светоотдачу . Для этой цели реакционную смесь можно облучать либо непосредственно, либо в проточном боковом рукаве реактора подходящим источником света. [12]
Недостатком фотохимических процессов является низкая эффективность преобразования электрической энергии в энергию излучения необходимой длины волны . Помимо излучения, источники света генерируют много тепла, что, в свою очередь, требует энергии охлаждения. Кроме того, большинство источников света излучают полихроматический свет, хотя необходим только монохроматический свет . [13] Однако высокий квантовый выход компенсирует эти недостатки.
Работа при низких температурах выгодна, поскольку позволяет избежать побочных реакций (поскольку повышается селективность) и увеличивается выход (поскольку газообразные реагенты меньше вытесняются из растворителя).
Исходные материалы иногда можно охладить перед реакцией до такой степени, что тепло реакции поглощается без дальнейшего охлаждения смеси. В случае газообразных или низкокипящих исходных материалов необходима работа под избыточным давлением. Из-за большого количества возможного сырья описано большое количество процессов. [14] [15] Крупномасштабные реакции обычно проводятся в реакторе с мешалкой , барботажном колонном реакторе или трубчатом реакторе с последующей дальнейшей обработкой в зависимости от целевого продукта. [16] В случае реактора с мешалкой лампа (обычно имеющая форму удлиненного цилиндра) снабжается охлаждающей рубашкой и помещается в реакционный раствор. Трубчатые реакторы изготавливаются из кварцевых или стеклянных трубок, которые облучаются снаружи. Преимущество использования реактора с мешалкой заключается в том, что свет не теряется в окружающую среду. Однако интенсивность света быстро падает с увеличением расстояния до источника света из-за адсорбции реагентов. [12]
Влияние излучения на скорость реакции часто можно представить степенным законом , основанным на плотности квантового потока, т.е. мольного кванта света (ранее измерявшегося в единицах Эйнштейна ) на площадь и время. Поэтому одной из целей проектирования реакторов является определение экономически наиболее выгодных размеров с точки зрения оптимизации плотности квантового тока. [17]
Олефины димеризуются под действием УФ-излучения. [18]
Совершенно параллельно примеру с сантонином в люмисантонин происходит перегруппировка 4,4-дифенилциклогексадиенона [9]. Здесь n-pi* -триплетное возбужденное состояние подвергается той же бета-бета-связи. За этим следует межсистемное пересечение (т.е. ISC) с образованием синглетного основного состояния, которое рассматривается как цвиттер-ион . Последним шагом является перегруппировка в бициклический фотопродукт. Реакция называется циклогексадиеноновой перегруппировкой типа А.
Чтобы предоставить дополнительные доказательства механизма диенона, в котором существует связь между двумя двойными связями, здесь представлен случай 4,4-дифенилциклогексенона. Видно, что перегруппировка совершенно иная; таким образом, для перегруппировки типа А необходимы две двойные связи. При одной двойной связи одна из фенильных групп, первоначально находившаяся в положении С-4, мигрировала к С-3 (т.е. к бета-углероду). [19]
Когда одна из арильных групп имеет парациано- или пара-метоксигруппу, эта замещенная арильная группа мигрирует преимущественно. [20] Исследование альтернативных видов фенониевого типа, в которых арильная группа начала мигрировать к бета-углероду, выявило большую делокализацию электрона с пара-заместителем в мигрирующей арильной группе и, следовательно, более стабилизированный путь.

Еще одним типом фотохимической реакции является ди- π -метановая перегруппировка . [21] Еще двумя ранними примерами были перегруппировка 1,1,5,5-тетрафенил-3,3-диметил-1,4-пентадиена (молекула «Мариано») [22] и перегруппировка баррелена в семибуллвален . [23] Отметим, что в отличие от циклогексадиеноновых реакций, в которых используются возбужденные состояния n- π *, в перегруппировках ди- π -метана используются возбужденные состояния π - π *.
При фотоокислительно-восстановительном катализе фотон поглощается сенсибилизатором (молекулой или ионом антенны), который затем вызывает окислительно-восстановительные реакции на органическом субстрате. Распространенным сенсибилизатором является трис(бипиридин) рутения(II) . Иллюстрацией фотоокислительно-восстановительного катализа являются некоторые реакции аминотрифторметилирования. [24]

Фотохлорирование — одно из крупнейших применений фотохимии в органическом синтезе. Однако фотон поглощается не органическим соединением, а хлором . Фотолиз Cl 2 дает атомы хлора, которые отрывают атомы H от углеводородов, что приводит к хлорированию.
{{cite journal}}: CS1 maint: числовые имена: список авторов ( ссылка )