1-Пропанол (также пропан-1-ол , пропанол , н-пропиловый спирт ) — первичный спирт с формулой CH 3 CH 2 CH 2 OH и иногда представленный как PrOH или n -PrOH . Это бесцветная жидкость и изомер 2- пропанола . Он образуется естественным путем в небольших количествах в ходе многих процессов ферментации и используется в фармацевтической промышленности в качестве растворителя , главным образом для смол и эфиров целлюлозы , а иногда и как дезинфицирующее средство.
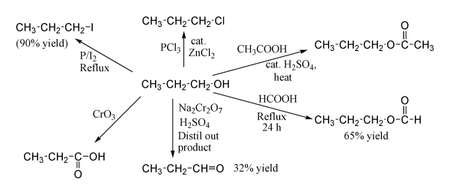
1-Пропанол демонстрирует нормальные реакции первичного спирта . Таким образом, его можно превратить в алкилгалогениды ; например, красный фосфор и йод дают н-пропилйодид с выходом 80%, а PCl 3 с каталитическим ZnCl 2 дает н-пропилхлорид . Реакция с уксусной кислотой в присутствии катализатора H 2 SO 4 в условиях этерификации Фишера дает пропилацетат , тогда как кипячение пропанола с обратным холодильником в течение ночи с одной муравьиной кислотой может дать пропилформиат с выходом 65%. Окисление 1-пропанола Na 2 Cr 2 O 7 и H 2 SO 4 дает 36% выход пропиональдегида , поэтому для этого типа реакции рекомендуются более высокопроизводительные методы с использованием PCC или окисления Сверна . Окисление хромовой кислотой дает пропионовую кислоту .
1- Пропанол получают каталитическим гидрированием пропиональдегида . Пропиональдегид получают оксо- процессом гидроформилированием этилена с использованием монооксида углерода и водорода в присутствии катализатора, такого как октакарбонил кобальта или комплекс родия . [5]
Традиционное лабораторное получение 1-пропанола включает обработку н -пропилйодида влажным Ag 2 O .
Считается, что 1-пропанол аналогичен этанолу по своему воздействию на организм человека, но, согласно исследованию, проведенному на кроликах, в 2–4 раза более эффективен. Многие токсикологические исследования показывают, что острая ЛД 50 при пероральном приеме варьируется от 1,9 г/кг до 6,5 г/кг (по сравнению с 7,06 г/кг для этанола). Метаболизируется в пропионовую кислоту . Последствия включают алкогольную интоксикацию и метаболический ацидоз с высокой анионной щелью . По состоянию на 2011 год был зарегистрирован один случай смертельного отравления после перорального приема 500 мл 1-пропанола. [6] Из-за отсутствия долгосрочных данных канцерогенность 1-пропанола для человека неизвестна.
1-Пропанол имеет высокое октановое число и пригоден для использования в качестве моторного топлива. Однако пропанол слишком дорог для использования в качестве моторного топлива. Октановое число (RON) пропанола по исследовательскому методу составляет 118, а антидетонационный индекс (AKI) — 108. [7]