Семейство Bcl-2 (TC# 1.A.21) состоит из ряда эволюционно консервативных белков, которые имеют общие домены гомологии Bcl-2 (BH). Семейство Bcl-2 наиболее примечательно своей регуляцией апоптоза — формы запрограммированной гибели клеток в митохондриях . [2] Белки семейства Bcl-2 состоят из членов, которые либо способствуют, либо ингибируют апоптоз и контролируют апоптоз, регулируя проницаемость внешней мембраны митохондрий (MOMP), что является ключевым этапом внутреннего пути апоптоза. К 2008 году было идентифицировано 25 генов семейства Bcl-2.
Члены семейства BCL-2 регулируют апоптоз у млекопитающих, рептилий, земноводных, рыб и других типов многоклеточных животных, за исключением нематод и насекомых. [3] Их молекулярная структура и функция, а также динамика белков хорошо сохраняются на протяжении сотен миллионов лет в тканеобразующих формах жизни. [4]

Белки семейства Bcl-2 имеют общую структуру, состоящую из гидрофобной α-спирали, окруженной амфипатическими α-спиралями. Некоторые члены семейства имеют трансмембранные домены на С-конце, которые в первую очередь служат для их локализации в митохондриях.
Bcl-x(L) имеет длину 233 аминокислотных остатка (aas) и в мембране имеет один предполагаемый очень гидрофобный трансмембранный α-спиральный сегмент (остатки 210–226). Гомологи Bcl-x включают белки Bax (крыса; 192 аминокислоты) и Bak (мышь; 208 аминокислот), которые также влияют на апоптоз. Структура с высоким разрешением мономерной растворимой формы человеческого Bcl-x(L) была определена как рентгеновской кристаллографией, так и ЯМР. [6]
Структура состоит из двух центральных преимущественно гидрофобных α-спиралей, окруженных амфипатическими спиралями. Расположение α-спиралей в Bcl-X(L) напоминает таковое для дифтерийного токсина и колицинов . Дифтерийный токсин образует трансмембранную пору и переносит токсичный каталитический домен в цитоплазму клеток животных. Колицины аналогичным образом образуют поры в липидных бислоях. Таким образом, структурная гомология предполагает, что члены семейства Bcl-2, которые содержат домены BH1 и BH2 (Bcl-X(L) Bcl-2 и Bax), функционируют одинаково.
Члены семейства Bcl-2 имеют один или несколько характерных доменов гомологии , называемых доменами гомологии Bcl-2 (BH) (названными BH1, BH2, BH3 и BH4) (см. рисунок). Известно, что домены BH имеют решающее значение для функционирования, поскольку удаление этих доменов посредством молекулярного клонирования влияет на скорость выживаемости/апоптоза. Антиапоптотические белки Bcl-2, такие как Bcl-2 и Bcl-xL, сохраняют все четыре домена BH. Домены BH также служат для разделения проапоптотических белков Bcl-2 на белки с несколькими доменами BH (например, Bax и Bak) или на белки, которые имеют только домен BH3 (например, Bim Bid и BAD ).
Все белки, принадлежащие к семейству Bcl-2 [7], содержат домен BH1, BH2, BH3 или BH4. Все антиапоптотические белки содержат домены BH1 и BH2, некоторые из них содержат дополнительный N-концевой домен BH4 (Bcl-2, Bcl-x(L) и Bcl-w), который также наблюдается в некоторых проапоптотических белках, таких как Bcl-x(S), Дива, Бок-Л и Бок-С. С другой стороны, все проапоптотические белки содержат домен BH3, необходимый для димеризации с другими белками семейства Bcl-2 и имеющий решающее значение для их убийственной активности, некоторые из них также содержат домены BH1 и BH2 (Bax и Bak). Домен BH3 также присутствует в некоторых антиапоптотических белках, таких как Bcl-2 или Bcl-x(L). Три функционально важных участка гомологии Bcl-2 (BH1, BH2 и BH3) находятся в непосредственной пространственной близости. Они образуют удлиненную щель, которая может служить местом связывания для других членов семейства Bcl-2.
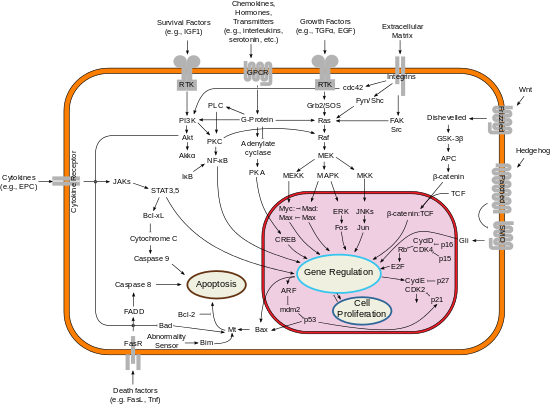
Регулируемая гибель клеток ( апоптоз ) индуцируется такими событиями, как удаление факторов роста и токсинов. Он контролируется регуляторами, которые либо оказывают ингибирующее действие на запрограммированную гибель клеток (антиапоптотическое), либо блокируют защитное действие ингибиторов (проапоптотическое). [8] [9] Многие вирусы нашли способ противодействия защитному апоптозу путем кодирования собственных генов антиапоптоза, предотвращающих слишком раннюю гибель клеток-мишеней.
Bcl-x является доминантным регулятором запрограммированной гибели клеток в клетках млекопитающих. [10] [11] Длинная форма ( Bcl-x(L)) проявляет активность репрессора гибели клеток, но короткая изоформа (Bcl-x(S)) и β-изоформа (Bcl-xβ) способствуют гибели клеток. -x(L), Bcl-x(S) и Bcl-xβ представляют собой три изоформы , полученные путем альтернативного сплайсинга РНК .
Существует ряд теорий относительно того, как семейство генов Bcl-2 оказывает про- или антиапоптотический эффект. Важным из них является то, что это достигается за счет активации или инактивации внутренней переходной поры проницаемости митохондрий , которая участвует в регуляции матрикса Ca 2+ , pH и напряжения. Также считается, что некоторые белки семейства Bcl-2 могут индуцировать (проапоптотические члены) или ингибировать (антиапоптотические члены) высвобождение цитохрома с в цитозоль , который, оказавшись там, активирует каспазу-9 и каспазу-3, что приводит к к апоптозу. Хотя Замзами и др. предполагают, что высвобождение цитохрома с косвенно опосредовано порой PT на внутренней мембране митохондрий, [12] убедительные доказательства позволяют предположить более раннее влияние поры MAC на внешнюю мембрану. [13] [14]
Другая теория предполагает, что белки Rho играют роль в активации Bcl-2, Mcl-1 и Bid. Ингибирование Rho снижает экспрессию антиапоптотических белков Bcl-2 и Mcl-1 и увеличивает уровни проапоптотических белков Bid, но не влияет на уровни Bax или FLIP. Ингибирование Rho индуцирует каспазу-9 и каспазу-3-зависимый апоптоз культивируемых эндотелиальных клеток человека. [15]
Эти белки локализованы на внешней митохондриальной мембране животной клетки, где, как полагают, они образуют комплекс с порином потенциалзависимых анионных каналов (VDAC). Взаимодействие Bcl-2 с VDAC1 или с пептидами, полученными из VDAC3, защищает от гибели клеток путем ингибирования высвобождения цитохрома с. Было продемонстрировано прямое взаимодействие Bcl-2 с очищенным двухслойным VDAC, при этом Bcl-2 снижает проводимость канала. [16]
Внутри митохондрий находятся апоптогенные факторы (цитохром с, гомолог Smac/Diablo , Omi), которые при высвобождении активируют исполнителей апоптоза — каспазы . [17] В зависимости от своей функции, после активации белки Bcl-2 либо способствуют высвобождению этих факторов, либо удерживают их в митохондриях. В то время как активированные проапоптозные Bak и/или Bax будут образовывать MAC и опосредовать высвобождение цитохрома с, антиапоптотический Bcl-2 будет блокировать его, возможно, посредством ингибирования Bax и/или Bak. [18]
Белки семейства Bcl-2 также присутствуют в перинуклеарной оболочке и широко распространены во многих тканях организма. Их способность образовывать олигомерные поры в искусственных липидных бислоях документирована, но физиологическое значение образования пор неясно. Каждый из этих белков обладает отличительными свойствами, включая некоторую степень ионной селективности. [19]
The generalized transport reaction proposed for membrane-embedded, oligomeric Bcl-2 family members is:
The BH3-only subset of the Bcl-2 family of proteins contain only a single BH3-domain. The BH3-only members play a key role in promoting apoptosis. The BH3-only family members are Bim, Bid, BAD and others. Various apoptotic stimuli induce expression and/or activation of specific BH3-only family members, which translocate to the mitochondria and initiate Bax/Bak-dependent apoptosis.[20]
Proteins that are known to contain these domains include vertebrate Bcl-2 (alpha and beta isoforms) and Bcl-x (isoforms Bcl-x(L).
На момент редактирования в этой статье используется контент из «1.A.21 The Bcl-2 (Bcl-2) Family» , который лицензируется таким образом, чтобы его можно было повторно использовать в соответствии с непортированной лицензией Creative Commons Attribution-ShareAlike 3.0 , но не в рамках ГФДЛ . Все соответствующие условия должны быть соблюдены.