Карбид бора (химическая формула примерно B 4 C) представляет собой чрезвычайно твердую бор - углеродную керамику , ковалентный материал, используемый в танковой броне , бронежилетах , диверсионных порохах для двигателей [2] , а также в многочисленных промышленных применениях. Имея твердость по Виккерсу >30 ГПа, это один из самых твердых известных материалов после кубического нитрида бора и алмаза . [3]
Карбид бора был открыт в XIX веке как побочный продукт реакций с участием боридов металлов, но его химическая формула была неизвестна. Лишь в 1930-х годах химический состав был оценен как B 4 C. [4] Остались споры относительно того, имел ли материал эту точную стехиометрию 4: 1 , поскольку на практике материал всегда имеет небольшой дефицит углерода с Что касается этой формулы, то рентгеновская кристаллография показывает, что ее структура очень сложна, со смесью цепей CBC и икосаэдров B 12 .
Эти особенности противоречили очень простой точной эмпирической формуле B 4 C. [5] Из-за структурной единицы В 12 химическую формулу «идеального» карбида бора часто записывают не как В 4 С, а как В 12 С 3 , а дефицит углерода в карбиде бора описывают сочетанием агрегаты B 12 C 3 и B 12 CBC.
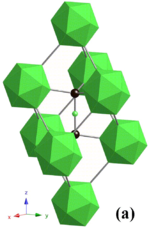

Карбид бора имеет сложную кристаллическую структуру, типичную для боридов на основе икосаэдра . Там икосаэдры B 12 образуют ромбоэдрическую единицу решетки (пространственная группа: R 3 m (№ 166), постоянные решетки: a = 0,56 нм и c = 1,212 нм), окружающую цепь CBC, находящуюся в центре элементарной ячейки , и оба атома углерода соединяют три соседних икосаэдра. Эта структура является слоистой: икосаэдры B 12 и мостиковые атомы углерода образуют плоскость сетки, которая распространяется параллельно плоскости c и укладывается вдоль оси c . Решетка имеет две основные структурные единицы — икосаэдр B 12 и октаэдр B 6 . Из-за небольшого размера октаэдров B 6 они не могут соединяться между собой. Вместо этого они связываются с икосаэдрами B 12 в соседнем слое, и это снижает прочность связи в c -плоскости. [6]
Из-за структурной единицы B 12 химическую формулу «идеального» карбида бора часто записывают не как B 4 C, а как B 12 C 3 , а дефицит углерода карбида бора описывают через комбинацию B 12 С 3 и В 12 С 2 ед. [5] [7] Некоторые исследования указывают на возможность включения одного или нескольких атомов углерода в икосаэдры бора, что приводит к появлению таких формул, как (B 11 C)CBC = B 4 C на тяжелом углеродном конце стехиометрии, но такие формулы, как B 12 (CBB) = B 14 C на конце, богатом бором. Таким образом, «карбид бора» представляет собой не одно соединение, а семейство соединений различного состава. Обычным промежуточным соединением, которое приближается к обычно встречающемуся соотношению элементов, является B 12 (CBC) = B 6,5 C. [8] Квантово-механические расчеты показали, что конфигурационный беспорядок между атомами бора и углерода в различных положениях в кристалле определяет некоторые из свойства материалов – в частности, кристаллическая симметрия композиции B 4 C [9] и неметаллический электрический характер композиции B 13 C 2 . [10]
Карбид бора известен как прочный материал, обладающий чрезвычайно высокой твердостью (от 9,5 до 9,75 по шкале Мооса ), высоким поперечным сечением поглощения нейтронов (т.е. хорошими экранирующими свойствами против нейтронов), устойчивостью к ионизирующему излучению и большинству химических веществ. [11] Его твердость по Виккерсу (38 ГПа), модуль упругости (460 ГПа) [12] и вязкость разрушения (3,5 МПа·м 1/2 ) приближаются к соответствующим значениям для алмаза (1150 ГПа и 5,3 МПа·м 1/2 ). . [13]
По состоянию на 2015 год [обновлять]карбид бора является третьим по твердости известным веществом после алмаза и кубического нитрида бора , за что получил прозвище «черный алмаз». [14] [15]
Карбид бора — полупроводник , в электронных свойствах которого преобладает транспорт прыжкового типа. [8] Ширина запрещенной зоны зависит от состава, а также от степени порядка. Ширина запрещенной зоны оценивается в 2,09 эВ, причем несколько состояний в середине запрещенной зоны усложняют спектр фотолюминесценции . [8] Обычно это материал p-типа.
Карбид бора был впервые синтезирован Анри Муассаном в 1899 году [7] путем восстановления триоксида бора углеродом или магнием в присутствии углерода в электродуговой печи . В случае углерода реакция протекает при температуре выше температуры плавления B 4 C и сопровождается выделением большого количества окиси углерода : [16]
Если используется магний, реакцию можно проводить в графитовом тигле , а побочные продукты магния удаляют обработкой кислотой. [17]


По своей твердости:
Для других объектов недвижимости:
Способность карбида бора поглощать нейтроны без образования долгоживущих радионуклидов делает его привлекательным в качестве поглотителя нейтронного излучения, возникающего на атомных электростанциях [18] и от противопехотных нейтронных бомб . Ядерные применения карбида бора включают защиту. [11]
... карбид бора является третьим по твердости материалом на Земле.