
В материаловедении химическая силовая микроскопия ( CFM ) является разновидностью атомно - силовой микроскопии (AFM), которая стала универсальным инструментом для характеристики поверхностей материалов . С помощью AFM структурная морфология исследуется с использованием простых режимов постукивания или контакта, которые используют ван-дер-ваальсовы взаимодействия между зондом и образцом для поддержания постоянной амплитуды отклонения зонда (режим постоянной силы) или поддержания высоты при измерении отклонения зонда (режим постоянной высоты). CFM, с другой стороны, использует химические взаимодействия между функционализированным зондовым наконечником и образцом. Химия выбора, как правило, представляет собой позолоченный наконечник и поверхность с прикрепленными тиолами R−SH , где R являются интересующими функциональными группами . CFM позволяет определять химическую природу поверхностей, независимо от их конкретной морфологии, и облегчает исследования базовой энтальпии химических связей и поверхностной энергии . Как правило, CFM ограничена тепловыми колебаниями внутри кантилевера, удерживающего зонд. Это ограничивает разрешение измерения силы до ~1 пН, что все еще очень приемлемо, учитывая, что слабые взаимодействия COOH/CH 3 составляют ~20 пН на пару. [1] [2] Гидрофобность используется в качестве основного примера в этом рассмотрении CFM, но, безусловно, любой тип связи может быть исследован с помощью этого метода.
CFM был первоначально разработан Чарльзом Либером в Гарвардском университете в 1994 году. [1] Метод был продемонстрирован с использованием гидрофобности, где полярные молекулы (например, COOH) имеют тенденцию иметь наиболее сильную связь друг с другом, за ними следует неполярная (например, CH 3 -CH 3 ) связь, а комбинация является самой слабой. Наконечники зондов функционализированы, а субстраты структурированы этими молекулами. Все комбинации функционализации были протестированы, как путем контакта кончика и удаления, так и путем пространственного картирования субстратов структурированы обеими группами и наблюдения за комплементарностью в контрасте изображения. Оба эти метода обсуждаются ниже. Используемый инструмент AFM аналогичен инструменту на рисунке 1.
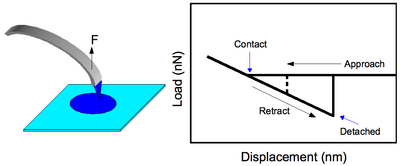
Это более простой режим работы CFM, где функционализированный наконечник приводится в контакт с поверхностью и тянется для наблюдения силы, при которой происходит разделение, (см. Рисунок 2). Теория механики адгезии Джонсона-Кендалла-Робертса (JKR) предсказывает это значение как [1] [2]
(1)
где — радиус наконечника, а — различные поверхностные энергии между наконечником, образцом и средой, в которой каждый находится (жидкости обсуждаются ниже). обычно получают из СЭМ и и из измерений угла контакта на подложках с заданными фрагментами. Когда используются одни и те же функциональные группы, и что приводит к Делая это дважды с двумя различными фрагментами (например, COOH и CH 3 ), получают значения и , оба из которых могут использоваться вместе в одном эксперименте для определения . Следовательно, можно рассчитать для любой комбинации функциональностей для сравнения со значениями, определенными CFM.
Для аналогично функционализированного кончика и поверхности при отрыве кончика теория JKR также предсказывает радиус контакта [2]
(2)
с «эффективным» модулем Юнга кончика, полученным из фактического значения и коэффициента Пуассона . Если известна эффективная площадь одной функциональной группы, (например, из моделирования квантовой химии), общее количество лигандов, участвующих в растяжении, можно оценить как Как было сказано ранее, силовое разрешение CFM позволяет исследовать отдельные связи даже самого слабого сорта, но кривизна кончика обычно препятствует этому. Используя уравнение 2, радиус кривизны < 10 нм был определен как требование для проведения испытания на растяжение отдельных линейных фрагментов. [2]
Краткое замечание: работа, соответствующая гистерезису в профиле силы (рисунок 2), не коррелирует с энергией связи. Работа, проделанная при втягивании кончика, аппроксимируется из-за линейного поведения деформации, где — сила, а — смещение непосредственно перед высвобождением. Используя результаты Фрисби и др. [1], нормализованные к предполагаемым 50 функциональным группам в контакте, значения работы оцениваются как 39 эВ, 0,25 эВ и 4,3 эВ для взаимодействий COOH/COOH , COOH/CH 3 и CH 3 /CH 3 соответственно. Грубо говоря, энергии межмолекулярных связей можно рассчитать следующим образом: — точка кипения. Согласно этому, = 32,5 мэВ для муравьиной кислоты , HCOOH , и 9,73 мэВ для метана , CH4 , каждое значение примерно на 3 порядка меньше, чем может предполагать эксперимент. Даже если бы рассматривалась пассивация поверхности с помощью EtOH (обсуждается ниже), большая ошибка кажется неустранимой. Самые сильные водородные связи имеют энергию не более ~1 эВ. [ 3] Это настоятельно подразумевает, что кантилевер имеет силовую постоянную, меньшую или порядка постоянной для взаимодействий связей, и, следовательно, его нельзя рассматривать как идеально жесткий. Это открывает путь для повышения полезности CFM, если можно будет использовать более жесткие кантилеверы, сохраняя при этом разрешение по силе.
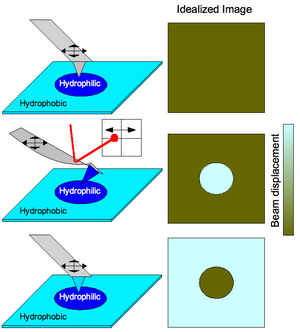
Химические взаимодействия также могут использоваться для картирования предварительно шаблонизированных субстратов с различными функциональными возможностями (см. Рисунок 3). Сканирование поверхности с различной гидрофобностью с помощью зонда, не имеющего прикрепленных функциональных групп, даст изображение без контраста, поскольку поверхность морфологически не имеет особенностей (простая операция АСМ). Функционализация зонда как гидрофильного приведет к изгибу кантилевера, когда зонд сканирует гидрофильные участки субстрата из-за сильных взаимодействий зонд-субстрат. Это обнаруживается с помощью отклонения лазера в позиционно-чувствительном детекторе , тем самым создавая изображение химического профиля поверхности. Как правило, более яркая область будет соответствовать большей амплитуде отклонения, поэтому более сильная связь соответствует более светлым областям карты изображения CFM. Когда функционализация кантилевера переключается таким образом, что зонд изгибается при столкновении с гидрофобными областями субстрата, наблюдается дополнительное изображение.
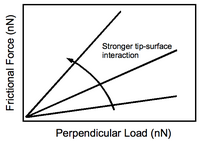
Реакция силы трения на величину перпендикулярной нагрузки, приложенной наконечником к подложке, показана на рисунке 4. Увеличение взаимодействия наконечника с подложкой приводит к более крутому наклону, как и следовало ожидать. Экспериментальное значение имеет тот факт, что контраст между различными функциями на поверхности может быть усилен приложением большей перпендикулярной силы. Конечно, это происходит за счет потенциального повреждения подложки.
Капиллярная сила является основной проблемой при измерениях силы растяжения, поскольку она эффективно усиливает взаимодействие наконечника с поверхностью. Обычно она вызвана адсорбированной влагой на подложках из окружающей среды. Чтобы устранить эту дополнительную силу, можно проводить измерения в жидкостях. С наконечником с X-терминатором и подложкой в жидкости L, добавление к F ad рассчитывается с использованием уравнения 1 с W XLX = 2γ LL ; то есть дополнительная сила возникает из-за притяжения молекул жидкости друг к другу. Это составляет ~10 пН для EtOH, что все еще позволяет наблюдать даже самые слабые полярные/неполярные взаимодействия (~20 пН). [2] Выбор жидкости зависит от того, какие взаимодействия представляют интерес. Когда растворитель не смешивается с функциональными группами, существует более сильная, чем обычно, связь наконечника с поверхностью. Поэтому органические растворители подходят для изучения ван-дер-ваальсовых и водородных связей, в то время как электролиты лучше всего подходят для исследования гидрофобных и электростатических сил.

Биологическая реализация CFM на наноуровне представляет собой разворачивание белков с функционализированным кончиком и поверхностью (см. Рисунок 5). [4] Благодаря увеличенной площади контакта кончик и поверхность действуют как якоря, удерживающие пучки белков при их разделении. По мере того, как происходит разворачивание, требуемая сила скачет, указывая на различные стадии разворачивания: (1) разделение на пучки, (2) разделение пучка на домены кристаллического белка, удерживаемые вместе силами Ван-дер-Ваальса, и (3) линеаризация белка при преодолении вторичной связи. Этот метод предоставляет информацию о внутренней структуре этих сложных белков, а также лучшее понимание взаимодействий компонентов.
Второе соображение заключается в использовании уникальных свойств наноматериалов. Высокое соотношение сторон углеродных нанотрубок (легко >1000) используется для отображения поверхностей с глубокими особенностями. [5] Использование углеродного материала расширяет химию функционализации, поскольку существует бесчисленное множество путей химической модификации боковых стенок нанотрубок (например, с помощью диазония, простых алкилов, водорода, озона/кислорода и аминов). Многослойные нанотрубки обычно используются из-за их жесткости. Благодаря их приблизительно плоским концам можно оценить количество функциональных групп, которые находятся в контакте с подложкой, зная диаметр трубки и количество стенок, что помогает в определении свойств растяжения отдельных фрагментов. Конечно, этот метод имеет очевидные последствия и в трибологии .