Закон Гей-Люссака обычно относится к закону Жозефа-Луи Гей-Люссака объединения объемов газов , открытом в 1808 году и опубликованному в 1809 году. [1] Однако иногда он относится к пропорциональности объема газа его абсолютному значению . температура при постоянном давлении . Последний закон был опубликован Гей-Люссаком в 1802 году, [2] но в статье, в которой он описывал свою работу, он цитировал ранее неопубликованную работу 1780-х годов Жака Шарля . Следовательно, пропорциональность объема и температуры обычно известна как закон Чарльза .
Закон объединения объемов гласит, что когда газы химически реагируют друг с другом, они делают это в объемных количествах, которые имеют небольшие целочисленные соотношения (объемы, рассчитанные при одинаковых температуре и давлении).
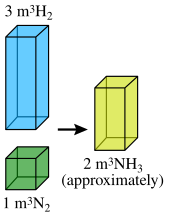
Соотношение объемов газов-реагентов и газообразных продуктов можно выразить простыми целыми числами .
Например, Гей-Люссак обнаружил, что два объема водорода реагируют с одним объемом кислорода с образованием двух объемов газообразной воды. Говоря конкретно, 100 мл водорода соединяются с 50 мл кислорода, образуя 100 мл водяного пара: Водород (100 мл) + Кислород (50 мл) = Вода (100 мл). Таким образом, объемы водорода и кислорода, которые объединяются (т.е. 100 мл и 50 мл), имеют простое соотношение 2:1, как и в случае соотношения водяного пара продукта и реагирующего кислорода.
На основе результатов Гей-Люссака Амедео Авогадро в 1811 году выдвинул гипотезу, что при одинаковых температуре и давлении равные объемы газов (любого рода) содержат одинаковое количество молекул ( закон Авогадро ). Он указал, что если эта гипотеза верна, то ранее изложенный результат
также может быть выражено как
Закон объединения объемов газов был публично объявлен Жозефом Луи Гей-Люссаком в последний день 1808 года и опубликован в 1809 году. [3] [4] Поскольку не было прямых доказательств молекулярной теории Авогадро, очень немногие химики приняли закон Авогадро. Гипотеза считалась общедействительной до тех пор, пока итальянский химик Станислао Канниццаро не аргументировал ее убедительно во время Первого Международного химического конгресса в 1860 году. [5]
В 17 веке Гийом Амонтон обнаружил закономерную зависимость между давлением и температурой газа при постоянном объеме. В некоторых вводных учебниках физики зависимость давления от температуры до сих пор определяется как закон Гей-Люссака. [6] [7] [8] Гей-Люссак в первую очередь исследовал взаимосвязь между объемом и температурой и опубликовал ее в 1802 году, но его работа все же охватывала некоторое сравнение давления и температуры. [9] Учитывая относительную технологию, доступную обоим мужчинам, Амонтон мог работать только с воздухом в качестве газа, тогда как Гей-Люссак мог экспериментировать с несколькими типами обычных газов, таких как кислород, азот и водород. [10]
Что касается зависимости объема от температуры, Гей-Люссак приписал свои открытия Жаку Шарлю , потому что он использовал большую часть неопубликованных данных Шарля 1787 года - следовательно, закон стал известен как закон Шарля или Закон Шарля и Гей-Люссака. [11]
Законы Амонтона, Чарльза и Бойля образуют объединенный газовый закон . Эти три газовых закона в сочетании с законом Авогадро могут быть обобщены законом идеального газа .
Гей-Люссак использовал формулу, полученную из ΔV/V = αΔT, чтобы определить скорость расширения α газов. Для воздуха он нашел относительное расширение ΔV/V = 37,50% и получил значение α = 37,50%/100 °C = 1/266,66 °C, что указывало на то, что значение абсолютного нуля было примерно на 266,66 °C ниже 0 °C. . [12] Величина скорости расширения α примерно одинакова для всех газов, и это также иногда называют законом Гей-Люссака. См. введение к этой статье и Закон Чарльза .