В химии соединениями благородных газов называют химические соединения , в состав которых входит элемент из благородных газов 18- й группы таблицы Менделеева . Хотя благородные газы, как правило, являются нереакционноспособными элементами, наблюдалось множество таких соединений, особенно с участием элемента ксенона .
С точки зрения химии благородные газы можно разделить на две группы: [ нужна ссылка ] относительно реактивный криптон ( энергия ионизации 14,0 эВ ), ксенон (12,1 эВ) и радон (10,7 эВ) с одной стороны, и самые нереакционноспособный аргон (15,8 эВ), неон (21,6 эВ) и гелий (24,6 эВ) с другой. В соответствии с этой классификацией Kr, Xe и Rn образуют соединения, которые можно изолировать в массе при стандартной температуре и давлении или около них , тогда как He, Ne, Ar, как было замечено, образуют настоящие химические связи с помощью спектроскопических методов, но только при замораживании в матрица благородного газа при температуре 40 К (-233 ° C; -388 ° F) или ниже, в сверхзвуковых струях благородного газа или под чрезвычайно высоким давлением с металлами.
Более тяжелые благородные газы имеют больше электронных оболочек , чем более легкие. Следовательно, самые внешние электроны подвергаются экранирующему эффекту со стороны внутренних электронов, что делает их более легко ионизируемыми , поскольку они менее сильно притягиваются к положительно заряженному ядру . Это приводит к достаточно низкой энергии ионизации для образования стабильных соединений с наиболее электроотрицательными элементами , фтором и кислородом , и даже с менее электроотрицательными элементами, такими как азот и углерод, при определенных обстоятельствах. [1] [2]
Когда в конце девятнадцатого века впервые было идентифицировано семейство благородных газов, ни один из них не наблюдал образования каких-либо соединений, поэтому первоначально считалось, что все они представляют собой инертные газы (как их тогда называли), которые не могут образовывать соединения. . С развитием теории атома в начале двадцатого века их инертность стала приписываться полной валентной электронной оболочке , которая делает их очень химически стабильными и нереакционноспособными. Все благородные газы имеют полные внешние электронные оболочки s и p (за исключением гелия , у которого нет подуровня p ), и поэтому с трудом образуют химические соединения . Их высокая энергия ионизации и почти нулевое сродство к электрону объясняют их нереакционную способность.
В 1933 году Лайнус Полинг предсказал, что более тяжелые благородные газы смогут образовывать соединения с фтором и кислородом . В частности, он предсказал существование гексафторида криптона ( Kr F 6 ) и гексафторида ксенона ( Xe F 6 ), предположил, что XeF 8 может существовать как нестабильное соединение, и предположил, что ксеновая кислота будет образовывать перксенатные соли. [3] [4] Эти предсказания оказались весьма точными, хотя последующие предсказания для XeF 8 показали, что он будет не только термодинамически нестабильным, но и кинетически нестабильным . [5] По состоянию на 2022 год XeF 8 не производился, хотя анион октафтороксената(VI) ( [XeF 8 ] 2- ) наблюдался.
К 1960 году еще не было синтезировано ни одного соединения с ковалентно связанным атомом благородного газа. [6] Первый опубликованный отчет о соединении благородного газа в июне 1962 года был сделан Нилом Бартлеттом , который заметил, что высокоокисляющее соединение гексафторид платины ионизирует O 2 до O.+2. Поскольку энергия ионизации O 2 в O+2(1165 кДж моль -1 ) почти равна энергии ионизации Xe в Xe + (1170 кДж моль -1 ), он попробовал реакцию Xe с PtF 6 . В результате был получен кристаллический продукт — гексафторплатинат ксенона , формула которого была предложена как Xe + [PtF 6 ] − . [4] [7] Позже было показано, что соединение на самом деле более сложное и содержит как [XeF] + [PtF 5 ] -, так и [XeF] + [Pt 2 F 11 ] - . [8] Тем не менее, это было первое настоящее соединение благородного газа.
О первых бинарных соединениях благородных газов сообщалось позже, в 1962 году. Бартлетт синтезировал тетрафторид ксенона ( XeF 4 ), подвергая смесь ксенона и фтора воздействию высокой температуры. [9] Рудольф Хоппе , среди других групп, синтезировал дифторид ксенона ( XeF 2 ) путем реакции элементов. [10]
После первого успешного синтеза соединений ксенона в 1963 году сообщалось о синтезе дифторида криптона ( KrF 2 ). [11]
В этом разделе нерадиоактивные благородные газы рассматриваются в порядке убывания атомного веса , что в целом отражает приоритет их открытия и широту доступной информации об этих соединениях. Радиоактивные элементы радон и оганессон более сложны для изучения и рассматриваются в конце раздела.
После первоначальных исследований XeF 4 и XeF 2 в 1962 году были синтезированы соединения ксенона, включая другие фториды ( XeF 6 ), оксифториды ( XeOF 2 , XeOF 4 , XeO 2 F 2 , XeO 3 F 2 , XeO 2 F 4 ) и оксиды ( XeO 2 , XeO 3 и XeO 4 ). Фториды ксенона реагируют с несколькими другими фторидами с образованием фтороксенатов, таких как октафтороксенат(VI) натрия ( (Na + ) 2 [XeF 8 ] 2- ), [ нужна ссылка ] и соли фтороксенония, такие как гексафторантимонат трифтороксенония ( [XeF 3 ] + [SbF 6 ] − ). [12]
Что касается реакционной способности других галогенидов, короткоживущие эксимеры галогенидов благородных газов , таких как XeCl 2 или XeCl, получают in situ и используют в качестве эксимерных лазеров . [13]
Недавно [ когда? ] ксенон, как было показано, образует широкий спектр соединений типа XeO n X 2 , где n равно 1, 2 или 3, а X представляет собой любую электроотрицательную группу, такую как CF 3 , C(SO 2 CF 3 ) 3 , N( SO 2 F) 2 , N(SO 2 CF 3 ) 2 , OTeF 5 , O(IO 2 F 2 ) и т.д.; диапазон соединений впечатляет, он аналогичен тому, который наблюдается с соседним элементом йодом , исчисляется тысячами и включает связи между ксеноном и кислородом, азотом, углеродом, бором и даже золотом, а также перксеновой кислотой, несколькими галогенидами и сложными ионами. . [ нужна цитата ]
Соединение [Xe 2 ] + [Sb 4 F 21 ] − содержит связь Xe–Xe, которая является самой длинной из известных связей элемент-элемент (308,71 пм = 3,0871 Å ). [14] Сообщается, что короткоживущие эксимеры Xe 2 существуют как часть функции эксимерных лазеров . [ нужна цитата ]
Газ криптон реагирует с газообразным фтором в экстремальных условиях воздействия, образуя KrF 2 согласно следующему уравнению:
KrF 2 реагирует с сильными кислотами Льюиса с образованием солей катионов [KrF] + и [Kr 2 F 3 ] + . [11] Получение KrF 4 , о котором сообщил Гроссе в 1963 году, с использованием метода Клаасена, впоследствии оказалось ошибочной идентификацией. [15]
Также описаны соединения криптона со связями, отличными от Kr-F (соединения с атомами, отличными от фтора ). KrF 2 реагирует с B(OTeF 5 ) 3 с образованием нестабильного соединения Kr(OTeF 5 ) 2 со связью криптон- кислород . Связь криптон- азот обнаружена в катионе [H-C≡N-Kr-F] + , образующемся при реакции KrF 2 с [H-C≡N-H] + [AsF 6 ] − ниже −50°. С. [16]
Об открытии HArF было объявлено в 2000 году. [17] [18] Соединение может существовать в низкотемпературных аргоновых матрицах для экспериментальных исследований, а также изучалось вычислительно . [18] Ион гидрида аргона [ArH] + был получен в 1970-х годах. [19] Этот молекулярный ион также был идентифицирован в Крабовидной туманности на основании частоты его светового излучения. [20]
Существует возможность получения твердой соли [ArF] + с анионами [SbF6 ] - или [AuF6]-. [21] [22]
Ионы Ne + , [NeAr] + , [NeH] + и [HeNe] + известны из оптических и масс-спектрометрических исследований. Неон также образует нестабильный гидрат. [23] Существуют некоторые эмпирические и теоретические доказательства существования нескольких метастабильных соединений гелия , которые могут существовать при очень низких температурах или экстремальных давлениях. О стабильном катионе [HeH] + сообщалось в 1925 г. [24] , но он не считался настоящим соединением, поскольку он не является нейтральным и не может быть выделен. В 2016 году ученые создали соединение гелия динатрийгелид ( Na 2 He ), которое стало первым открытым соединением гелия. [25]
Радон не химически инертен, но его короткий период полураспада (3,8 дня для 222 Rn) и высокая энергия его радиоактивности затрудняют исследование его единственного фторида ( RnF 2 ), его известного оксида ( RnO 3 ) и их реакции. продукты. [26]
Все известные изотопы оганессона имеют еще более короткий период полураспада в миллисекундном диапазоне, и соединения пока не известны, [27], хотя некоторые из них были предсказаны теоретически. Ожидается, что он будет даже более реактивным, чем радон, и по своему химическому составу больше похож на обычный элемент, чем на благородный газ. [28]

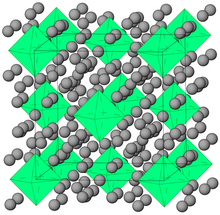
До 1962 г. единственными изолированными соединениями благородных газов были клатраты (в том числе клатратные гидраты ); другие соединения, такие как координационные соединения, наблюдались только спектроскопическими методами. [4] Клатраты (также известные как клеточные соединения) представляют собой соединения благородных газов, в которых они задерживаются в полостях кристаллических решеток некоторых органических и неорганических веществ. Ar, Kr, Xe и Ne [30] могут образовывать клатраты с кристаллическим гидрохиноном . Кр и Хе могут выступать в качестве гостей в кристаллах меланофлогита . [31]
Кристаллы гелия-азота ( He(N 2 ) 11 ) были выращены при комнатной температуре и давлениях ок. 10 ГПа в ячейке с алмазной наковальней . [32] Твердый аргон-водородный клатрат ( Ar(H 2 ) 2 ) имеет ту же кристаллическую структуру, что и фаза Лавеса MgZn 2 . Он образуется при давлениях от 4,3 до 220 ГПа, хотя измерения комбинационного рассеяния света показывают, что молекулы H 2 в Ar(H 2 ) 2 диссоциируют при давлении выше 175 ГПа. Аналогичное твердое вещество Kr(H 2 ) 4 образуется при давлениях выше 5 ГПа. Он имеет гранецентрированную кубическую структуру, в которой криптоновые октаэдры окружены случайно ориентированными молекулами водорода. Между тем, в твердом состоянии Xe(H 2 ) 8 атомы ксенона образуют димеры внутри твердого водорода . [29]
Предполагалось , что координационные соединения, такие как Ar·BF 3, существуют при низких температурах, но это никогда не было подтверждено. [ нужна цитация ] Также сообщалось, что такие соединения, как WHe 2 и HgHe 2, образовались в результате электронной бомбардировки, но недавние исследования показали, что они, вероятно, являются результатом адсорбции He на поверхности металла; следовательно, эти соединения нельзя по-настоящему считать химическими соединениями. [ нужна цитата ]
Гидраты образуются при сжатии благородных газов в воде, при этом считается, что молекула воды, сильный диполь, индуцирует слабый диполь в атомах благородного газа, что приводит к диполь-дипольному взаимодействию. Более тяжелые атомы подвергаются большему влиянию, чем более мелкие, поэтому сообщалось, что Xe·5,75H 2 O был наиболее стабильным гидратом; [33] его температура плавления составляет 24 °C. [34] Также была произведена дейтерированная версия этого гидрата. [35]
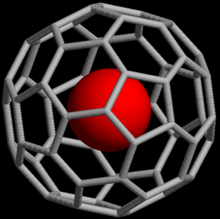
Благородные газы также могут образовывать эндоэдральные соединения фуллеренов, в которых атом благородного газа захвачен внутри молекулы фуллерена . В 1993 году было обнаружено, что когда C 60 подвергается воздействию He или Ne под давлением около 3 бар , образуются комплексы He@C 60 и Ne@C 60 . [36] В этих условиях только примерно одна из каждых 650 000 клеток C 60 была легирована атомом гелия ; при более высоких давлениях (3000 бар) можно достичь выхода до 0,1%. Также получены эндоэдральные комплексы с аргоном , криптоном и ксеноном , а также многочисленные аддукты He @C 60 . [37]
В большинстве случаев соединения благородных газов используются либо в качестве окислителей, либо в качестве средства хранения благородных газов в плотной форме. Ксеновая кислота является ценным окислителем, поскольку она не способна вносить примеси — ксенон просто высвобождается в виде газа — и поэтому в этом отношении с ней может конкурировать только озон . [4] Перксенаты являются еще более мощными окислителями. [ нужна цитация ] Окислители на основе ксенона также использовались для синтеза карбокатионов, стабильных при комнатной температуре, в растворе SO 2 ClF . [38] [ нужен неосновной источник ]
Стабильные соли ксенона, содержащие очень высокие весовые доли фтора (такие как гептафтороксенат тетрафтораммония(VI), [NF 4 ][XeF 7 ] и родственный октафтороксенат тетрафтораммония(VI) [NF 4 ] 2 [XeF 8 ] ), имеют были разработаны как высокоэнергетические окислители для использования в качестве топлива в ракетной технике. [39] [ необходим неосновной источник ] [40]
Фториды ксенона являются хорошими фторирующими агентами. [41]
Клатраты использовались для отделения He и Ne от Ar, Kr и Xe, а также для транспортировки Ar, Kr и Xe. [ нужна ссылка ] (Например, радиоактивные изотопы криптона и ксенона трудно хранить и утилизировать, а с соединениями этих элементов легче обращаться, чем с газообразными формами. [4] ) Кроме того, клатраты радиоизотопов могут обеспечить подходящие составы. для экспериментов, требующих источников определенных видов излучений; следовательно. Клатрат 85 Kr обеспечивает безопасный источник бета-частиц , а клатрат 133 Xe является полезным источником гамма-лучей . [42]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ){{cite book}}: |journal=игнорируется ( помощь )