S -Аденозилметионин ( SAM ), также известный под коммерческими названиями SAMe , SAM-e или AdoMet , является распространенным косубстратом, участвующим в переносе метильных групп , транссульфурировании и аминопропилировании. Хотя эти анаболические реакции происходят по всему организму, большая часть SAM вырабатывается и потребляется в печени. [1] Известно более 40 переносов метила от SAM к различным субстратам, таким как нуклеиновые кислоты , белки , липиды и вторичные метаболиты . Он производится из аденозинтрифосфата (АТФ) и метионина под действием метионин-аденозилтрансферазы . ЗРК был впервые обнаружен Джулио Кантони в 1952 году. [1]
У бактерий SAM связан с рибопереключателем SAM , который регулирует гены , участвующие в биосинтезе метионина или цистеина . В эукариотических клетках SAM служит регулятором множества процессов, включая метилирование ДНК , тРНК и рРНК ; иммунная реакция ; [2] метаболизм аминокислот; транссульфурация ; и более. У растений SAM имеет решающее значение для биосинтеза этилена , важного растительного гормона и сигнальной молекулы. [3]
S -Аденозилметионин состоит из аденозильного катиона, присоединенного к сере метионина. Он синтезируется из АТФ и метионина ферментом S -аденозилметионинсинтетазой по следующей реакции:
Сульфониевая функциональная группа, присутствующая в S -аденозилметионине , является центром его своеобразной реакционной способности. В зависимости от фермента S -аденозилметионин может превращаться в один из трех продуктов:
Реакции, которые производят, потребляют и регенерируют SAM, называются циклом SAM. На первом этапе этого цикла SAM-зависимые метилазы (EC 2.1.1), использующие SAM в качестве субстрата, производят в качестве продукта S -аденозилгомоцистеин. [4] S -аденозилгомоцистеин является сильным негативным регулятором почти всех SAM-зависимых метилаз, несмотря на их биологическое разнообразие. Он гидролизуется до гомоцистеина и аденозина S - аденозилгомоцистеингидролазой EC 3.3.1.1, а гомоцистеин рециркулируется обратно в метионин посредством переноса метильной группы от 5-метилтетрагидрофолата одним из двух классов метионинсинтаз (т.е. кобаламин -зависимых (EC) 2.1.1.13) или кобаламин-независимый (EC 2.1.1.14)). Этот метионин затем может быть преобразован обратно в SAM, завершая цикл. [5] На лимитирующей стадии цикла SAM MTHFR (метилентетрагидрофолатредуктаза) необратимо восстанавливает 5,10-метилентетрагидрофолат до 5-метилтетрагидрофолата. [6]
Большое количество ферментов восстановительно расщепляет SAM с образованием радикалов: 5'-дезоксиаденозил-5'-радикала , метилового радикала и других. Эти ферменты называются радикальными SAM . Все они имеют в своих активных центрах железо-серный кластер . [7] Большинство ферментов с такой способностью имеют общую область гомологии последовательности, которая включает мотив CxxxCxxC или близкий вариант. Эта последовательность обеспечивает три цистеинилтиолатных лиганда, которые связываются с тремя из четырех металлов в кластере 4Fe-4S. Четвертый Fe связывает SAM.
Радикальные промежуточные продукты, генерируемые этими ферментами, выполняют множество необычных химических реакций. Примеры радикальных SAM-ферментов включают лиазу фотопродукта спор , активазы пируватформиат-лиазы и анаэробных сульфатаз, лизин-2,3-аминомутазу и различные ферменты биосинтеза кофакторов, модификации пептидов, образования металлопротеиновых кластеров, модификации тРНК , липидного обмена и т. д. Некоторые радикальные ферменты Ферменты SAM используют второй SAM в качестве донора метила. Радикальные ферменты SAM гораздо более распространены у анаэробных бактерий, чем у аэробных организмов. Их можно найти во всех сферах жизни, и они практически не изучены. Недавнее биоинформатическое исследование пришло к выводу, что это семейство ферментов включает по меньшей мере 114 000 последовательностей, включая 65 уникальных реакций. [8]
Дефицит радикальных ферментов SAM связан с различными заболеваниями, включая врожденные пороки сердца , боковой амиотрофический склероз и повышенную восприимчивость к вирусам. [8]
Другая важная роль SAM заключается в биосинтезе полиаминов . Здесь SAM декарбоксилируется аденозилметиониндекарбоксилазой ( EC 4.1.1.50) с образованием S -аденозилметионинамина . Это соединение затем жертвует свою н -пропиламиновую группу при биосинтезе полиаминов, таких как спермидин и спермин, из путресцина . [9]
SAM необходим для роста и восстановления клеток. Он также участвует в биосинтезе некоторых гормонов и нейротрансмиттеров, влияющих на настроение, таких как адреналин . Метилтрансферазы также ответственны за добавление метильных групп к 2'-гидроксилам первого и второго нуклеотидов рядом с 5'-кэпом в информационной РНК . [10] [11]
По состоянию на 2012 год данные о том, может ли SAM облегчить боль при остеоартрите, были неубедительными ; Проведенные клинические испытания были слишком малы, чтобы можно было делать обобщения. [12]
Цикл SAM тесно связан с печенью с 1947 года, поскольку у людей с алкогольным циррозом печени в крови накапливается большое количество метионина. [13] Хотя многочисленные данные лабораторных испытаний на клетках и моделях животных позволяют предположить, что SAM может быть полезен для лечения различных заболеваний печени , по состоянию на 2012 год SAM не изучался ни в каких крупных рандомизированных плацебо-контролируемых клинических исследованиях, которые позволили бы провести оценку. его эффективности и безопасности. [14] [15]
Кокрейновский обзор 2016 года пришел к выводу, что в отношении большого депрессивного расстройства «учитывая отсутствие доказательств высокого качества и невозможность сделать твердые выводы на основе этих данных, следует продолжить изучение использования SAMe для лечения депрессии у взрослых». [16]
Систематический обзор 2020 года показал, что он действует значительно лучше, чем плацебо, и дает такие же результаты, как и другие широко используемые антидепрессанты (имипрамин и эсциталопрам). [17]
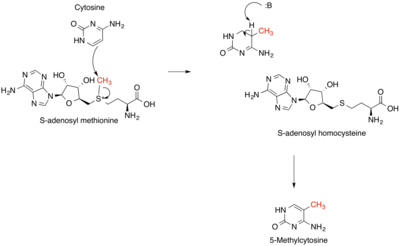
Недавно было показано, что SAM играет роль в эпигенетической регуляции. Метилирование ДНК является ключевым регулятором эпигенетической модификации во время развития и дифференцировки клеток млекопитающих. В моделях на мышах избыточные уровни SAM были вовлечены в ошибочные паттерны метилирования, связанные с диабетической нейропатией. SAM служит донором метила при метилировании цитозина, которое является ключевым процессом эпигенетической регуляции. [18] Из-за такого влияния на эпигенетическую регуляцию SAM был протестирован в качестве противоракового средства. При многих видах рака пролиферация зависит от низкого уровня метилирования ДНК. Было показано, что добавление in vitro при таких видах рака реметилирует последовательности промотора онкогена и снижает выработку протоонкогенов. [19] При других видах рака, таких как колоректальный рак, аберрантное глобальное гиперметилирование может ингибировать промоторные области генов, подавляющих опухоль.
При пероральном приеме САМ достигает пиковых концентраций в плазме через три-пять часов после приема таблетки с энтеросолюбильным покрытием (400–1000 мг). Период полувыведения составляет около 100 минут. [20]
В Канаде, Великобритании [21] и США SAM продается в виде пищевой добавки под торговым названием SAM-e (также пишется SAME или SAMe, произносится как «Сэмми»). [22] Он был представлен в США в 1999 году, после того как в 1994 году был принят Закон о пищевых добавках, здравоохранении и образовании. [23]
Он был представлен как рецептурный препарат в Италии в 1979 году, в Испании в 1985 году и в Германии в 1989 году . [23] По состоянию на 2012 год он продавался как рецептурный препарат в России, Индии, Китае, Италии, Германии, Вьетнаме, и Мексика. [15]
При употреблении SAM могут возникнуть желудочно-кишечные расстройства, диспепсия и беспокойство . [20] Долгосрочные последствия неизвестны. SAM является слабым ДНК- алкилирующим агентом. [24]
Другим зарегистрированным побочным эффектом SAM является бессонница ; поэтому добавку часто принимают утром. Другие сообщения о легких побочных эффектах включают отсутствие аппетита, запор, тошноту, сухость во рту, потливость и беспокойство/нервозность, но в плацебо-контролируемых исследованиях эти побочные эффекты возникают примерно с такой же частотой в группах плацебо. [ нужна медицинская ссылка ]
Прием SAM одновременно с некоторыми лекарствами может увеличить риск серотонинового синдрома — потенциально опасного состояния, вызванного избытком серотонина. Эти препараты включают декстрометорфан (Робитуссин), меперидин (Демерол), пентазоцин (Талвин) и трамадол (Ультрам). [25]
SAM также может взаимодействовать с антидепрессантами, включая триптофан и зверобой продырявленный (зверобой продырявленный), увеличивая вероятность серотонинового синдрома или других побочных эффектов, а также может снижать эффективность леводопы при болезни Паркинсона. [26]
Людям с биполярным расстройством не следует использовать SAM, поскольку это увеличивает риск маниакальных эпизодов. [26]
Исследование 2022 года пришло к выводу, что SAMe может быть токсичным. Жан-Мишель Фустин из Манчестерского университета сообщил, что исследователи обнаружили, что избыток SAMe распадается в организме на аденин и метилтиоаденозин , что приводит к парадоксальному эффекту ингибирования метилирования. Это было обнаружено у лабораторных мышей , наносящее вред здоровью, и при испытаниях in vitro на клетках человека. [27] [21]