
Ион карбения — это положительный ион со структурой RR’R″C + , то есть химическая разновидность с атомом углерода, имеющим три ковалентные связи, и несет формальный заряд +1 . Но ИЮПАК путает координационное число с валентностью , ошибочно считая углерод в карбении трехвалентным. [1]
В старой литературе для этого класса использовалось название «ион карбония» , но теперь оно относится исключительно к другому семейству карбокатионов , ионам карбония , где заряженный углерод ошибочно считается ИЮПАК пятивалентным , [1] но он является пятикоординированным, а не пятивалентным. , потому что координационное число и валентность — это две разные вещи. Современные определения были предложены химиком Джорджем Эндрю Олахом в 1972 году [2] и в настоящее время получили широкое признание.
Ионы карбения обычно обладают высокой реакционной способностью из-за наличия неполного октета электронов; однако некоторые ионы карбения, такие как ион тропилия , относительно стабильны из-за делокализации положительного заряда между атомами углерода.
Ионы карбения классифицируются как первичные , вторичные или третичные в зависимости от того, равно ли число атомов углерода, связанных с ионизированным углеродом, 1, 2 или 3. (Ионы с нулевым содержанием углерода, присоединенные к ионизированному углероду, такие как метений , CH+
3, обычно включаются в основной класс).
Стабильность обычно увеличивается с увеличением количества алкильных групп, связанных с несущим заряд углеродом. Третичные карбокатионы более стабильны (и образуются легче), чем вторичные карбокатионы, поскольку они стабилизируются за счет гиперконъюгации . Первичные карбокатионы крайне нестабильны. Следовательно, такие реакции, как реакция S N 1 и реакция элиминирования E1, обычно не происходят, если образуется первичный карбений.
Однако углерод, связанный двойной связью с ионизированным углеродом, может стабилизировать ион за счет резонанса . Такие катионы, как аллильный катион CH
2=СН-СН+
2и бензильный катион C
6ЧАС
5−CH+
2, более стабильны, чем большинство других карбокатионов. Особенно реакционноспособны молекулы, которые могут образовывать аллил- или бензилкарбении. Ионы карбения также могут быть стабилизированы гетероатомами . [3]
Ионы карбения могут подвергаться реакциям перегруппировки из менее стабильных структур в столь же стабильные или более стабильные с константами скорости , превышающими 10 9 с -1 . Этот факт усложняет пути синтеза многих соединений. Например, при нагревании пентан-3-ола с водной HCl первоначально образовавшийся 3-пентилкарбокатион перегруппировывается в статистическую смесь 3-пентила и 2-пентила. Эти катионы реагируют с хлорид-ионом с образованием 3-хлорпентана и 2-хлорпентана в соотношении примерно 1:2.
Ионы карбения можно получить непосредственно из алканов путем удаления гидрид- аниона H.−
, с сильной кислотой. Например, волшебная кислота , смесь пентафторида сурьмы ( SbF
5) и фторсерная кислота ( ФСО
3H ), превращает изобутан в катион триметилкарбения (CH
3)
3С+
. [4]
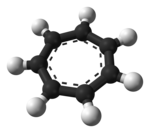
Ион тропилия представляет собой ароматическую разновидность с формулой C.
7ЧАС+
7. [5] Его название происходит от молекулы тропина (сама названа в честь молекулы атропина ). Соли катиона тропилия могут быть стабильными, например тетрафторборат тропилия . Его можно получить из циклогептатриена (тропилидена) и пентахлорида брома или фосфора . [6]
Это планарный циклический семиугольный ион; у него также есть 6 π-электронов (4 n + 2, где n = 1), что соответствует правилу ароматичности Хюккеля . Он может координировать свои действия с атомами металлов как лиганд .
Показанная структура представляет собой совокупность семи резонансных вкладчиков , в которых каждый углерод несет часть положительного заряда.
В 1891 Г. Мерлинг получил водорастворимую соль реакцией циклогептатриена и брома. [7] Структура была объяснена Эггерсом Дерингом и Ноксом в 1954 году. [8] [9]
Другим ионом ароматического карбения является ион циклопропенила или циклопропения , C
3ЧАС+
3, полученный Рональдом Бреслоу и Джоном Т. Гроувсом в 1970 году. [10] Хотя этот ион карбения менее стабилен, чем катион тропилия, он также может образовывать соли при комнатной температуре. Бреслоу и Гровс обнаружили, что растворы таких солей имеют спектроскопические и химические свойства, соответствующие ожиданиям для ароматического иона карбения.
Катион трифенилкарбения или трифенилметила [C(C
6ЧАС
5)
3]+
, особенно стабилен, поскольку положительный заряд может быть распределен между 10 атомами углерода (3 атома углерода в орто- и пара -положениях каждой из трех фенильных групп плюс центральный атом углерода). Он существует в соединениях трифенилметилгексафторфосфата [C(C
6ЧАС
5)
3]+
[ПФ
6]−
, трифенилметилтетрафторборат [C(C
6ЧАС
5)
3]+
[БФ
4]−
и трифенилметилперхлорат [C(C
6ЧАС
5)
3]+
[ClO
4]−
. [11] Его производные включают триарилметановые красители .

Ион арения представляет собой циклогексадиенильный катион, который появляется как реакционноспособный промежуточный продукт при электрофильном ароматическом замещении . [12] По историческим причинам этот комплекс также называют промежуточным соединением Уиланда , [13] или σ-комплексом .
Два атома водорода, связанные с одним углеродом, лежат в плоскости, перпендикулярной бензольному кольцу. [14] Ион арения больше не является ароматическим веществом; однако он относительно стабилен из-за делокализации: положительный заряд делокализован по 5 атомам углерода через π-систему , как показано на следующих резонансных структурах :
Другим вкладом в стабильность ионов арения является выигрыш в энергии за счет прочной связи между бензолом и комплексным электрофилом.
Наименьший ион арения — это протонированный бензол , C
6ЧАС+
7. Ион бензола можно выделить как стабильное соединение, когда бензол протонируется карборановой суперкислотой H(CB 11 H(CH 3 ) 5 Br 6 ). [15] Бензениевая соль является кристаллической с термической стабильностью до 150 °C. Длины связей , определенные с помощью рентгеновской кристаллографии, соответствуют структуре циклогексадиенильного катиона.
Ион ацилия представляет собой катион с формулой RCO + . [16] Структура описывается как R−C≡O + или R−.=О. Это синтетический и реакционноспособный эквивалент ацилкарбокатиона, но в реальной структуре кислород и углерод связаны тройной связью. Такие виды являются обычными реакционноспособными промежуточными продуктами, например, при ацилировании Фриделя-Крафтса, а также во многих других органических реакциях , таких как перегруппировка Хаяши . Соли, содержащие ионы ацилия, могут быть получены путем удаления галогенида из ацилгалогенидов :
Расстояние C–O в этих катионах составляет около 1,1 ангстрем , что даже меньше, чем в монооксиде углерода . [17] Катионы ацилия представляют собой характерные фрагменты, наблюдаемые в ЭУ- масс -спектрах кетонов .