
Высоковалентное железо обычно обозначает соединения и промежуточные соединения, в которых железо находится в формальной степени окисления > 3 и имеет число связей > 6 с координационным числом ≤ 6. Этот термин довольно необычен для гептакоординированных соединений железа. [1] Его следует отличать от терминов «гипервалентный» и «гиперкоординатный» , поскольку соединения высоковалентного железа не обязательно нарушают правило 18 электронов и не обязательно имеют координационные числа> 6. Ион феррата (VI) [FeO 4 ] 2- был синтезирована первая структура этого класса. Синтетические соединения, обсуждаемые ниже, в целом содержат сильно окисленное железо, поскольку эти концепции тесно связаны.
Разновидности оксоферрилов обычно предлагаются в качестве промежуточных продуктов в каталитических циклах , особенно в биологических системах, в которых требуется активация O 2 . Двухатомный кислород обладает высоким потенциалом восстановления (Е 0 = 1,23 В), но первым шагом, необходимым для использования этого потенциала, является термодинамически невыгодное одноэлектронное восстановление Е 0 = -0,16 В. Это восстановление происходит в природе путем образования супероксидного комплекса . при котором восстановленный металл окисляется O 2 . Продуктом этой реакции является пероксидный радикал, который более активен в реакции. Широко применимым методом получения высоковалентных форм оксоферрилов является окисление йодзобензолом : [ 2]

Сообщалось о нескольких синтезах разновидностей оксо железа (IV). [3] Эти соединения моделируют биологические комплексы, такие как цитохром P450 , NO-синтаза и изопенициллин-N-синтаза. Двумя такими зарегистрированными соединениями являются тиолат-лигированное оксоирон (IV) и циклам-ацетат оксоирон (IV). Тиолат-лигированное оксоирон (IV) образуется в результате окисления предшественника [Fe II (TMCS)](PF 6 ) (TMCS = 1-меркаптоэтил-4,8,11-триметил-1,4,8,11- тетраза циклотетрадекан) и 3-5 эквивалентов H 2 O 2 при -60 ˚C в метаноле . Соединение железа (IV) имеет темно-синий цвет и демонстрирует интенсивные особенности поглощения при 460, 570, 850 и 1050 нм. Этот вид Fe IV (=O)(TMCS)+ стабилен при -60 ˚C, но сообщается о разложении при повышении температуры. Соединение 2 было идентифицировано методами мессбауэровской спектроскопии , масс-спектрометрии с ионизацией электрораспылением высокого разрешения (ESI-MS), рентгеновской абсорбционной спектроскопии , расширенной тонкой структуры рентгеновского поглощения (EXAFS), ультрафиолетово-видимой спектроскопии (УФ-Вид), преобразования Фурье. инфракрасная спектроскопия (FT-IR), и результаты сравнивались с расчетами теории функционала плотности (DFT). [4]
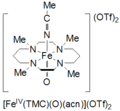
Тетраметилциклам оксоирон(IV) образуется по реакции Fe II (TMC)(OTf) 2 , TMC = 1,4,8,11-тетраметил-1,4,8,11-тетраазациклотетрадекан; OTf = CF 3 SO 3 , с йодозилбензолом (PhIO) в CH 3 CN при -40 ˚C. Сообщается о втором методе образования оксижелеза(IV) циклама как реакции Fe II (TMC)(OTf) 2 с 3 эквивалентами H 2 O 2 в течение 3 часов. Этот вид имеет бледно-зеленый цвет и имеет максимум поглощения при 820 нм. Сообщается, что он стабилен в течение как минимум 1 месяца при температуре -40 ˚C. Он был охарактеризован методами мессбауэровской спектроскопии, ESI-MS, EXAFS, UV-vis, рамановской спектроскопии и FT-IR. [5]
Комплексы биспидина высоковалентного железа способны окислять циклогексан до циклогексанола и циклогексанона с выходом 35% при соотношении спирта к кетону до 4. [6]
Fe V TAML(=O), TAML = тетраамидо макроциклический лиганд , образуется при реакции [Fe III (TAML)(H 2 O)](PPh 4 ) с 2-5 эквивалентами мета-хлорпербензойной кислоты при - 60 ˚C в н-бутиронитриле. Это темно-зеленое соединение (два λ max при 445 и 630 нм соответственно) стабильно при 77 К. Стабилизация Fe(V) объясняется сильной π-донорной способностью депротонированных амидных азотов. [7]
Феррат(VI) – неорганический анион химической формулы [FeO 4 ] 2- . Он светочувствителен и придает своим соединениям и растворам бледно-фиолетовый цвет. Это один из самых сильных известных водоустойчивых окислителей . Хотя феррат (VI) классифицируется как слабое основание , концентрированные растворы феррата (VI) стабильны только при высоком pH .
Дан обзор электронной структуры порфириновых оксожелезосодержащих соединений. [8]

Соединения нитридожелеза [9] и имидожелеза [10] тесно связаны с химией железа и азота . [11] Рассмотрено биологическое значение порфиринов нитридо железа (V). [12] [13] Широко применимым методом получения высоковалентных частиц нитридо железа является термическое или фотохимическое окислительное удаление молекулярного азота из азидного комплекса.
Существует несколько структурно охарактеризованных соединений нитридо железа (IV). [14] [15] [16]
Первое соединение нитридо железа(V) было синтезировано и охарактеризовано Вагнером и Накамото (1988, 1989) с использованием фотолиза и рамановской спектроскопии при низких температурах. [17] [18]
Сообщалось о второй разновидности Fe VI , помимо иона феррата (VI) , [(Me 3 cy-ac)FeN](PF 6 ) 2 . Эта разновидность образуется в результате окисления с последующим фотолизом с образованием разновидности Fe(VI). Характеристика комплекса Fe(VI) выполнена методами мессбауэровского, EXAFS, ИК-расчета и DFT-расчетов. В отличие от иона феррата(VI), соединение 5 диамагнитно . [19]
Соединения фталоцианина дижелеза с мостиковой связью, такие как фталоцианин железа (II), катализируют окисление метана в метанол , формальдегид и муравьиную кислоту с использованием перекиси водорода в качестве жертвенного окислителя. [20] [21]
Виды нитридо железа (IV) и нитридо железа (V) были впервые теоретически исследованы в 2002 году. [22]