В термодинамике изобарный процесс — это тип термодинамического процесса , при котором давление системы остается постоянным: Δ P = 0. Тепло , передаваемое системе, совершает работу , но также изменяет внутреннюю энергию ( U ) системы. В этой статье для обозначения работы используется соглашение о физических знаках, согласно которому положительная работа — это работа, совершаемая системой . Используя это соглашение, согласно первому закону термодинамики ,

где W — работа, U — внутренняя энергия, а Q — тепло. [1] Работа давление- объем в закрытой системе определяется как:
где Δ означает изменение в течение всего процесса, тогда как d обозначает дифференциал. Поскольку давление постоянно, это означает, что
Применяя закон идеального газа , это становится
где R представляет собой газовую постоянную , а n представляет количество вещества , которое, как предполагается, остается постоянным (например, во время химической реакции нет фазового перехода ). Согласно теореме о равнораспределении [2] изменение внутренней энергии связано с температурой системы соотношением
где c V, m – молярная теплоемкость при постоянном объеме .
Подстановка последних двух уравнений в первое уравнение дает:
где c P — молярная теплоемкость при постоянном давлении .
Чтобы найти молярную удельную теплоемкость рассматриваемого газа, следующие уравнения применимы для любого обычного газа, который является калорически совершенным. Свойство γ называется либо показателем адиабаты , либо коэффициентом теплоемкости . В некоторых опубликованных источниках вместо γ может использоваться k .
Молярная изохорная удельная теплоемкость:
Молярная изобарная удельная теплоемкость:
Значения γ : γ = 7/5для двухатомных газов, таких как воздух и его основные компоненты , и γ = 5/3для одноатомных газов , таких как благородные газы . В этих особых случаях формулы для удельной теплоемкости уменьшаются:
Одноатомный:
Двухатомный:
Изобарный процесс изображается на P – V -диаграмме в виде прямой горизонтальной линии, соединяющей начальное и конечное термостатические состояния. Если процесс движется вправо, то это расширение. Если процесс движется влево, то это сжатие.
Мотивация принятия особых соглашений о знаках в термодинамике исходит из раннего развития тепловых двигателей. При проектировании теплового двигателя цель состоит в том, чтобы система производила и обеспечивала рабочую мощность. Источником энергии в тепловой машине является тепловложение.
Изохорный процесс описывается уравнением Q = Δ U . Было бы удобно иметь аналогичное уравнение для изобарических процессов. Подставив второе уравнение в первое, получим
Величина U + pV является функцией состояния, поэтому ей можно дать имя. Она называется энтальпией и обозначается как H. Поэтому изобарный процесс можно более кратко описать как
Энтальпия и изохорная удельная теплоемкость являются очень полезными математическими конструкциями, поскольку при анализе процесса в открытой системе возникает ситуация нулевой работы, когда жидкость течет при постоянном давлении. В открытой системе энтальпия — это величина, которую полезно использовать для отслеживания энергосодержания жидкости.
Обратимое расширение идеального газа можно использовать как пример изобарного процесса. [3] Особый интерес представляет способ преобразования тепла в работу, когда расширение осуществляется при различных давлениях рабочего/окружающего газа.
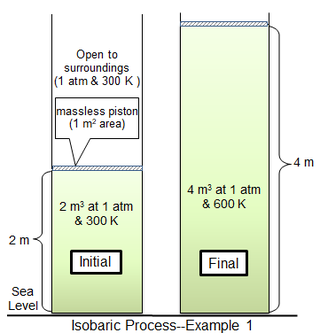
В первом примере процесса цилиндрическая камера площадью 1 м 2 содержит 81,2438 моль идеального двухатомного газа с молекулярной массой 29 г моль -1 при 300 К. Окружающий газ при 1 атм и температуре 300 К отделен от цилиндра. газ тонким поршнем. Для предельного случая безмассового поршня газ в цилиндре также находится под давлением 1 атм и начальным объемом 2 м 3 . Тепло добавляют медленно до тех пор, пока температура газа не станет равномерной 600 К, после чего объем газа составит 4 м 3 и поршень окажется на 2 м выше своего исходного положения. Если движение поршня достаточно медленное, то давление газа в каждый момент времени будет иметь практически одно и то же значение ( p сис = 1 атм) на всем протяжении.
Для термически совершенного двухатомного газа молярная удельная теплоемкость при постоянном давлении ( c p ) равна 7 / 2 R или 29,1006 Дж моль -1 град -1 . Молярная теплоемкость при постоянном объеме ( c v ) равна 5 / 2 R или 20,7862 Дж моль -1 град -1 . Отношение двух теплоемкостей равно 1,4. [4]
Теплота Q , необходимая для нагрева газа от 300 до 600 К, равна
Увеличение внутренней энергии происходит
Поэтому,
Также
, что, конечно, идентично разнице между Δ H и Δ U .
Здесь работа полностью поглощается расширением окружающей среды . Из общего количества приложенного тепла (709,3 кДж) выполненная работа (202,7 кДж) составляет около 28,6% от подведенного тепла.

Второй технологический пример аналогичен первому, за исключением того, что безмассовый поршень заменен на поршень массой 10332,2 кг, что увеличивает давление баллонного газа в два раза до 2 атм. Объем газа в баллоне тогда составляет 1 м 3 при начальной температуре 300 К. Тепло добавляют медленно до тех пор, пока температура газа не станет равномерной 600 К, после чего объем газа составит 2 м 3 и поршень окажется на 1 м выше своего исходного положения. Если движение поршня достаточно медленное, то давление газа в каждый момент времени будет иметь практически одно и то же значение ( p сис = 2 атм) на всем протяжении.
Поскольку энтальпия и внутренняя энергия не зависят от давления,
Как и в первом примере, в работу преобразуется около 28,6% подведенного тепла. Но здесь работа применяется двумя различными способами: частично за счет расширения окружающей атмосферы и частично за счет подъема 10 332,2 кг на расстояние h , равное 1 м. [5]
Таким образом, половина работы поднимает массу поршня (работа силы тяжести, или «полезная» работа), а другая половина расширяет окружающую среду.
Результаты этих двух примеров процесса иллюстрируют разницу между долей тепла, преобразованной в полезную работу ( мг Δ ч) , и долей, преобразованной в работу давление-объем, выполненную против окружающей атмосферы. Полезная работа приближается к нулю, когда давление рабочего газа приближается к давлению окружающего газа, тогда как максимальная полезная работа достигается при отсутствии давления окружающего газа. Отношение всей выполненной работы к подводу тепла для идеального изобарного расширения газа равно
Данное количество (масса m ) газа в изменяющемся объеме вызывает изменение плотности ρ . В этом контексте закон идеального газа записывается
где T — термодинамическая температура , а M — молярная масса . Когда R и M принимаются постоянными, тогда давление P может оставаться постоянным, поскольку квадрант плотности-температуры ( ρ , T ) подвергается отображению сжатия . [6]
Прилагательное «изобарический» происходит от греческих слов ἴσος ( isos ), означающих «равный», и βάρος ( baros ), означающих «вес».
{{cite book}}: CS1 maint: multiple names: authors list (link) CS1 maint: numeric names: authors list (link)