Papillomaviridae — это семейство ДНК-вирусов без оболочки , члены которого известны как папилломавирусы. [1] Было идентифицированонесколько сотен видов папилломавирусов, традиционно называемых «типами», [2] которые заражают всех тщательно проверенных млекопитающих, [2] а также других позвоночных, таких как птицы, змеи, черепахи и рыбы. [3] [4] [5] Заражение большинством типов папилломавирусов, в зависимости от типа, либо протекает бессимптомно (например, большинство бета-PV), либо вызывает небольшие доброкачественные опухоли, известные как папилломы или бородавки (например, вирус папилломы человека 1, ВПЧ6 или ВПЧ11). ). Однако папилломы, вызванные некоторыми типами, такими как вирусы папилломы человека 16 и 18, несут риск перерождения в рак . [6]
Папилломавирусы обычно считаются высокотропными к хозяину и тканям и редко передаются между видами. [7] Папилломавирусы реплицируются исключительно в базальном слое поверхностных тканей тела . Все известные типы папилломавирусов поражают определенную поверхность тела [2] , обычно кожу или эпителий слизистых оболочек половых органов, ануса, рта или дыхательных путей. [8] Например, вирус папилломы человека (ВПЧ) 1-го типа имеет тенденцию поражать подошвы ног, а ВПЧ 2-го типа — ладони рук, где они могут вызывать бородавки . Дополнительно имеются описания наличия ДНК папилломавируса в крови и в мононуклеарных клетках периферической крови .
Папилломавирусы были впервые идентифицированы в начале 20 века, когда было показано, что кожные бородавки или папилломы могут передаваться между людьми фильтрующимся инфекционным агентом. В 1935 году Фрэнсис Пейтон Роус , который ранее продемонстрировал существование вызывающего рак вируса саркомы у кур, продолжил показывать, что папилломавирус может вызывать рак кожи у инфицированных кроликов. Это была первая демонстрация того, что вирус может вызывать рак у млекопитающих.

Известно более 100 видов папилломавирусов [9] , хотя ICTV официально признает меньшее их количество, разделенное на 53 рода, по состоянию на 2019 год. [10] [11] [12] Все папилломавирусы (PV) имеют схожую геномную организацию, и любая пара ПВ содержит не менее пяти гомологичных генов , хотя нуклеотидная последовательность может отличаться более чем на 50%. Филогенетические алгоритмы , позволяющие сравнивать гомологии, привели к созданию филогенетических деревьев , имеющих схожую топологию, независимо от анализируемого гена. [13]
Филогенетические исследования убедительно свидетельствуют о том, что PV обычно развиваются вместе со своими видами-млекопитающими и птицами-хозяевами, но адаптивная радиация , случайные зоонозные события и рекомбинации также могут влиять на их диверсификацию. [13] Их основная геномная организация, по-видимому, сохранялась в течение периода, превышающего 100 миллионов лет, и эти сравнения последовательностей заложили основу для таксономии PV, которая теперь официально признана Международным комитетом по таксономии вирусов . Все PV образуют семейство Papillomaviridae , которое отличается от Polyomaviridae , что исключает термин Papovaviridae . Основными ветвями филогенетического дерева ПВ считаются роды , которые обозначаются греческими буквами. Второстепенные ветви считаются видами и объединяют типы PV, которые геномно различны, но не имеют известных биологических различий. Эта новая таксономическая система не влияет на традиционную идентификацию и характеристику «типов» PV и их независимых изолятов с незначительными геномными различиями, называемых «подтипами» и «вариантами», все из которых являются таксонами ниже уровня «вида». [14] Кроме того, были предложены филогенетические группировки на более высоком таксономическом уровне. [15]
Эта классификация может нуждаться в пересмотре в свете существования рекомбинантов вируса папилломы и полиомы. [16] Также были описаны дополнительные виды. Папилломавирус 1 Sparus aurata выделен из рыбы. [17]
Полностью секвенировано более 170 типов вируса папилломы человека. [18] Их разделили на 5 родов: альфапапилломавирус, бетапапилломавирус, гаммапапилломавирус, мупапилломавирус и нупапилломавирус. Было идентифицировано по меньшей мере 200 дополнительных вирусов, ожидающих секвенирования и классификации. [ нужна цитата ]

Отдельные типы вируса папилломы, как правило, хорошо адаптированы к репликации у одного вида животных. В одном исследовании исследователи взяли мазки с кожи лба различных животных в зоопарке и использовали ПЦР для амплификации любой ДНК папилломавируса, которая могла присутствовать. [19] Хотя в ходе исследования было идентифицировано большое количество последовательностей вируса папилломы, авторы обнаружили мало доказательств межвидовой передачи. У одного смотрителя зоопарка был обнаружен временный положительный результат на последовательность папилломавируса, специфичную для шимпанзе. Однако авторы отмечают, что специфичная для шимпанзе последовательность папилломавируса могла быть результатом поверхностного загрязнения кожи смотрителя зоопарка, а не продуктивной инфекции. [ нужна цитата ]
Вирус папилломы кролика (CRPV) может вызывать выступающие бородавки у своего родного хозяина, североамериканского кролика рода Sylvilagus . Эти роговидные бородавки могут стать исходной основой городских легенд об американском рогатом кролике шакалопе и европейском вольпертингере . [20] Европейские домашние кролики (род Oryctolagus ) могут быть транзиторно инфицированы CRPV в лабораторных условиях. Однако, поскольку европейские домашние кролики не производят вирус инфекционного потомства, они считаются случайными или «тупиковыми» хозяевами CRPV. [21]
Межвидовая передача также была зарегистрирована для вируса папилломы крупного рогатого скота (BPV) типа 1. [22] У естественного хозяина (крупного рогатого скота) BPV-1 вызывает появление крупных фиброзных бородавок на коже. Заражение BPV-1 лошадей, которые являются случайным хозяином вируса, может привести к развитию доброкачественных опухолей, известных как саркоиды . Сельскохозяйственное значение BPV-1 стимулировало успешные усилия по разработке вакцины против этого вируса. [ нужна цитата ]
В нескольких сообщениях папилломавирусы были выявлены у более мелких грызунов, таких как сирийские хомяки , африканская многососковая крыса и евразийская промысловая мышь . [23] Однако не известно, что папилломавирусы способны заражать лабораторных мышей . Отсутствие поддающейся лечению мышиной модели папилломавирусной инфекции было основным ограничением для лабораторных исследований папилломавирусов. [ нужна цитата ]
Известно, что четыре папилломавируса заражают птиц: папилломавирус 1 Fringilla coelebs, папилломавирус 1 Francolinus leucoscepus, папилломавирус 1 Psittacus erithacus и папилломавирус 1 Pygoscelis adeliae. [24] Все эти виды имеют ген (E9) неизвестной функции, что указывает на общее происхождение.
Считается, что эволюция папилломавирусов происходит медленно по сравнению со многими другими типами вирусов, но экспериментальных измерений в настоящее время нет. Вероятно, это связано с тем, что геном папилломавируса состоит из генетически стабильной двухцепочечной ДНК, которая с высокой точностью реплицируется механизмом репликации ДНК клетки-хозяина. [ нужна цитата ]
Считается, что вирусы папилломы обычно эволюционируют совместно с определенным видом животного-хозяина в течение многих лет, хотя существуют убедительные доказательства против гипотезы коэволюции. [13] [25] В качестве особенно быстрого примера можно привести ВПЧ-16, который немного изменился по мере увеличения численности населения по всему миру и теперь различается в разных географических регионах, что, вероятно, отражает историю миграции людей. [26] [27] Кутанеотропные типы ВПЧ иногда передаются между членами семьи в течение всей жизни, но при передаче вируса следует учитывать и других доноров. [28]
Другие типы ВПЧ, такие как ВПЧ-13, относительно мало различаются в разных популяциях человека. Фактически, последовательность ВПЧ-13 очень напоминает вирус папилломы бонобо (также известного как карликовые шимпанзе). [29] Неясно, связано ли это сходство с недавней передачей вируса между видами или с тем, что ВПЧ-13 просто очень мало изменился за шесть или около того миллионов лет, прошедших с тех пор, как люди и бонобо разошлись. [27]
По оценкам, самый последний общий предок этой группы вирусов существовал 424 миллиона лет назад . [30]
Существует пять основных родов, заражающих человека (Альфа, Бета, Гамма, Му и Ню). Последний общий предок этих родов появился 49,7 миллиона лет назад – 58,5 миллиона лет назад . [31] По оценкам, самый последний предок рода гамма появился между 45,3 и 67,5 миллионами лет назад . [ нужна цитата ]
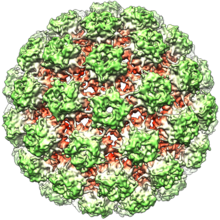
Папилломавирусы не имеют оболочки, то есть внешняя оболочка или капсид вируса не покрыта липидной мембраной . Один вирусный белок, известный как L1, необходим и достаточен для образования капсида размером 55–60 нанометров, состоящего из 72 звездчатых капсомеров (см. Рисунок). Как и у большинства вирусов без оболочки, капсид имеет геометрическую правильную форму и обладает икосаэдрической симметрией . Самособирающиеся вирусоподобные частицы, состоящие из L1, являются основой успешной группы профилактических вакцин против ВПЧ , предназначенных для выработки вируснейтрализующих антител , которые защищают от первичной инфекции ВПЧ. Таким образом, папилломавирусы устойчивы во внешней среде . [ нужна цитата ]
Геном папилломавируса представляет собой двухцепочечную кольцевую молекулу ДНК длиной около 8000 пар оснований . Он упакован внутри оболочки L1 вместе с клеточными белками -гистонами , которые служат для обертывания и конденсации ДНК. [ нужна цитата ]
Капсид папилломавируса также содержит вирусный белок, известный как L2, которого меньше. Хотя неясно, как L2 устроен внутри вириона, известно, что он выполняет несколько важных функций, включая облегчение упаковки вирусного генома в формирующиеся вирионы, а также инфекционное проникновение вируса в новые клетки-хозяева. L2 представляет интерес как возможная мишень для вакцин более широкого защитного действия против ВПЧ .
Вирусный капсид состоит из 72 капсомеров, из которых 12 пятикоординированных и 60 шестикоординированных, расположенных на икосаэдрической поверхностной решетке T = 7d. [32]
Папилломавирусы реплицируются исключительно в кератиноцитах . Кератиноциты образуют внешние слои кожи, а также некоторые поверхности слизистых оболочек , например, внутреннюю часть щеки или стенки влагалища. Эти поверхностные ткани, известные как многослойный плоский эпителий , состоят из сложенных слоев уплощенных клеток. Слои клеток формируются посредством процесса, известного как клеточная дифференциация , при котором кератиноциты постепенно становятся специализированными, в конечном итоге образуя твердую сшитую поверхность, которая предотвращает потерю влаги и действует как барьер против патогенов. Менее дифференцированные стволовые клетки кератиноцитов, пополняющиеся в поверхностном слое, считаются начальной мишенью продуктивных папилломавирусных инфекций. Последующие этапы жизненного цикла вируса строго зависят от процесса дифференцировки кератиноцитов. В результате папилломавирусы могут реплицироваться только в поверхностных тканях тела. [ нужна цитата ]
Папилломавирусы получают доступ к стволовым клеткам кератиноцитов через небольшие раны, известные как микротравмы, на поверхности кожи или слизистой оболочки. Взаимодействие между L1 и сульфатированными сахарами на поверхности клетки способствует начальному прикреплению вируса. [33] [34] Затем вирус может проникнуть внутрь с поверхности клетки посредством взаимодействия со специфическим рецептором, вероятно, через интегрин альфа-6 бета-4, [35] [36] и транспортироваться в закрытые мембраной везикулы , называемые эндосомы . [37] [38] Капсидный белок L2 разрушает мембрану эндосомы посредством катионного проникающего в клетку пептида , позволяя вирусному геному ускользнуть и переместиться вместе с L2 в ядро клетки. [39] [40] [41]
После успешного заражения кератиноцита вирус экспрессирует белки E1 и E2, которые предназначены для репликации и поддержания вирусной ДНК в виде кольцевой эписомы . Вирусные онкогены E6 и E7 способствуют росту клеток, инактивируя белки-супрессоры опухолей p53 и pRb . Стволовые клетки кератиноцитов в базальном слое эпителия могут сохранять геномы папилломавируса в течение десятилетий. [8]
В настоящее время считается, что репликация вирусной ДНК, вероятно, происходит в фазе G 2 клеточного цикла и зависит от рекомбинационно-зависимой репликации, поддерживаемой механизмами ответа на повреждение ДНК (активируемыми белком E7) для производства потомства вирусных геномов. [42] Геномы папилломавирусов иногда интегрируются в геном хозяина, что особенно заметно при онкогенных ВПЧ, но это не является нормальной частью жизненного цикла вируса и тупиком, исключающим возможность производства вирусного потомства. [42]
Экспрессия поздних генов вируса, L1 и L2, ограничивается исключительно дифференцировкой кератиноцитов в самых внешних слоях кожи или поверхности слизистой оболочки. Повышенная экспрессия L1 и L2 обычно коррелирует с резким увеличением количества копий вирусного генома. Поскольку внешние слои многослойного плоского эпителия подлежат относительно ограниченному наблюдению со стороны клеток иммунной системы, считается, что это ограничение экспрессии поздних вирусных генов представляет собой форму уклонения от иммунитета. [ нужна цитата ]
В ядре клетки собираются новые инфекционные вирусы-потомки . Папилломавирусы развили механизм высвобождения вирионов в окружающую среду. Другие виды вирусов животных без оболочки используют активный литический процесс для уничтожения клетки-хозяина, позволяя высвободить вирусные частицы-потомки. Часто этот литический процесс связан с воспалением , которое может спровоцировать иммунную атаку против вируса. Папилломавирусы используют десквамацию как скрытый, невоспалительный механизм высвобождения. [ нужна цитата ]
Хотя некоторые типы папилломавирусов могут вызывать рак эпителиальных тканей, в которых они обитают, рак не является типичным исходом инфекции. Развитие рака, вызванного вирусом папилломы, обычно происходит в течение многих лет. Папилломавирусы связаны с развитием рака шейки матки , рака полового члена [43] и рака полости рта . [44] Также была отмечена связь рака вульвы и уротелиальной карциномы с плоскоклеточной дифференцировкой у пациенток с нейрогенным мочевым пузырем. [45] [46] Существует геном папилломавируса, вызывающего рак, который кодирует два небольших белка, называемых E6 и E7, которые имитируют онкогены, вызывающие рак. Они работают так: стимулируют неестественный рост клеток и блокируют их естественную защиту. Также они действуют на многие сигнальные белки, контролирующие пролиферацию и апоптоз. [47]
Тот факт, что жизненный цикл папилломавируса строго требует дифференцировки кератиноцитов, представляет собой существенный барьер для изучения папилломавирусов в лаборатории, поскольку он исключает использование обычных клеточных линий для выращивания вирусов. Поскольку инфекционные вирионы BPV-1 могут быть извлечены из больших бородавок, которые вирус вызывает у крупного рогатого скота, в течение многих лет этот тип папилломавируса был рабочей лошадкой. CRPV, вирус оральной папилломы кролика (ROPV) и вирус оральной папилломы собаки (COPV) также широко использовались в лабораторных исследованиях. Как только исследователи обнаружили, что эти вирусы вызывают рак, они начали вместе искать вакцину от него. В настоящее время наиболее эффективным способом добиться этого является имитация вируса, состоящего из белка L1, но лишенного ДНК. По сути, наша иммунная система вырабатывает защиту от инфекций, но если эти инфекции не вызывают заболевания, их можно использовать в качестве вакцины. Запись 6bt3 в PDB показывает, как поверхности антител атакуют поверхность вируса, чтобы вывести его из строя. [48]
Некоторые типы ВПЧ, передающиеся половым путем, размножаются с использованием мышиной системы «ксенотрансплантата», при которой инфицированные ВПЧ человеческие клетки имплантируются мышам с иммунодефицитом . Совсем недавно некоторым группам удалось изолировать инфекционный ВПЧ-16 из поражений шейки матки человека. Однако выделение инфекционных вирионов с использованием этого метода затруднено, а выход инфекционного вируса очень низок. [ нужна цитата ]
Дифференцировку кератиноцитов можно имитировать in vitro , подвергая культивированные кератиноциты воздействию поверхности раздела воздух/жидкость. Адаптация таких систем «плотной культуры» к изучению папилломавирусов стала значительным прорывом в изучении жизненного цикла вируса in vitro . [49] Однако системы культивирования на плотах относительно громоздки, а выход инфекционных ВПЧ может быть низким. [50]
Разработка системы на основе дрожжей, обеспечивающей стабильную эписомальную репликацию ВПЧ, обеспечивает удобный, быстрый и недорогой способ изучения некоторых аспектов жизненного цикла ВПЧ (Angeletti 2002). Например, E2-зависимая транскрипция, амплификация генома и эффективная инкапсидация полноразмерных ДНК ВПЧ могут быть легко воссозданы у дрожжей (Angeletti 2005).
Недавно были разработаны временные высокопроизводительные методы получения псевдовирусов ВПЧ, несущих репортерные гены. Хотя псевдовирусы не подходят для изучения некоторых аспектов жизненного цикла вирусов, первоначальные исследования показывают, что их структура и начальное инфекционное проникновение в клетки, вероятно, во многом аналогичны подлинным папилломавирусам.
Вирус папилломы человека связывается с молекулами гепарина на поверхности клеток, которые он заражает. Исследования показали, что кристалл изолированных капсомеров L1 имеет цепи гепарина, узнаваемые по бороздкам лизиновых линий на поверхности вируса. Также те, у кого есть антитела, показывают, что они могут блокировать это распознавание. [51]
[52]
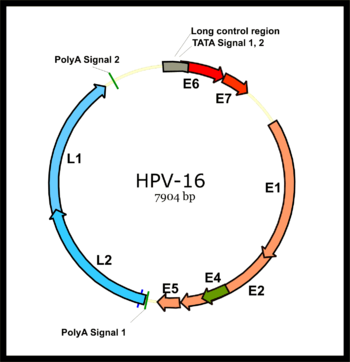
Геном папилломавируса разделен на раннюю область (Е), кодирующую шесть открытых рамок считывания (ORF) (Е1, Е2, Е4, Е5, Е6 и Е7), которые экспрессируются сразу после первичного заражения клетки-хозяина, и позднюю область. область (L), кодирующая основной капсидный белок L1 и минорный капсидный белок L2. Все вирусные ORF кодируются на одной цепи ДНК (см. рисунок). Это представляет собой резкое различие между папилломавирусами и полиомавирусами , поскольку последний тип вируса экспрессирует свои ранние и поздние гены посредством двунаправленной транскрипции обеих цепей ДНК. Это различие стало основным фактором в установлении консенсуса о том, что папилломавирусы и полиомавирусы, вероятно, никогда не имели общего предка, несмотря на поразительное сходство в структурах их вирионов. [ нужна цитата ]
После инфицирования клетки-хозяина активируется ранний промотор HPV16 и транскрибируется полицистронная первичная РНК, содержащая все шесть ранних ORF. Эта полицистронная РНК содержит три экзона и два интрона и подвергается активному сплайсингу РНК с образованием множества изоформ мРНК. [52] Одна из сплайсированных изоформ РНК, E6*I, служит мРНК E7 для трансляции онкобелка E7. [53] Напротив, интрон в ORF E6, который остается интактным без сплайсинга, необходим для трансляции онкобелка E6. [53] Однако ранняя вирусная транскрипция подвергается вирусной регуляции E2, а высокие уровни E2 подавляют транскрипцию. Геномы ВПЧ интегрируются в геном хозяина путем разрушения ORF E2, предотвращая репрессию E2 на E6 и E7. Таким образом, интеграция вирусного генома в геном ДНК хозяина увеличивает экспрессию E6 и E7, что способствует клеточной пролиферации и вероятности злокачественного новообразования. [ нужна цитата ]
Основной поздний промотор вируса в ранней области вируса становится активным только в дифференцированных клетках, и его активность может быть значительно усилена за счет репликации вирусной ДНК. Поздний транскрипт также представляет собой полицистронную РНК, содержащую два интрона и три экзона. Альтернативный сплайсинг РНК этого позднего транскрипта важен для экспрессии L1 и L2 и может регулироваться цис-элементами РНК и факторами сплайсинга хозяина. [52] [54] [55]
Гены в геноме папилломавируса обычно идентифицируются по сходству с другими ранее идентифицированными генами. Однако некоторые ложные открытые рамки считывания могли быть ошибочно приняты за гены просто по их положению в геноме и не могли быть настоящими генами. Это особенно относится к некоторым открытым рамкам считывания E3, E4, E5 и E8 . [ нужна цитата ]
Кодирует белок, который связывается с точкой начала репликации вируса в длинной контрольной области вирусного генома. E1 использует АТФ для проявления активности геликазы , которая раздвигает цепи ДНК, тем самым подготавливая вирусный геном к репликации факторами репликации клеточной ДНК .
Белок Е2 служит главным регулятором транскрипции для вирусных промоторов , расположенных преимущественно в длинной контрольной области. Белок имеет домен трансактивации , связанный относительно неструктурированной шарнирной областью с хорошо изученным ДНК-связывающим доменом. E2 облегчает связывание E1 с вирусной точкой начала репликации. E2 также использует клеточный белок, известный как Бромодомен -4 (Brd4), для привязки вирусного генома к клеточным хромосомам. [56] Эта привязка к ядерному матриксу клетки обеспечивает точное распределение вирусных геномов между каждой дочерней клеткой после клеточного деления. Считается, что Е2 служит негативным регулятором экспрессии онкогенов Е6 и Е7 в латентно инфицированных ВПЧ кератиноцитах базального слоя . Генетические изменения, такие как интеграция вирусной ДНК в хромосому клетки-хозяина, которые инактивируют экспрессию E2, имеют тенденцию увеличивать экспрессию онкогенов E6 и E7, что приводит к клеточной трансформации и, возможно, дальнейшей генетической дестабилизации.
Этот небольшой предполагаемый ген существует только в нескольких типах папилломавирусов. Неизвестно, что этот ген экспрессируется в виде белка и, по-видимому, не выполняет никакой функции.
Хотя белки Е4 экспрессируются на низких уровнях на ранней стадии вирусной инфекции, экспрессия Е4 резко возрастает на поздней стадии инфекции. Другими словами, его название «E» может быть неправильным. В случае ВПЧ-1 Е4 может составлять до 30% общего белка на поверхности бородавки. [57] Считается, что белок E4 многих типов папилломавирусов способствует высвобождению вирионов в окружающую среду, разрушая промежуточные нити цитоскелета кератиноцитов . Вирусные мутанты, неспособные экспрессировать E4, не поддерживают репликацию вирусной ДНК на высоком уровне, но пока неясно, как E4 облегчает репликацию ДНК. Также было показано, что E4 участвует в остановке клеток в фазе G2 клеточного цикла .
E5 — это маленькие, очень гидрофобные белки, которые дестабилизируют функцию многих мембранных белков в инфицированной клетке. [58] Белок E5 некоторых типов вируса папилломы животных (в основном вируса папилломы крупного рогатого скота типа 1) действует как онкоген , прежде всего, активируя способствующую росту клеток передачу сигналов рецепторов тромбоцитарного фактора роста . Однако белки E5 вирусов папилломы человека, связанных с раком, по-видимому, активируют сигнальный каскад, инициируемый эпидермальным фактором роста при связывании лиганда. Также было показано, что HPV16 E5 и HPV2 E5 подавляют поверхностную экспрессию белков класса I главного комплекса гистосовместимости , что может препятствовать уничтожению инфицированной клетки Т-клетками-киллерами .

E6 представляет собой пептид из 151 аминокислоты, который включает мотив типа 1 с консенсусной последовательностью –(T/S)-(X)-(V/I)-COOH. [60] [61] Он также имеет два мотива в виде цинковых пальцев . [60]
E6 представляет особый интерес, поскольку он, по-видимому, выполняет множество ролей в клетке и взаимодействует со многими другими белками. Однако его основная роль заключается в опосредовании деградации р53 , основного белка -супрессора опухолей , снижая способность клетки реагировать на повреждение ДНК . [62] [63]
Также было показано, что E6 воздействует на другие клеточные белки, тем самым изменяя несколько метаболических путей . Одной из таких мишеней является NFX1-91 , который обычно подавляет выработку теломеразы , белка, который позволяет клеткам делиться неограниченное количество раз. Когда NFX1-91 разрушается под действием E6, уровни теломеразы повышаются, инактивируя основной механизм, сдерживающий рост клеток. [64] Кроме того, E6 может действовать как кофактор транскрипции, в частности, как активатор транскрипции, при взаимодействии с клеточным фактором транскрипции E2F1/DP1. [60]
E6 также может связываться с PDZ-доменами — короткими последовательностями, которые часто встречаются в сигнальных белках. Структурный мотив E6 позволяет взаимодействовать с доменами PDZ в генах-супрессорах опухолей DLG (большие диски) и hDLG (большие дрозофилы). [61] [65] Связывание в этих местах вызывает трансформацию белка DLG и нарушение его супрессорной функции. Белки E6 также взаимодействуют с белками MAGUK (семейство мембранассоциированных гуанилаткиназ). Эти белки, включая MAGI-1, MAGI-2 и MAGI-3, обычно являются структурными белками и могут способствовать передаче сигналов. [61] [65] Что еще более важно, они, как полагают, участвуют в подавляющей активности DLG. Когда E6 образует комплекс с доменами PDZ на белках MAGI, это искажает их форму и тем самым нарушает их функцию. В целом, белок E6 препятствует нормальной активности белка таким образом, что позволяет клетке расти и размножаться с повышенной скоростью, характерной для рака.
Поскольку экспрессия Е6 строго необходима для поддержания злокачественного фенотипа при раке, индуцированном ВПЧ, она является привлекательной мишенью для терапевтических вакцин против ВПЧ , предназначенных для искоренения уже сформировавшихся опухолей рака шейки матки.
В большинстве типов папилломавирусов основной функцией белка Е7 является инактивация членов семейства белков-супрессоров опухоли pRb . Вместе с E6 E7 служит для предотвращения гибели клеток ( апоптоза ) и содействия развитию клеточного цикла , тем самым подготавливая клетку к репликации вирусной ДНК. Е7 также участвует в иммортализации инфицированных клеток путем активации клеточной теломеразы . Как и E6, E7 является предметом пристального исследовательского интереса и, как полагают, оказывает широкий спектр других эффектов на инфицированные клетки. Как и в случае с E6, продолжающаяся экспрессия E7 необходима для выживания линий раковых клеток, таких как HeLa , которые происходят из опухолей, индуцированных ВПЧ. [66]
Лишь несколько типов папилломавирусов кодируют короткий белок гена Е8. В случае BPV-4 (род папилломавирусов Xi ) открытая рамка считывания E8 может заменять открытую рамку считывания E6, которая отсутствует у этого рода папилломавирусов. [67] Эти гены E8 химически и функционально аналогичны генам E5 некоторых вирусов папилломы человека и также называются E5/E8.
L1 спонтанно самоорганизуется в пентамерные капсомеры. Очищенные капсомеры могут образовывать капсиды, которые стабилизируются дисульфидными связями между соседними молекулами L1. Капсиды L1, собранные in vitro , составляют основу профилактических вакцин против нескольких типов ВПЧ. По сравнению с генами других папилломавирусов, аминокислотные последовательности большинства частей L1 хорошо консервативны между типами. Однако поверхностные петли L1 могут существенно различаться даже у разных представителей конкретного вида папилломавируса. Вероятно, это отражает механизм уклонения от реакции нейтрализующих антител, вызванной предыдущими папилломавирусными инфекциями. [68]
L2 существует в окисленном состоянии внутри вириона папилломавируса, при этом два консервативных остатка цистеина образуют внутримолекулярную дисульфидную связь. [69] Было показано, что помимо сотрудничества с L1 для упаковки вирусной ДНК в вирион, L2 взаимодействует с рядом клеточных белков во время процесса проникновения инфекции. После первоначального связывания вириона с клеткой L2 должен быть расщеплен клеточной протеазой фурином . [70] Вирион интернализуется, вероятно, посредством клатрин-опосредованного процесса, в эндосому, где кислые условия, как полагают, приводят к обнажению дестабилизирующих мембрану частей L2. [39] Клеточные белки бета- актин [71] и синтаксин -18 [72] также могут участвовать в событиях входа, опосредованных L2. После выхода из эндосомы L2 и вирусный геном импортируются в ядро клетки, где они перемещаются в субъядерный домен, известный как тельце ND-10, богатый факторами транскрипции . [40] Небольшие части L2 хорошо консервативны между различными типами папилломавирусов, и экспериментальные вакцины, нацеленные на эти консервативные домены, могут обеспечить защиту от широкого спектра типов ВПЧ. [73]