Простациклин (также называемый простагландином I 2 или PGI 2 ) является простагландином , членом семейства эйкозаноидных липидных молекул . Он ингибирует активацию тромбоцитов, а также является эффективным сосудорасширяющим средством.
При использовании в качестве лекарственного средства он также известен как эпопростенол . [1] Эти термины иногда используются как взаимозаменяемые. [2]
Простациклин главным образом предотвращает образование тромбоцитарной пробки , участвующей в первичном гемостазе (часть образования тромба ). Это происходит путем ингибирования активации тромбоцитов. [3] Это также эффективное сосудорасширяющее средство . Взаимодействие простациклина контрастирует с взаимодействием тромбоксана (TXA 2 ), другого эйкозаноида. Обе молекулы являются производными арахидоновой кислоты и действуют вместе, оказывая противоположные эффекты агрегации тромбоцитов. Это убедительно свидетельствует о механизме сердечно-сосудистого гомеостаза между этими двумя гормонами в отношении повреждения сосудов .
Его применяют для лечения легочной артериальной гипертензии (ЛАГ), [4] [5] легочного фиброза , [6] а также атеросклероза . [6] В частности, эпопростенол назначают пациентам с ЛАГ III или IV класса. [ нужна цитата ]
Простациклин, период полувыведения которого составляет 42 секунды, [7] расщепляется до 6-кето-PGF 1 , который является гораздо более слабым сосудорасширяющим средством. Способ стабилизации простациклина в его активной форме, особенно во время доставки лекарства, заключается в приготовлении простациклина в щелочном буфере. Даже при физиологическом pH простациклин может быстро образовывать неактивный продукт гидратации 6-кето-простагландин F1α. [8]
Как упоминалось выше, простациклин (PGI 2 ) высвобождается здоровыми эндотелиальными клетками и выполняет свою функцию через паракринный сигнальный каскад, который задействует рецепторы, связанные с G-белком , на близлежащих тромбоцитах и эндотелиальных клетках. Рецептор простациклина, связанный с белком Gs тромбоцитов ( рецептор простациклина ), активируется, когда он связывается с PGI 2 . Эта активация, в свою очередь, сигнализирует аденилатциклазе о выработке цАМФ . цАМФ ингибирует любую чрезмерную активацию тромбоцитов (чтобы стимулировать кровообращение), а также противодействует любому повышению уровня цитозольного кальция, которое может возникнуть в результате связывания тромбоксана А2 (TXA 2 ) (что приводит к активации тромбоцитов и последующей коагуляции ). PGI 2 также связывается с эндотелиальными рецепторами простациклина и таким же образом повышает уровни цАМФ в цитозоле. Затем этот цАМФ активирует протеинкиназу А (ПКА). Затем PKA продолжает каскад, способствуя фосфорилированию киназы легкой цепи миозина , что ингибирует его и приводит к расслаблению гладких мышц и расширению сосудов . Можно отметить, что PGI 2 и TXA 2 действуют как физиологические антагонисты.

Синтетические аналоги простациклина ( илопрост , цизапрост) применяют внутривенно, подкожно или ингаляционно:
Продукция простациклина ингибируется действием НПВП на ферменты циклооксигеназы ЦОГ1 и ЦОГ2. Они превращают арахидоновую кислоту в простагландин H2 (PGH 2 ), непосредственный предшественник простациклина. Поскольку тромбоксан ( эйкозаноидный стимулятор агрегации тромбоцитов) также находится ниже ферментов ЦОГ, можно подумать, что эффект НПВП будет способствовать балансированию. Однако концентрация простациклина восстанавливается гораздо быстрее, чем уровень тромбоксана, поэтому введение аспирина первоначально практически не оказывает никакого эффекта, но в конечном итоге предотвращает агрегацию тромбоцитов (эффект простагландинов преобладает по мере их регенерации). Это объясняется пониманием клеток, которые производят каждую молекулу, TXA 2 и PGI 2 . Поскольку PGI 2 в основном продуцируется в ядросодержащих эндотелиальных клетках, ингибирование ЦОГ НПВП можно со временем преодолеть за счет увеличения активации гена ЦОГ и последующей продукции большего количества ферментов ЦОГ, катализирующих образование PGI 2 . Напротив, TXA 2 высвобождается преимущественно безъядерными тромбоцитами, которые не способны реагировать на ингибирование ЦОГ НПВП дополнительной транскрипцией гена ЦОГ, поскольку им не хватает материала ДНК , необходимого для выполнения такой задачи. Это позволяет НПВП привести к доминированию PGI 2 , что способствует кровообращению и замедляет тромбоз .
У пациентов с легочной гипертензией ингаляционный эпопростенол снижает легочное давление и улучшает ударный объем правого желудочка у пациентов, перенесших кардиохирургию. Доза 60 мкг гемодинамически безопасна, ее эффект полностью прекращается через 25 минут. Никаких признаков дисфункции тромбоцитов или увеличения хирургического кровотечения после введения ингаляционного эпопростенола не обнаружено. [10] Известно, что препарат вызывает приливы, головные боли и гипотонию. [11]
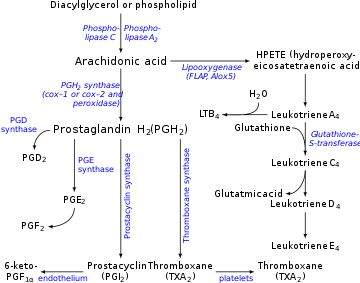
Простациклин вырабатывается в эндотелиальных клетках , выстилающих стенки артерий и вен, [12] из простагландина H 2 (PGH 2 ) под действием фермента простациклинсинтазы . Хотя простациклин считается независимым медиатором, в эйкозаноидной номенклатуре он называется PGI 2 (простагландин I 2 ) и входит в группу простаноидов (вместе с простагландинами и тромбоксаном ). PGI 2 , полученный в основном из ЦОГ-2 у человека, является основным метаболитом арахидоната, высвобождаемым из эндотелия сосудов. Это спорный момент, некоторые относят ЦОГ-1 к основному простациклину, продуцирующему циклооксигеназу в эндотелиальных клетках кровеносных сосудов. [13]
Простагландин PGH 3 серии-3 также следует по пути простациклинсинтазы, образуя другой простациклин, PGI 3 . [14] Неквалифицированный термин «простациклин» обычно относится к PGI 2 . PGI 2 получен из арахидоновой кислоты ω-6 . PGI 3 получен из ω-3 EPA .
Простациклин можно синтезировать из метилового эфира простагландина F 2α . [15] После синтеза препарат восстанавливают в физиологическом растворе и глицерине. [16]
Поскольку простациклин настолько химически лабильен, для оценки скорости его синтеза используется количественное определение его неактивных метаболитов, а не активных соединений. [17]
В 1960-е годы британская исследовательская группа во главе с профессором Джоном Вейном начала изучать роль простагландинов в анафилаксии и респираторных заболеваниях. Работая с командой из Королевского колледжа хирургов , Вейн обнаружил, что аспирин и другие пероральные противовоспалительные препараты действуют путем ингибирования синтеза простагландинов. Это важное открытие открыло дверь к более широкому пониманию роли простагландинов в организме.
Команда The Wellcome Foundation под руководством Сальвадора Монкады идентифицировала липидный медиатор, который они назвали «PG-X», который ингибирует агрегацию тромбоцитов. PG-X, позже известный как простациклин, в 30 раз более эффективен, чем любой другой известный на тот момент антиагрегационный агент. Они сделали это в поисках фермента, который генерирует аналогичный нестабильный простаноид, тромбоксан А2 [18].
В 1976 году Вейн и его коллеги-исследователи Сальвадор Монкада , Рышард Грыглевски и Стюарт Бантинг опубликовали первую статью о простациклине в журнале Nature . [19] В результате сотрудничества была синтезирована молекула, получившая название эпопростенол. Но, как и нативный простациклин, молекула эпопростенола нестабильна в растворе и склонна к быстрой деградации. [ нужна цитация ] Это представляло проблему как для экспериментов in vitro, так и для клинического применения.
Чтобы преодолеть эту проблему, исследовательская группа, открывшая простациклин, продолжила исследования. Исследовательская группа синтезировала около 1000 аналогов. [ нужна цитата ]