Триоксид серы (альтернативное написание триоксид серы , также известный как ниссо сульфан ) представляет собой химическое соединение с формулой SO 3 . Его описывают как «несомненно самый [экономически важный]» оксид серы. [1] Его получают в промышленных масштабах как прекурсор серной кислоты .
Триоксид серы существует в нескольких формах — газообразный мономер, кристаллический тример и твердый полимер. Триоксид серы представляет собой твердое вещество при температуре чуть ниже комнатной с относительно узким диапазоном жидкости. Газообразный SO 3 является основным предшественником кислотных дождей . [6]
Молекула SO 3 тригонально -плоская . Как предсказывает теория VSEPR , его структура принадлежит точечной группе D3h . Атом серы имеет степень окисления +6, и ему может быть присвоено формальное значение заряда от 0 (если предполагается, что все три связи сера-кислород являются двойными связями) или до +2 (если предполагается правило октетов). ). [7] Когда формальный заряд отличен от нуля, предполагается, что SO-связь делокализована. В любом случае длины трех связей SO равны друг другу и составляют 1,42 Å. [1] Электрический дипольный момент газообразного триоксида серы равен нулю.
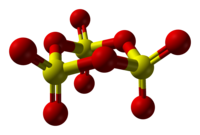
Как жидкая, так и газообразная [8] SO 3 существует в равновесии между мономером и циклическим тримером. Природа твердого SO 3 сложна, и известны по меньшей мере три его полиморфные модификации , конверсия между которыми зависит от следов воды. [9]
Абсолютно чистый SO 3 замерзает при 16,8°C с образованием формы γ -SO 3 , которая принимает конфигурацию циклического тримера [S(=O) 2 ( μ -O)] 3 . [10] [1]

Если SO 3 конденсируется выше 27 °С, то образуется α -SO 3 , температура плавления которого составляет 62,3 °С. α -SO 3 имеет волокнистый вид. Структурно это полимер [S(=O) 2 ( μ -O)] n . Каждый конец полимера имеет на конце ОН-группы. [1] β -SO 3 , как и альфа-форма, является волокнистым, но имеет другую молекулярную массу, состоит из полимера с гидроксильными группами, но плавится при 32,5 °C. И гамма-, и бета-формы метастабильны и в конечном итоге преобразуются в стабильную альфа-форму, если оставить их стоять на достаточное время. Это преобразование вызвано следами воды. [11]
Относительное давление паров твердого SO 3 составляет альфа < бета < гамма при одинаковых температурах, что указывает на их относительную молекулярную массу . Жидкий триоксид серы имеет давление паров, соответствующее гамма-форме. Таким образом, нагрев кристалла α -SO 3 до температуры плавления приводит к внезапному увеличению давления пара, которое может быть достаточно сильным, чтобы разрушить стеклянный сосуд, в котором он нагревается. Этот эффект известен как «альфа-взрыв». [11]
Триоксид серы вступает во множество реакций. [1]
SO 3 представляет собой ангидрид H 2 SO 4 . Таким образом, он подвержен гидратации:
Газообразный триоксид серы обильно дымит даже в относительно сухой атмосфере вследствие образования тумана серной кислоты. SO 3 агрессивно гигроскопичен . Теплоты гидратации достаточно, чтобы смеси SO 3 и дерева или хлопка могли воспламениться. В таких случаях SO 3 обезвоживает эти углеводы . [11]
Подобно поведению H 2 O, присоединение фтористого водорода дает сернофтористую кислоту :
SO 3 реагирует с пятиокисью азота с образованием нитрониевой соли пиросульфата:
Триоксид серы является окислителем. Окисляет дихлорид серы до тионилхлорида .
SO 3 представляет собой сильную кислоту Льюиса , легко образующую аддукты с основаниями Льюиса. [13] С пиридином образуется комплекс триоксида серы с пиридином . Родственные аддукты образуются из диоксана и триметиламина .
Триоксид серы является сильным сульфирующим агентом , т.е. он присоединяет группы SO 3 к субстратам. Часто субстраты являются органическими, как при ароматическом сульфировании . [14] Для активированных субстратов аддукты основания Льюиса с триоксидом серы являются эффективными сульфирующими агентами. [15]
Прямое окисление диоксида серы до триоксида серы на воздухе протекает очень медленно:
В промышленности SO 3 производится контактным способом . Диоксид серы получают путем сжигания серы или железного пирита (сульфидной руды железа). После очистки электростатическим осаждением SO 2 затем окисляется кислородом воздуха при температуре от 400 до 600°C над катализатором. Типичный катализатор состоит из пятиокиси ванадия (V 2 O 5 ), активированной оксидом калия K 2 O на кизельгуре или кремнеземном носителе. Платина также работает очень хорошо, но она слишком дорога и гораздо легче отравляется (делается неэффективной) примесями. [16] Большая часть триоксида серы, полученного таким способом, превращается в серную кислоту .
Триоксид серы можно получить в лаборатории двухстадийным пиролизом бисульфата натрия . Пиросульфат натрия является промежуточным продуктом: [17]
Напротив, KHSO 4 не вступает в такую реакцию. [17]
Другой двухэтапный метод, включающий пиролиз соли, начинается с концентрированной серной кислоты и безводного тетрахлорида олова:
Преимущество этого метода перед методом с использованием бисульфата натрия состоит в том, что он требует гораздо более низких температур и может быть выполнен с использованием обычной боросиликатной лабораторной посуды без риска разбиения. Недостатком является то, что при этом образуются значительные количества газообразного хлористого водорода, который также необходимо улавливать.
SO 3 также можно получить путем дегидратации серной кислоты пятиокисью фосфора . [18]
Триоксид серы является реагентом в реакциях сульфирования . Эти процессы позволяют получать моющие средства , красители и фармацевтические препараты . Триоксид серы образуется на месте из серной кислоты или используется в виде раствора в кислоте.
Стабилизированный B 2 O 3 триоксид серы продавался компанией Baker & Adamson под торговой маркой « Сульфан » в 20 веке. [19]
Помимо того, что триоксид серы является окислителем, он обладает высокой коррозионной активностью. Он бурно реагирует с водой с образованием очень агрессивной серной кислоты.
Использовался триоксид серы в виде чистой бесцветной жидкости SO3, продаваемой Бейкером и Адамсоном под торговым названием Sulfan.