В химии трансферная гидрогенизация — это химическая реакция , включающая добавление водорода к соединению из источника, отличного от молекулярного H 2 . Она применяется в лабораторном и промышленном органическом синтезе для насыщения органических соединений и восстановления кетонов до спиртов , а иминов до аминов . Она позволяет избежать необходимости в молекулярном H 2 высокого давления, используемом при обычной гидрогенизации . Трансферная гидрогенизация обычно происходит при умеренных условиях температуры и давления с использованием органических или металлоорганических катализаторов, многие из которых являются хиральными , что позволяет проводить эффективный асимметричный синтез . Она использует соединения-доноры водорода, такие как муравьиная кислота , изопропанол или дигидроантрацен , дегидрируя их до CO 2 , ацетона или антрацена соответственно. [1] Часто донорные молекулы также выполняют функцию растворителей для реакции. Крупномасштабным применением трансферной гидрогенизации является сжижение угля с использованием «донорных растворителей», таких как тетралин . [2] [3]
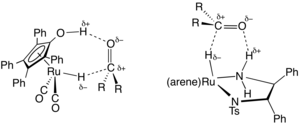
В области органического синтеза было разработано полезное семейство катализаторов переноса водорода на основе комплексов рутения и родия , часто с диаминовыми и фосфиновыми лигандами. [4] Представительный предшественник катализатора получен из димера дихлорида (цимен)рутения и тозилированного дифенилэтилендиамина . Эти катализаторы в основном используются для восстановления кетонов и иминов до спиртов и аминов соответственно. Донором водорода (агентом переноса) обычно является изопропанол , который превращается в ацетон при отдаче водорода. Гидрогенизации переноса могут протекать с высокой энантиоселективностью , когда исходный материал является прохиральным :
где RR'C*H−OH — хиральный продукт. Типичным катализатором является (цимен) R,R -HNCHPhCHPhNTs , где Ts относится к тозильной группе ( SO 2 C 6 H 4 Me ), а R,R относится к абсолютной конфигурации двух хиральных углеродных центров. Эта работа была отмечена Нобелевской премией по химии 2001 года, присужденной Рёдзи Ноёри . [5]
Другое семейство агентов переноса водорода основано на алкоголятах алюминия, таких как изопропоксид алюминия в восстановлении MPV ; однако их активность относительно низка по сравнению с системами на основе переходных металлов.
Каталитическое асимметричное гидрирование кетонов было продемонстрировано с использованием комплексов BINAP на основе рутения . [6] [7]
Хотя дигалогенидный катализатор BINAP-Ru мог восстанавливать функционализированные кетоны, гидрирование простых кетонов оставалось нерешенным. Эта задача была решена с помощью прекатализаторов типа RuCl 2 ( дифосфан )(диамин). [8] Эти катализаторы преимущественно восстанавливают кетоны и альдегиды, оставляя олефины и многие другие заместители незатронутыми.

До разработки каталитического гидрирования было разработано много методов гидрирования ненасыщенных субстратов. Многие из этих методов представляют только исторический и педагогический интерес. Одним из выдающихся агентов переноса гидрирования является диимид или (NH) 2 , также называемый диазеном. Он окисляется до очень стабильного N2 :
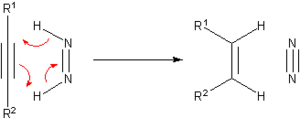
Диимид может быть получен из гидразина или некоторых других органических прекурсоров.
Два углеводорода, которые могут служить донорами водорода, — это циклогексен или циклогексадиен . В этом случае образуется алкан вместе с бензолом . Движущей силой реакции является прирост энергии ароматической стабилизации при образовании бензола. В качестве катализатора можно использовать Pd, а температура применяется 100 °C. Сообщалось о более экзотических трансферных гидрированиях, включая это внутримолекулярное:

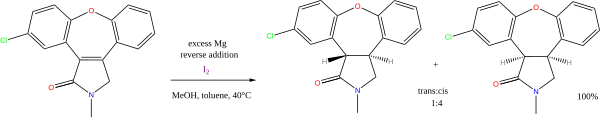
Существует множество реакций , в которых в качестве доноров протонов выступают спирт или амины , а в качестве доноров электронов — щелочные металлы. Неизменно ценным является восстановление аренов (другое название ароматических углеводородов) по методу Берча, опосредованное металлическим натрием . Менее важным в настоящее время является восстановление сложных эфиров по методу Буво-Блана . Сочетание магния и метанола используется в восстановлении алкенов, например, в синтезе азенапина : [11]
Органокаталитическое переносное гидрирование было описано группой Листа в 2004 году в системе с эфиром Ганча в качестве донора гидрида и аминным катализатором: [12]
В этой конкретной реакции субстратом является α,β-ненасыщенное карбонильное соединение . Донор протона окисляется до пиридиновой формы и напоминает биохимически соответствующий кофермент NADH . В каталитическом цикле для этой реакции амин и альдегид сначала образуют иминиевый ион , затем перенос протона сопровождается гидролизом иминиевой связи, восстанавливая катализатор. При использовании хирального имидазолидинонового органокатализатора MacMillan была получена энантиоселективность 81% ee :
[13]
В случае стереоконвергенции как E-изомер , так и Z-изомер в этой реакции дают (S) -энантиомер .
Расширение области действия этой реакции в сторону кетонов или, скорее, енонов требует тонкой настройки катализатора (добавления бензильной группы и замены трет-бутильной группы на фуран ) и эфира Ганча (добавления более объемных трет-бутильных групп): [14]
С другим органическим катализатором гидрирование может быть также осуществлено для иминов . Одна каскадная реакция катализируется хиральной фосфорной кислотой : [15]
Реакция протекает через хиральный ион иминия . Традиционные катализаторы на основе металлов, гидрирование ароматических или гетероароматических субстратов, как правило, не дают результата.