Сульфат кальция (или сульфат кальция ) — неорганическое соединение с формулой CaSO4 и родственные ему гидраты . В форме γ- ангидрида ( безводная форма) он используется в качестве осушителя . Один конкретный гидрат более известен как алебастр , а другой встречается в природе как минеральный гипс . Он имеет множество применений в промышленности. Все формы представляют собой белые твердые вещества, которые плохо растворяются в воде. [5] Сульфат кальция вызывает постоянную жесткость воды.
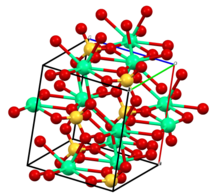
Соединение существует в трех степенях гидратации, соответствующих различным кристаллографическим структурам и минералам:
Основное применение сульфата кальция — производство алебастра и штукатурки . Эти применения используют тот факт, что сульфат кальция, который был измельчен и прокален, образует формуемую пасту при гидратации и затвердевает как кристаллический дигидрат сульфата кальция. Также удобно, что сульфат кальция плохо растворяется в воде и не растворяется легко при контакте с водой после затвердевания.
При разумном нагревании гипс превращается в частично обезвоженный минерал, называемый бассанитом или гипсом Парижа . Этот материал имеет формулу CaSO 4 ·( n H 2 O), где 0,5 ≤ n ≤ 0,8. [8] Для удаления воды из его структуры требуются температуры от 100 до 150 °C (212–302 °F). Детали температуры и времени зависят от влажности окружающей среды. При промышленной кальцинации используются температуры до 170 °C (338 °F), но при этих температурах начинает образовываться γ-ангидрит. Тепловая энергия, передаваемая гипсу в это время (тепло гидратации), имеет тенденцию идти на удаление воды (в виде водяного пара), а не на повышение температуры минерала, которая медленно поднимается до тех пор, пока вода не исчезнет, а затем увеличивается быстрее. Уравнение для частичной дегидратации имеет вид:
Эндотермическое свойство этой реакции имеет отношение к эксплуатационным характеристикам гипсокартона , придавая огнестойкость жилым и другим конструкциям. При пожаре конструкция за листом гипсокартона останется относительно холодной, поскольку вода теряется из гипса, тем самым предотвращая (или существенно замедляя) повреждение каркаса ( из-за сгорания деревянных элементов или потери прочности стали при высоких температурах) и последующее разрушение конструкции. Но при более высоких температурах сульфат кальция будет выделять кислород и действовать как окислитель . Это свойство используется в алюминотермии . В отличие от большинства минералов, которые при регидратации просто образуют жидкие или полужидкие пасты или остаются порошкообразными, кальцинированный гипс обладает необычным свойством: при смешивании с водой при нормальной (окружающей) температуре он быстро химически возвращается в предпочтительную дигидратную форму, в то время как физически «застывает», образуя жесткую и относительно прочную кристаллическую решетку гипса:
Эта реакция является экзотермической и отвечает за легкость, с которой гипс может быть отлит в различные формы, включая листы (для гипсокартона ), палочки (для школьного мела) и формы (для иммобилизации сломанных костей или для литья металла). Смешанный с полимерами, он использовался в качестве цемента для восстановления костей. Небольшие количества кальцинированного гипса добавляются в землю для создания прочных структур непосредственно из литой земли , альтернативы саману (который теряет свою прочность при намокании). Условия дегидратации можно изменять, чтобы регулировать пористость полугидрата, в результате чего получаются так называемые α- и β-полугидраты (которые более или менее химически идентичны).
При нагревании до 180 °C ( 356 °F) образуется почти безводная форма, называемая γ-ангидридом (CaSO4 · nH2O , где n = от 0 до 0,05). γ-ангидрит медленно реагирует с водой, возвращаясь в состояние дигидрата, свойство, используемое в некоторых коммерческих осушителях . При нагревании выше 250 °C образуется полностью безводная форма, называемая β-ангидридом или «природным» ангидридом . Природный ангидрит не реагирует с водой даже в геологических масштабах времени, если только он не очень тонко измельчен.
Переменный состав полугидрата и γ-ангидрида, а также их легкое взаимопревращение обусловлены их почти идентичными кристаллическими структурами, содержащими «каналы», которые могут вмещать различные количества воды или других небольших молекул, таких как метанол .
Гидраты сульфата кальция используются в качестве коагулянта в таких продуктах, как тофу . [9]
Согласно FDA , он разрешен в сыре и связанных с ним сырных продуктах; зерновой муке; хлебобулочных изделиях; замороженных десертах; искусственных подсластителях для желе и консервов; приправленных овощах; приправленных томатах и некоторых конфетах. [10]
В серии E он известен как E516 , а ФАО ООН знает его как укрепляющий агент, агент для обработки муки, секвестрант и разрыхлитель. [10]
Сульфат кальция имеет долгую историю использования в стоматологии. [11] Он использовался при регенерации костей в качестве материала для трансплантата и связующего вещества для трансплантата (или удлинителя), а также в качестве барьера при направленной регенерации костной ткани. Это биосовместимый материал, который полностью рассасывается после имплантации. [12] Он не вызывает значительной реакции хозяина и создает богатую кальцием среду в области имплантации. [13]

При продаже в безводном состоянии в качестве осушителя с цветным индикаторным агентом под названием Дриерит он имеет синий (безводный) или розовый (гидратированный) цвет из-за пропитки хлоридом кобальта(II) , который действует как индикатор влажности.
До 1970-х годов коммерческие объемы серной кислоты производились из безводного сульфата кальция. [14] При смешивании со сланцем или мергелем и обжиге при 1400°C сульфат выделяет сернистый газ, предшественник серной кислоты . В результате реакции также образуется силикат кальция , используемый в производстве цементного клинкера . [15] [16]
Некоторые реакции компонентов, относящиеся к сульфату кальция:
Основными источниками сульфата кальция являются природный гипс и ангидрит , которые встречаются во многих местах по всему миру в виде эвапоритов . Их можно добывать открытым способом или путем глубокой разработки. Мировое производство природного гипса составляет около 127 миллионов тонн в год. [17]
Помимо природных источников, сульфат кальция производится как побочный продукт в ряде процессов:
В схожих методах улавливания серы используется известь , а некоторые из них приводят к образованию неочищенного сульфита кальция , который при хранении окисляется до сульфата кальция.
Эти процессы осаждения имеют тенденцию концентрировать радиоактивные элементы в продукте сульфата кальция. Эта проблема особенно актуальна для побочного продукта фосфата, поскольку фосфатные руды естественным образом содержат уран и продукты его распада, такие как радий-226 , свинец-210 и полоний-210 . Извлечение урана из фосфорных руд может быть экономичным само по себе в зависимости от цен на рынке урана , или же разделение урана может быть предписано экологическим законодательством, а его продажа используется для возмещения части стоимости процесса. [19] [20] [21]
Сульфат кальция также является распространенным компонентом отложений в промышленных теплообменниках, поскольку его растворимость уменьшается с повышением температуры (см. специальный раздел о ретроградной растворимости).

Растворимость сульфата кальция уменьшается с ростом температуры. Такое поведение («ретроградная растворимость») встречается нечасто: растворение большинства солей эндотермично , и их растворимость увеличивается с температурой.Ретроградная растворимость сульфата кальция также отвечает за его осаждение в самой горячей зоне систем отопления и за его вклад в образование накипи в котлах вместе с осаждением карбоната кальция , растворимость которого также уменьшается, когда CO2 дегазируется из горячей воды или может выйти из системы.