Ацетилацетон представляет собой органическое соединение с химической формулой CH 3 -C(=O)-CH 2 -C(=O)-CH 3 . Его классифицируют как 1,3- дикетон . Он существует в равновесии с таутомером CH 3 -C(=O)-CH=C(-OH)-CH 3 . Смесь представляет собой бесцветную жидкость. Эти таутомеры в большинстве случаев взаимопревращаются так быстро, что в большинстве случаев их рассматривают как одно соединение. [2] Ацетилацетон является строительным блоком для синтеза многих координационных комплексов , а также гетероциклических соединений .
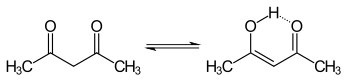
Кето- и енольные таутомеры ацетилацетона сосуществуют в растворе. Енольная форма имеет симметрию C2v , что означает, что атом водорода поровну разделен между двумя атомами кислорода. [4] В газовой фазе константа равновесия K кето→енол равна 11,7, что соответствует енольной форме. Две таутомерные формы можно различить с помощью ЯМР-спектроскопии , ИК-спектроскопии и других методов. [5] [6]
Константа равновесия имеет тенденцию быть высокой в неполярных растворителях; когда K кето→енол равен или больше 1, енольная форма является предпочтительной. Кето-форма становится более предпочтительной в полярных растворителях с водородными связями, таких как вода. [7] Енольная форма является винилологичным аналогом карбоновой кислоты .
Ацетилацетон — слабая кислота . Образует ацетилацетонат- анион C 5 H 7 O.−2(обычно сокращенно acac − ):

В ацетилацетонат-анионе обе связи С - О эквивалентны. Обе центральные связи CC также эквивалентны: один атом водорода связан с центральным атомом углерода ( атомом C3 ). Эти две эквивалентности возникают потому, что существует резонанс между четырьмя связями в связи O-C2-C3-C4-O в ацетилацетонат-анионе, где порядок этих четырех связей составляет около 1,5. Оба атома кислорода в равной степени разделяют отрицательный заряд . Ацетилацетонат-анион является бидентатным лигандом .
Рекомендуемые ИЮПАК значения p K a для этого равновесия в водном растворе при 25 °C составляют 8,99 ± 0,04 ( I = 0), 8,83 ± 0,02 ( I = 0,1 М NaClO 4 ) и 9,00 ± 0,03 ( I = 1,0 М NaClO 4 ; I) . = Ионная сила ). [9] Доступны значения для смешанных растворителей. Очень сильные основания , такие как литийорганические соединения, дважды депротонируют ацетилацетон. Полученные частицы дилития затем могут быть алкилированы по атому углерода в положении 1 .
Ацетилацетон получают в промышленности термической перегруппировкой изопропенилацетата . [10]
Лабораторные пути получения ацетилацетона также начинаются с ацетона . Ацетон и уксусный ангидрид ( (CH 3 C(O)) 2 O ) при добавлении катализатора трифторида бора ( BF 3 ): [11]
Второй синтез включает катализируемую основанием конденсацию (например, этоксидом натрия CH 3 CH 2 O - Na + ) ацетона и этилацетата с последующим подкислением ацетилацетоната натрия (например, хлористым водородом HCl): [11]
Из-за простоты такого синтеза известно множество аналогов ацетилацетонатов. Некоторыми примерами являются бензоилацетон , дибензоилметан (dbaH) [ необходимы пояснения ] и трет -бутильный аналог 2,2,6,6-тетраметил-3,5-гептандион. Трифторацетилацетон и гексафторацетилацетонат также используются для образования летучих комплексов металлов .
Ацетилацетон является универсальным бифункциональным предшественником гетероциклов, поскольку обе кетогруппы могут подвергаться конденсации . Например, конденсация с гидразином дает пиразолы , а конденсация с мочевиной дает пиримидины . Конденсация с двумя арил- или алкиламинами дает NacNacs , в котором атомы кислорода в ацетилацетоне заменены на NR (R = арил, алкил).
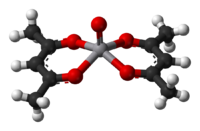
Ацетилацетонат натрия Na(acac) является предшественником многих ацетилацетонатных комплексов . Общий метод синтеза заключается в обработке соли металла ацетилацетоном в присутствии основания : [ 12]
Оба атома кислорода связываются с металлом, образуя шестичленное хелатное кольцо. В некоторых случаях хелатный эффект настолько силен, что для образования комплекса не требуется добавление основания.
Фермент ацетилацетондиоксигеназа расщепляет углерод-углеродную связь ацетилацетона с образованием ацетата и 2-оксопропаналя . Фермент является железо(II) -зависимым, но доказано, что он также связывается с цинком . Деградация ацетилацетона была охарактеризована у бактерии Acinetobacter johnsonii . [13]
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )