В металлоорганической химии литийорганические реагенты — химические соединения , содержащие связи углерод — литий (C—Li) . Эти реагенты важны в органическом синтезе и часто используются для переноса органической группы или атома лития на субстраты на стадиях синтеза посредством нуклеофильного присоединения или простого депротонирования . [1] Литийорганические реагенты используются в промышленности в качестве инициатора анионной полимеризации , что приводит к производству различных эластомеров . Они также нашли применение в асимметричном синтезе в фармацевтической промышленности. [2] Из-за большой разницы в электроотрицательности между атомом углерода и атомом лития связь C-Li является высокоионной . Благодаря полярной природе связи C-Li литийорганические реагенты являются хорошими нуклеофилами и сильными основаниями. Для лабораторного органического синтеза многие литийорганические реагенты коммерчески доступны в виде растворов. Эти реагенты высокореактивны, а иногда и пирофорны .


Исследования литийорганических реагентов начались в 1930-х годах и были впервые осуществлены Карлом Циглером , Георгом Виттигом и Генри Гилманом . По сравнению с реагентами Гриньяра (магний) литийорганические реагенты часто могут проводить те же реакции с повышенной скоростью и более высокими выходами, например, в случае металлирования . [3] С тех пор литийорганические реагенты в общем использовании обогнали реактивы Гриньяра. [4]
Хотя простые формы алкиллития часто представлены в виде мономера RLi, они существуют в виде агрегатов ( олигомеров ) или полимеров. [5] Степень агрегации зависит от органического заместителя и присутствия других лигандов. [6] [7] Эти структуры были выяснены различными методами, в частности 6 Li, 7 Li и 13 C ЯМР-спектроскопией и рентгеноструктурным анализом. [1] Вычислительная химия поддерживает эти задания. [5]

Относительная электроотрицательность углерода и лития предполагает, что связь C-Li будет высокополярной. [8] [9] [10] Однако некоторые литийорганические соединения обладают такими свойствами, как растворимость в неполярных растворителях, которые усложняют проблему.[8] Хотя большинство данных показывают, что связь C-Li по существу ионная, ведутся споры о том, насколько в ней существует ковалентный характер. [9] [10] По одной из оценок, процент ионного характера соединений алкиллития составляет от 80 до 88%. [11]
В соединениях аллиллития катион лития координируется с поверхностью π-связи углерода по образцу η 3 вместо локализованного карбанионного центра, таким образом, аллиллитий часто менее агрегирован, чем алкиллитий. [6] [12] В комплексах ариллития катион лития координируется с одним карбанионным центром через связь типа Li-C σ. [6] [13]
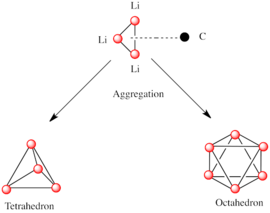
Как и другие виды, состоящие из полярных субъединиц, литийорганические виды агрегируют. [7] [14] На образование агрегатов влияют электростатические взаимодействия, координация между литием и окружающими молекулами растворителя или полярными добавками, а также стерические эффекты. [7]
Основным строительным блоком для построения более сложных структур является карбанионный центр, взаимодействующий с треугольником Li 3 по схеме η 3 -. [5] В простых алкиллитиевых реагентах эти треугольники объединяются, образуя структуры тетраэдра или октаэдра. Например, метиллитий , этиллитий и трет -бутиллитий существуют в тетрамере [RLi] 4 . Метиллитий существует в виде тетрамеров в кластере кубанового типа в твердом состоянии, с четырьмя литиевыми центрами, образующими тетраэдр. Каждый метанид в тетрамере в метиллитии может вступать в агостическое взаимодействие с катионами лития в соседних тетрамерах. [5] [7] Этиллитий и трет -бутиллитий, с другой стороны, не проявляют этого взаимодействия и, таким образом, растворимы в неполярных углеводородных растворителях. Другой класс алкиллития имеет гексамерные структуры, такие как н -бутиллитий , изопропиллитий и циклогексаниллитий. [5]
Обычные амиды лития, например бис(триметилсилил)амид лития и диизопропиламид лития , также подвержены агрегации. [15] Амиды лития принимают структуры типа полимерной лестницы в некоординационном растворителе в твердом состоянии и обычно существуют в виде димеров в эфирных растворителях. В присутствии сильнодонорных лигандов образуются три- или тетрамерные литиевые центры. [16] Например, ЛДА существует в основном в виде димеров в ТГФ. [15] Структуры обычных амидов лития, таких как диизопропиламид лития (LDA) и гексаметилдисилазид лития (LiHMDS), были тщательно изучены Коллумом и его коллегами с использованием ЯМР-спектроскопии . [17] Другим важным классом реагентов являются силиллитии, широко используемые в синтезе металлоорганических комплексов и полисилановых дендримеров . [7] [18] В твердом состоянии, в отличие от алкиллитиевых реагентов, большинство силиллитий имеют тенденцию образовывать мономерные структуры, координированные с молекулами растворителя, такими как ТГФ, и лишь несколько силиллитий были охарактеризованы как высшие агрегаты. [7] Это различие может быть связано с методом получения силиллития, стерическими затруднениями, вызванными объемистыми алкильными заместителями на кремнии, и менее поляризованной природой связей Si-Li. Добавление сильнодонорных лигандов, таких как TMEDA и (-)- спартеин , может вытеснять координирующие молекулы растворителя в силиллитии. [7]
Литийорганические реагенты могут иметь в растворе структуры, отличные от твердого состояния. [6] [19] ЯМР-спектроскопия стала мощным инструментом для изучения литийорганических агрегатов в растворе. Для разновидностей алкиллития сочетание C-Li J часто можно использовать для определения количества лития, взаимодействующего с карбанионным центром, а также того, являются ли эти взаимодействия статическими или динамическими. [6] Отдельные сигналы ЯМР также позволяют отличить наличие нескольких агрегатов от общей мономерной единицы. [20]
Литийорганические соединения связывают основания Льюиса, такие как тетрагидрофуран (THF), диэтиловый эфир (Et 2 O), тетраметилэтилендиамин (TMEDA) или гексаметилфосфорамид (HMPA). [5] Метиллитий представляет собой особый случай: на его тетрамерную структуру не влияет эфир или даже HMPA. [7] С другой стороны, ТГФ деагрегирует гексамерный бутиллитий: тетрамер является основным типом, а ΔG для взаимного превращения между тетрамером и димером составляет около 11 ккал/моль. [21] TMEDA может также хелатировать катионы лития в н -бутиллитии и образовывать сольватированные димеры, такие как [(TMEDA) LiBu-n)] 2 . [5] [6] Было показано, что фениллитий существует в виде искаженного тетрамера в кристаллизованном эфирном сольвате и в виде смеси димера и тетрамера в эфирном растворе. [6]
Поскольку структура литийорганических реагентов меняется в зависимости от их химического окружения, изменяются также их реакционная способность и селективность. [7] [22] Один из вопросов, связанных со связью структура-реакционная способность, заключается в том, существует ли корреляция между степенью агрегации и реакционной способностью литийорганических реагентов. Первоначально предполагалось, что низшие агрегаты, такие как мономеры, более реакционноспособны по отношению к алкиллитию. [23] Однако также были обнаружены пути реакции, в которых димеры или другие олигомеры являются реакционноспособными частицами, [24] и для амидов лития, таких как LDA, реакции на основе димеров являются обычным явлением. [25] Ряд исследований кинетики растворения реакций, опосредованных LDA, показывают, что более низкие агрегаты енолятов не обязательно приводят к более высокой реакционной способности. [17]
Кроме того, некоторые основания Льюиса повышают реакционную способность литийорганических соединений. [26] [27] Однако не всегда ясно, действуют ли эти добавки как сильные хелатирующие лиганды и как наблюдаемое увеличение реакционной способности связано со структурными изменениями в агрегатах, вызванными этими добавками. [26] [27] Например, TMEDA увеличивает скорость и эффективность многих реакций с участием литийорганических реагентов. [7] По отношению к алкиллитиевым реагентам TMEDA действует как донорный лиганд, снижает степень агрегации [5] и увеличивает нуклеофильность этих частиц. [28] Однако TMEDA не всегда действует как донорный лиганд катиона лития, особенно в присутствии анионных кислородных и азотных центров. Например, он лишь слабо взаимодействует с ЛДА и LiHMDS даже в углеводородных растворителях без конкурирующих донорных лигандов. [29] При иминном литиировании, в то время как ТГФ действует как сильный донорный лиганд для LiHMDS, слабокоординирующий TMEDA легко диссоциирует от LiHMDS, что приводит к образованию димеров LiHMDS, которые являются более реакционноспособными видами. Таким образом, в случае LiHMDS TMEDA не увеличивает реакционную способность за счет снижения агрегатного состояния. [30] Кроме того, в отличие от простых соединений алкиллития, TMEDA не деагрегирует литиоацетофенолят в растворе ТГФ. [6] [31] Добавление HMPA к амидам лития, таким как LiHMDS и LDA, часто приводит к образованию смеси агрегатов димера/мономера в ТГФ. Однако соотношение видов димер/мономер не меняется с увеличением концентрации ГМПА, поэтому наблюдаемое увеличение реакционной способности не является результатом дезагрегации. Механизм повышения реакционной способности этих добавок все еще исследуется. [22]
Связь C–Li в литийорганических реагентах сильно поляризована. В результате углерод притягивает большую часть электронной плотности в связи и напоминает карбанион. Таким образом, литийорганические реагенты являются сильноосновными и нуклеофильными. Некоторые из наиболее распространенных применений литийорганических реагентов в синтезе включают их использование в качестве нуклеофилов, сильных оснований для депротонирования, инициатора полимеризации и исходного материала для получения других металлоорганических соединений.
Будучи нуклеофилами, литийорганические реагенты подвергаются реакциям карболитирования, в ходе которых связь углерод-литий присоединяется к двойной или тройной связи углерод - углерод, образуя новые литийорганические виды. [32] Эта реакция является наиболее широко используемой реакцией литийорганических соединений. Карболитирование является ключевым моментом в процессах анионной полимеризации, а н -бутиллитий используется в качестве катализатора для инициации полимеризации стирола , бутадиена или изопрена или их смесей. [33] [34]
Другое применение, в котором используется эта реакционная способность, - это образование карбоциклических и гетероциклических соединений путем внутримолекулярного карболитирования. [32] Как форма анионной циклизации, реакции внутримолекулярного карболитирования имеют ряд преимуществ перед радикальной циклизацией . Во-первых, образующиеся циклические литийорганические соединения могут вступать в реакцию с электрофилами, тогда как уловить радикальный интермедиат соответствующей структуры часто бывает трудно. Во-вторых, анионные циклизации часто более регио- и стереоспецифичны, чем радикальная циклизация, особенно в случае 5-гексениллития. Внутримолекулярное карболитирование позволяет присоединить алкил-, виниллитий к тройным связям и моноалкилзамещенным двойным связям. Ариллитий также может подвергаться присоединению, если образуется 5-членное кольцо. Ограничения внутримолекулярного карболитирования включают трудность образования 3- или 4-членных колец, поскольку промежуточные циклические литийорганические соединения часто имеют тенденцию подвергаться раскрытию кольца. [32] Ниже приведен пример реакции внутримолекулярного карболитирования. Разновидности лития, полученные в результате обмена литий-галоген, циклизуются с образованием виниллития посредством замыкания 5-экзо-триг-кольца. Виды виниллития далее реагируют с электрофилами и образуют функционализированные циклопентилиденовые соединения. [35]
Нуклеофильные литийорганические реагенты могут присоединяться к электрофильным карбонильным двойным связям с образованием связей углерод - углерод. Они могут реагировать с альдегидами и кетонами с образованием спиртов . Присоединение происходит в основном посредством полярного присоединения, при котором нуклеофильные литийорганические соединения атакуют с экваториального направления и образуют аксиальный спирт. [36] Добавление солей лития, таких как LiClO 4 , может улучшить стереоселективность реакции. [37]
Когда кетон стерически затруднен, использование реактивов Гриньяра часто приводит к восстановлению карбонильной группы вместо присоединения. [36] Однако алкиллитиевые реагенты с меньшей вероятностью восстанавливают кетон и могут использоваться для синтеза замещенных спиртов. [38] Ниже приведен пример добавления этиллития к адамантону для получения третичного спирта. [39]
Литийорганические реагенты также превосходят реактивы Гриньяра по способности вступать в реакцию с карбоновыми кислотами с образованием кетонов. [36] Эту реакцию можно оптимизировать, тщательно контролируя количество добавляемого литийорганического реагента или используя триметилсилилхлорид для гашения избытка литиевого реагента. [40] Более распространенный способ синтеза кетонов — добавление литийорганических реагентов к амидам Вейнреба ( N -метокси- N -метиламиды). Эта реакция дает кетоны, когда литийорганические реагенты используются в избытке, из-за хелатирования иона лития между N -метоксикислородом и карбонильным кислородом, который образует тетраэдрический промежуточный продукт, который разрушается при кислотной обработке. [41]
Литийорганические реагенты также реагируют с диоксидом углерода с образованием после обработки карбоновых кислот . [42]
В случае еноновых субстратов, где возможны два центра нуклеофильного присоединения (1,2-присоединение к карбонильному углероду или 1,4- сопряженное присоединение к β-углероду), большинство высокореакционноспособных литийорганических форм благоприятствуют 1,2-присоединению, однако Существует несколько способов заставить литийорганические реагенты подвергнуться конъюгатному присоединению. Во-первых, поскольку 1,4-аддукт, вероятно, будет более термодинамически выгодным, присоединение конъюгата может быть достигнуто путем уравновешивания (изомеризации двух продуктов), особенно когда нуклеофил лития слабый и присоединение 1,2 обратимо. Во-вторых, добавление донорных лигандов в реакцию образует стабилизированные гетероатомами частицы лития, что способствует присоединению 1,4-конъюгата. В одном примере добавление небольшого количества HMPA к растворителю благоприятствует добавлению 1,4. В отсутствие донорного лиганда катион лития тесно координирован с атомом кислорода, однако при сольватации катиона лития ГМПА координация между карбонильным кислородом и ионом лития ослабляется. Этот метод, как правило, не может быть использован для воздействия на региоселективность алкил- и ариллитиевых реагентов. [43] [44]
Литийорганические реагенты также могут осуществлять энантиоселективное нуклеофильное присоединение к карбонилу и его производным, часто в присутствии хиральных лигандов. Эта реакционная способность широко применяется в промышленном синтезе фармацевтических соединений. Примером является синтез компанией Merck и Dupont эфавиренца , мощного ингибитора обратной транскриптазы ВИЧ . Ацетилид лития добавляют к прохиральному кетону с получением хирального спиртового продукта. Методами ЯМР-спектроскопии в растворенном состоянии и рентгеноструктурной кристаллографии твердого состояния установлено строение активного интермедиата реакции: кубический тетрамер 2:2. [45]
Литийорганические реагенты могут служить нуклеофилами и осуществлять реакции типа SN 2 с алкил- или аллилгалогенидами. [46] Хотя они считаются более реакционноспособными, чем реактивы Гриньяра при алкилировании, их использование по-прежнему ограничено из-за конкурирующих побочных реакций, таких как радикальные реакции или обмен металл - галоген. Большинство литийорганических реагентов, используемых при алкилировании, более стабилизированы, менее основные и менее агрегированные, например, стабилизированные гетероатомами арил- или аллиллитиевые реагенты. [6] Было показано, что HMPA увеличивает скорость реакции и выход продукта, а реакционная способность ариллитиевых реагентов часто повышается за счет добавления алкоксидов калия. [36] Литийорганические реагенты также могут осуществлять нуклеофильную атаку эпоксидов с образованием спиртов.
Литийорганические реагенты обеспечивают широкий диапазон основности . Трет -Бутиллитий с тремя слабоэлектронодонорными алкильными группами является самым сильным коммерчески доступным основанием ( pKa = 53). В результате кислые протоны на -OH, -NH и -SH часто защищены в присутствии литийорганических реагентов. Некоторые обычно используемые литиевые основания представляют собой разновидности алкиллития, такие как н -бутиллитий и диалкиламиды лития (LiNR 2 ). Реагенты с объемистыми группами R, такие как диизопропиламид лития (LDA) и бис(триметилсилил)амид лития (LiHMDS), часто стерически затруднены для нуклеофильного присоединения и, следовательно, более селективны в отношении депротонирования. Диалкиламиды лития (LiNR 2 ) широко используются в образовании енолятов и альдольных реакциях. [47] На реакционную способность и селективность этих оснований также влияют растворители и другие противоионы.
Металлирование литийорганическими реагентами, также известное как литирование или литий-водородный обмен, достигается, когда литийорганический реагент, чаще всего алкиллитий, отрывает протон и образует новую литийорганическую разновидность.
Обычными реагентами металлирования являются бутиллитий. трет -бутиллитий и втор -бутиллитий обычно более реакционноспособны и обладают лучшей селективностью, чем н -бутиллитий, однако они также более дороги и с ними труднее обращаться. [47] Металлирование является распространенным способом приготовления универсальных литийорганических реагентов. Положение металлирования в основном контролируется кислотностью связи CH. Литиирование часто происходит в положении α электроноакцепторных групп, поскольку они хорошо стабилизируют электронную плотность аниона. Направляющие группы ароматических соединений и гетероциклов обеспечивают региоселективные центры металлирования; направленное орто-металлирование - важный класс реакций металлирования. Металлированные сульфоны, ацильные группы и α-металлированные амиды являются важными промежуточными соединениями в химическом синтезе. Металлирование аллилового эфира алкиллитием или LDA образует анион α по отношению к кислороду и может перейти к перегруппировке 2,3-Виттига . Добавление донорных лигандов, таких как TMEDA и HMPA, может увеличить скорость металлирования и расширить область применения субстратов. [48] Доступ к хиральным литийорганическим реагентам можно получить посредством асимметричного металлирования. [49]
Направленное орто-металлирование является важным инструментом в синтезе региоспецифических замещенных ароматических соединений. Этот подход к литиированию и последующему охлаждению промежуточных частиц лития электрофилом часто оказывается лучше, чем электрофильное ароматическое замещение из-за его высокой региоселективности. Эта реакция протекает путем депротонирования литийорганическими реагентами в положениях α до группы прямого металлирования (ДМГ) ароматического кольца. DMG часто представляет собой функциональную группу, содержащую гетероатом , который является основным по Льюису и может координироваться с кислотным катионом лития по Льюису. Это создает комплексно-индуцированный эффект близости, который направляет депротонирование в α-положении с образованием разновидностей ариллития, которые могут в дальнейшем реагировать с электрофилами. Некоторые из наиболее эффективных DMG — амиды, карбаматы , сульфоны и сульфонамиды . Это сильные электроноакцепторные группы, которые повышают кислотность альфа-протонов ароматического кольца. При наличии двух ДМГ металлирование часто происходит орто более сильной направляющей группы, хотя наблюдаются и смешанные продукты. Ряд гетероциклов, содержащих кислые протоны, также могут подвергаться орто-металлированию. Однако для бедных электронами гетероциклов обычно используются основания амида лития, такие как LDA, поскольку наблюдалось, что алкиллитий осуществляет присоединение к бедным электронами гетероциклам, а не депротонирование. В некоторых комплексах переходный металл-арен, таких как ферроцен , переходный металл притягивает электронную плотность от арена, тем самым делая ароматические протоны более кислыми и готовыми к орто-металлированию. [50]
Добавление алкоксида калия к алкиллитию значительно увеличивает основность литийорганических соединений. [51] Наиболее распространенное «супероснование» может быть образовано добавлением KOtBu к бутиллитию, часто называемому реагентами «LiCKOR». Эти «супероснования» являются высокореактивными и часто стереоселективными реагентами. В приведенном ниже примере основание LiCKOR генерирует стереоспецифические виды кротилбороната посредством металлирования и последующего литий-металлоидного обмена. [52]
Энантиообогащенные литийорганические виды можно получить путем асимметричного металлирования прохиральных субстратов. Асимметричная индукция требует присутствия хирального лиганда, такого как (-)- спартеин . [49] На энантиомерное соотношение хиральных видов лития часто влияют различия в скорости депротонирования. В приведенном ниже примере обработка N -Boc- N -бензиламина н -бутиллитием в присутствии (-)-спартеина дает один энантиомер продукта с высоким энантиомерным избытком . Трансметаллирование триметилоловохлоридом дает противоположный энантиомер. [53]
Еноляты лития образуются в результате депротонирования связи CH α с карбонильной группой литийорганическими соединениями. Еноляты лития широко используются в качестве нуклеофилов в реакциях образования углерод - углеродных связей, таких как альдольная конденсация и алкилирование. Они также являются важным промежуточным продуктом в образовании эфира силиленола .
Образование енолята лития можно обобщить как кислотно - основную реакцию, в которой относительно кислый протон α карбонильной группы (pK =20-28 в ДМСО) реагирует с литийорганическим основанием. Обычно используются сильные ненуклеофильные основания, особенно амиды лития, такие как LDA, LiHMDS и LiTMP. ТГФ и ДМСО являются обычными растворителями в реакциях енолята лития. [54]
Стереохимия и механизм образования енолятов вызвали большой интерес в химическом сообществе. На результат стереохимии енолята влияют многие факторы, такие как стерические эффекты, растворитель, полярные добавки и типы литийорганических оснований. Среди многих моделей, используемых для объяснения и прогнозирования селективности стереохимии енолятов лития, есть модель Ирландии. [55]
В этом предположении мономерный ЛДА реагирует с карбонильным субстратом и образует переходное состояние циклического типа Циммермана-Тракслера. (E)-енолят является предпочтительным из-за неблагоприятного взаимодействия синпентана в переходном состоянии (Z)-енолята. [54]

Добавление полярных добавок, таких как HMPA или DMPU, способствует образованию (Z)-енолятов. Модель Ирландии утверждает, что эти донорные лиганды координируются с катионами лития, в результате чего взаимодействие карбонильного кислорода и лития уменьшается, и переходное состояние не так прочно связано, как шестичленный стул. Процент енолятов (Z) также увеличивается при использовании литиевых оснований с более объемными боковыми цепями (таких как LiHMDS). [54] Однако механизм того, как эти добавки меняют стереоселективность, все еще обсуждается.
Модель Ирландии столкнулась с некоторыми проблемами, поскольку она изображает виды лития как мономеры в переходном состоянии. В действительности в растворах енолятов лития часто наблюдаются разнообразные агрегаты лития, и в зависимости от конкретного субстрата, растворителя и условий реакции может быть трудно определить, какой агрегат является фактическим химически активным веществом в растворе. [54]
Литий-галогеновый обмен включает обмен гетероатомами между галогенидами и литийорганическими соединениями.
Литий-галогеновый обмен очень полезен при получении новых литийорганических реагентов. Применение литий-галогенного обмена иллюстрируется циклизацией Пархема. [56]
Литийорганические реагенты часто используются для получения других металлоорганических соединений методом трансметаллирования. Медьорганические, оловоорганические , кремнийорганические, борорганические, фосфорорганические, церийорганические и сероорганические соединения часто получают путем взаимодействия литийорганических реагентов с соответствующими электрофилами.
Общие типы трансметаллирования включают обмен Li/Sn, Li/Hg и Li/Te, который протекает быстро при низкой температуре. [47] Преимущество обмена Li/Sn заключается в том, что предшественники три-алкилстаннана подвергаются небольшому количеству побочных реакций, поскольку образующиеся побочные продукты n-Bu 3 Sn нереакционноспособны по отношению к алкиллитиевым реагентам. [47] В следующем примере винилстаннан, полученный гидростаннилированием концевого алкина, образует виниллитий посредством трансметаллирования с n-BuLi. [57]
Литийорганический элемент также может быть использован для получения цинкорганических соединений путем трансметаллирования солями цинка. [58]
Диорганокупраты лития могут быть образованы путем реакции алкиллитиевых форм с галогенидом меди (I). Полученные органокупраты обычно менее реакционноспособны по отношению к альдегидам и кетонам, чем литийорганические реагенты или реактивы Гриньяра. [59]
Большинство простых алкиллитиевых реагентов и обычные амиды лития коммерчески доступны в различных растворителях и концентрациях. Литийорганические реагенты также можно приготовить в лаборатории. Ниже приведены некоторые распространенные методы приготовления литийорганических реагентов.
Восстановление алкилгалогенида металлическим литием может дать простые алкил- и арилорганические реагенты. [36]
Промышленное получение литийорганических реагентов этим методом достигается обработкой алкилхлорида металлическим литием, содержащим 0,5-2 % натрия . Превращение является сильно экзотермическим . Натрий инициирует радикальный путь и увеличивает скорость. [60] Восстановление происходит по радикальному пути. Ниже приведен пример приготовления функционализированного литиевого реагента с использованием восстановления металлическим литием. [61] Иногда металлический литий в виде мелкодисперсных порошков используется в реакции с некоторыми катализаторами, такими как нафталин или 4,4'-ди-т-бутилбифенил (DTBB). Другим субстратом, который можно восстановить металлическим литием для получения алкиллитиевых реагентов, являются сульфиды. Восстановление сульфидов полезно при образовании функционализированных литийорганических реагентов, таких как альфа-литиоэфиры, сульфиды и силаны. [62]
Второй метод приготовления литийорганических реагентов — металлирование (литий-водородный обмен). Относительная кислотность атомов водорода контролирует положение литиирования.
Это наиболее распространенный метод приготовления алкиниллитиевых реагентов, поскольку концевой водород, связанный с sp- углеродом, очень кислый и легко депротонируется. [36] Для ароматических соединений положение литиирования также определяется направляющим действием заместителей. [63] Некоторые из наиболее эффективных направляющих групп-заместителей представляют собой алкокси, амидо, сульфоксид, сульфонил. Металлирование часто происходит в орто-положении к этим заместителям. В гетероароматических соединениях металлирование обычно происходит в орто-положении по отношению к гетероатому. [36] [63]
См. Обмен литий-галоген (в разделе «Реакционная способность и применение»).
Третий метод приготовления литийорганических реагентов - обмен лития на галоген.
трет- бутиллитий или н- бутиллитий являются наиболее часто используемыми реагентами для получения новых литийорганических соединений путем обмена лития на галоген. Литий-галогеновый обмен чаще всего используют для превращения арил- и алкенилиодидов и бромидов с атомами углерода sp2 в соответствующие литийорганические соединения. Реакция протекает чрезвычайно быстро и часто протекает при температуре от -60 до -120 ° C. [48]
Четвертый метод получения литийорганических реагентов — трансметаллирование. Этот метод можно использовать для получения виниллития.
В реакции Шапиро два эквивалента сильного алкиллитиевого основания реагируют с соединениями п-тозилгидразона с образованием виниллития или после гашения олефинового продукта.
Литийорганические соединения являются высокореактивными соединениями и требуют специальных методов обращения. Они часто коррозионны, легковоспламеняемы, а иногда и пирофорны (самопроизвольное возгорание при воздействии воздуха или влаги). [64] Алкиллитиевые реагенты также могут подвергаться термическому разложению с образованием соответствующих алкильных разновидностей и гидрида лития. [65] Литийорганические реагенты обычно хранятся при температуре ниже 10 °C. Реакции проводят безвоздушными методами . [64] Концентрацию алкиллитиевых реагентов часто определяют методом титрования . [66] [67] [68]
Литийорганические реагенты реагируют, часто медленно, с простыми эфирами, которые, тем не менее, часто используются в качестве растворителей. [69]