
Электроотрицательность , обозначаемая как χ , представляет собой тенденцию атома данного химического элемента притягивать общие электроны (или электронную плотность ) при образовании химической связи . [1] На электроотрицательность атома влияет как его атомный номер , так и расстояние, на котором его валентные электроны находятся от заряженного ядра. Чем выше связанная электроотрицательность, тем больше атом или группа заместителя притягивает электроны. Электроотрицательность служит простым способом количественной оценки энергии связи , а также знака и величины химической полярности связи , которая характеризует связь в непрерывном масштабе от ковалентной до ионной связи . Свободно определенный термин электроположительность является противоположностью электроотрицательности: он характеризует склонность элемента отдавать валентные электроны.
На самом базовом уровне электроотрицательность определяется такими факторами, как заряд ядра (чем больше протонов имеет атом, тем большее «притяжение» он оказывает на электроны), а также количество и расположение других электронов в атомных оболочках (чем больше электронов находится в атомных оболочках). имеет атом, тем дальше от ядра будут находиться валентные электроны и, как следствие, тем меньший положительный заряд они будут испытывать - как из-за их увеличенного расстояния от ядра, так и из-за того, что другие электроны на орбиталях ядра с более низкой энергией будут действовать для защиты валентных электронов от положительно заряженного ядра).
Термин «электроотрицательность» был введен Йонсом Якобом Берцелиусом в 1811 году [2] , хотя это понятие было известно и раньше и изучалось многими химиками, включая Авогадро . [2] Несмотря на свою долгую историю, точная шкала электроотрицательности не была разработана до 1932 года, когда Лайнус Полинг предложил шкалу электроотрицательности, которая зависит от энергии связи, как развитие теории валентных связей . [3] Было показано, что он коррелирует с рядом других химических свойств. Электроотрицательность не может быть измерена напрямую и должна рассчитываться на основе других атомных или молекулярных свойств. Было предложено несколько методов расчета, и хотя в числовых значениях электроотрицательности могут быть небольшие различия, все методы показывают одни и те же периодические тенденции между элементами . [4]
Наиболее часто используемый метод расчета — метод, первоначально предложенный Лайнусом Полингом. Это дает безразмерную величину , обычно называемую шкалой Полинга ( χr ), в относительной шкале от 0,79 до 3,98 ( водород = 2,20). При использовании других методов расчета принято (хотя и не обязательно) приводить результаты в шкале, охватывающей тот же диапазон числовых значений: это известно как электроотрицательность в единицах Полинга .
Как обычно рассчитывают, электроотрицательность — это не свойство только атома, а скорее свойство атома в молекуле . [5] Несмотря на это, электроотрицательность атома сильно коррелирует с первой энергией ионизации . Электроотрицательность слегка отрицательно коррелирует (для меньших значений электроотрицательности) и довольно сильно положительно коррелирует (для большинства и больших значений электроотрицательности) со сродством к электрону . [6] Следует ожидать, что электроотрицательность элемента будет меняться в зависимости от его химического окружения, [7] но обычно считается, что это передаваемое свойство , то есть одинаковые значения будут действительны в различных ситуациях. .
Цезий — наименее электроотрицательный элемент (0,79); фтора больше всего (3,98).
Полинг впервые предложил [3] концепцию электроотрицательности в 1932 году, чтобы объяснить, почему ковалентная связь между двумя разными атомами (A–B) прочнее, чем среднее значение связей A–A и B–B. Согласно теории валентной связи , видным сторонником которой был Полинг, эта «дополнительная стабилизация» гетероядерной связи происходит за счет вклада в связь ионных канонических форм .
Разница в электроотрицательности между атомами A и B определяется выражением:
Поскольку определяются только различия в электроотрицательности, для построения шкалы необходимо выбрать произвольную точку отсчета. В качестве эталона был выбран водород, поскольку он образует ковалентные связи с большим разнообразием элементов: его электроотрицательность была зафиксирована сначала [3] на уровне 2,1, позже пересмотрена [8] до 2,20. Также необходимо решить, какой из двух элементов более электроотрицательный (что эквивалентно выбору одного из двух возможных знаков квадратного корня). Обычно это делается с помощью «химической интуиции»: в приведенном выше примере бромоводород растворяется в воде с образованием ионов H + и Br- , поэтому можно предположить, что бром более электроотрицательен, чем водород. Однако в принципе, поскольку для любых двух связующих соединений должна быть получена одинаковая электроотрицательность, данные фактически переопределены, и знаки уникальны, как только опорная точка определена (обычно для H или F).
Для расчета электроотрицательности Полинга элемента необходимо иметь данные об энергиях диссоциации как минимум двух типов ковалентных связей, образуемых этим элементом. А. Л. Оллред обновил исходные значения Полинга в 1961 году, чтобы принять во внимание большую доступность термодинамических данных [8] , и именно эти «пересмотренные Полинговские» значения электроотрицательности используются чаще всего.
Существенным моментом электроотрицательности Полинга является то, что существует основная, довольно точная, полуэмпирическая формула для энергий диссоциации, а именно:
Это приблизительные уравнения, но они выполняются с хорошей точностью. Полинг получил первое уравнение, отметив, что связь можно приближенно представить как квантовомеханическую суперпозицию ковалентной связи и двух ионных состояний связи. Ковалентная энергия связи, согласно квантово-механическим расчетам, является приблизительным средним геометрическим двух энергий ковалентных связей одних и тех же молекул, и существует дополнительная энергия, обусловленная ионными факторами, т.е. полярным характером связи.
Среднее геометрическое примерно равно среднему арифметическому , которое применяется в первой формуле выше, когда энергии имеют одинаковое значение, например, за исключением сильно электроположительных элементов, где существует большая разница в две энергии диссоциации; среднее геометрическое более точно и почти всегда дает положительную избыточную энергию из-за ионной связи. Квадратный корень из этой избыточной энергии, как отмечает Полинг, приблизительно аддитивен, и, следовательно, можно ввести электроотрицательность. Таким образом, именно эти полуэмпирические формулы для энергии связи лежат в основе концепции электроотрицательности Полинга.
Формулы приблизительны, но это грубое приближение на самом деле относительно хорошее и дает правильную интуицию, имея представление о полярности связи и некоторую теоретическую подготовку в области квантовой механики. Затем определяются электроотрицательности, которые наилучшим образом соответствуют данным.
В более сложных соединениях возникает дополнительная ошибка, поскольку электроотрицательность зависит от молекулярного окружения атома. Кроме того, оценку энергии можно использовать только для одинарных, а не для кратных связей. Энтальпию образования молекулы, содержащей только одинарные связи, можно впоследствии оценить по таблице электроотрицательностей, и она зависит от составляющих и суммы квадратов разностей электроотрицательностей всех пар связанных атомов. Такая формула для оценки энергии обычно имеет относительную погрешность порядка 10%, но ее можно использовать для получения грубого качественного представления и понимания молекулы.
См. Также: Электроотрицательность элементов (страница данных).
Надежных источников Pm, Eu и Yb, кроме диапазона 1,1–1,2, нет; см. Полинг, Лайнус (1960). Природа химической связи. 3-е изд., Издательство Корнельского университета, стр. 93.

Роберт С. Малликен предположил, что среднее арифметическое первой энергии ионизации (E i ) и сродства к электрону (E ea ) должно быть мерой склонности атома притягивать электроны: [9] [10]
Поскольку это определение не зависит от произвольной относительной шкалы, его также называют абсолютной электроотрицательностью [11] с единицами измерения: килоджоули на моль или электронвольты . Однако чаще используется линейное преобразование для преобразования этих абсолютных значений в значения, напоминающие более знакомые значения Полинга. Для энергий ионизации и сродства к электрону в электронвольтах [12]
Электроотрицательность Малликена можно рассчитать только для элемента, сродство к электрону которого известно. Измеренные значения доступны для 72 элементов, а для остальных элементов оценены или рассчитаны приблизительные значения. [ нужна цитата ]
Иногда говорят, что электроотрицательность атома по Малликену является отрицательной величиной химического потенциала . [14] Подставляя энергетические определения потенциала ионизации и сродства к электрону в электроотрицательность Малликена, можно показать, что химический потенциал Малликена представляет собой аппроксимацию конечной разности электронной энергии по отношению к числу электронов., т.е.

А. Луис Оллред и Юджин Дж. Рочоу считали [15] , что электроотрицательность должна быть связана с зарядом, который испытывает электрон на «поверхности» атома: чем выше заряд на единицу площади атомной поверхности, тем больше тенденция атом притягивает электроны. Эффективный заряд ядра Z eff , испытываемый валентными электронами , можно оценить с помощью правил Слейтера , а площадь поверхности атома в молекуле можно принять пропорциональной квадрату ковалентного радиуса r cov . Когда r cov выражается в пикометрах , [16]

Р.Т. Сандерсон также отметил связь между электроотрицательностью Малликена и размером атома и предложил метод расчета, основанный на обратной величине атомного объема. [17] Зная длину связей, модель Сандерсона позволяет оценить энергии связей в широком диапазоне соединений. [18] Модель Сандерсона также использовалась для расчета геометрии молекул, энергии s -электронов, констант спин-спинового взаимодействия ЯМР и других параметров органических соединений. [19] [20] Эта работа лежит в основе концепции выравнивания электроотрицательности , которая предполагает, что электроны распределяются вокруг молекулы, чтобы минимизировать или выровнять электроотрицательность Малликена. [21] Такое поведение аналогично выравниванию химического потенциала в макроскопической термодинамике. [22]

Возможно, самое простое определение электроотрицательности дано Леландом К. Алленом, который предположил, что она связана со средней энергией валентных электронов в свободном атоме, [23] [24] [25]
где ε s,p — одноэлектронные энергии s- и p-электронов в свободном атоме, n s,p — число s- и p-электронов в валентной оболочке. Обычно применяется масштабный коэффициент 1,75×10 -3 для энергий, выраженных в килоджоулях на моль, или 0,169 для энергий, измеряемых в электронвольтах, чтобы получить значения, численно аналогичные электроотрицательности Полинга. [ нужна цитата ]
Одноэлектронные энергии могут быть определены непосредственно из спектроскопических данных , поэтому электроотрицательности, рассчитанные этим методом, иногда называют спектроскопическими электроотрицательностями . Необходимые данные доступны почти для всех элементов, и этот метод позволяет оценить электроотрицательность элементов, которые не могут быть обработаны другими методами, например франция , электроотрицательность которого по Аллену равна 0,67. [26] Однако неясно, что следует считать валентными электронами для элементов d- и f-блока, что приводит к неоднозначности их электроотрицательностей, рассчитанных методом Аллена.
По этой шкале неон имеет самую высокую электроотрицательность среди всех элементов, за ним следуют фтор , гелий и кислород .

Широкое разнообразие методов расчета электроотрицательности, которые дают результаты, хорошо коррелирующие друг с другом, является одним из показателей количества химических свойств, на которые может влиять электроотрицательность. Наиболее очевидным применением электроотрицательности является обсуждение полярности связи , для которой эту концепцию ввел Полинг. В общем, чем больше разница в электроотрицательности между двумя атомами, тем более полярная связь образуется между ними, при этом атом, имеющий более высокую электроотрицательность, находится на отрицательном конце диполя. Полинг предложил уравнение, связывающее «ионный характер» связи с разницей в электроотрицательности двух атомов, [5], хотя оно несколько вышло из употребления.
Было показано несколько корреляций между частотами инфракрасного растяжения некоторых связей и электроотрицательностью участвующих атомов: [27] однако это неудивительно, поскольку такие частоты растяжения частично зависят от прочности связи, которая учитывается при расчете электроотрицательностей Полинга. Более убедительными являются корреляции между электроотрицательностью и химическими сдвигами в ЯМР-спектроскопии [28] или изомерными сдвигами в мессбауэровской спектроскопии [29] (см. рисунок). Оба этих измерения зависят от плотности s-электронов в ядре и поэтому являются хорошим показателем того, что различные меры электроотрицательности действительно описывают «способность атома в молекуле притягивать к себе электроны». [1] [5]
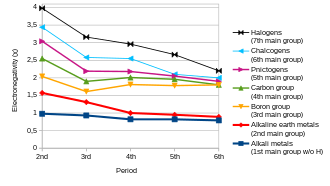
В общем случае электроотрицательность увеличивается при движении слева направо по периоду и уменьшается при уменьшении группы. Следовательно, фтор — наиболее электроотрицательный из элементов (не считая благородных газов ), тогда как цезий — наименее электроотрицательный, по крайней мере, из тех элементов, по которым имеются существенные данные. [26] Это заставило бы поверить, что фторид цезия является соединением , связь которого имеет наиболее ионный характер. [ нужна цитата ]
Из этого общего правила есть некоторые исключения. Галлий и германий имеют более высокую электроотрицательность, чем алюминий и кремний соответственно, из-за сжатия d-блока . Элементы четвертого периода сразу после первого ряда переходных металлов имеют необычно малые атомные радиусы, поскольку 3d-электроны неэффективны для экранирования увеличенного ядерного заряда, а меньший размер атома коррелирует с более высокой электроотрицательностью (см. Электроотрицательность Оллреда-Рочова и Сандерсона). электроотрицательность выше). Аномально высокая электроотрицательность свинца , особенно по сравнению с таллием и висмутом , является артефактом электроотрицательности, меняющейся в зависимости от степени окисления: его электроотрицательность лучше соответствует тенденциям, если его указывать для состояния +2 со значением Полинга 1,87 вместо +4 состояние.
В неорганической химии принято считать, что одно значение электроотрицательности справедливо для большинства «нормальных» ситуаций. Хотя этот подход имеет преимущество простоты, ясно, что электроотрицательность элемента не является неизменным свойством атома и, в частности, увеличивается с увеличением степени окисления элемента. [30]
Оллред использовал метод Полинга для расчета отдельных электроотрицательностей для различных степеней окисления нескольких элементов (включая олово и свинец), для которых было доступно достаточно данных. [8] Однако для большинства элементов недостаточно различных ковалентных соединений, для которых известны энергии диссоциации связей, чтобы сделать этот подход осуществимым. Это особенно верно в отношении переходных элементов, для которых указанные значения электроотрицательности обычно по необходимости усредняются по нескольким различным степеням окисления, и в результате тенденции в электроотрицательности увидеть труднее. [ нужна цитата ]
Химические эффекты этого увеличения электроотрицательности можно увидеть как в структуре оксидов и галогенидов, так и в кислотности оксидов и оксокислот. Следовательно, CrO 3 и Mn 2 O 7 — кислые оксиды с низкой температурой плавления , Cr 2 O 3 — амфотерен , а Mn 2 O 3 — полностью основной оксид .
Эффект также хорошо виден на константах диссоциации p K a оксокислот хлора . Эффект намного сильнее, чем можно было бы объяснить тем, что отрицательный заряд распределяется среди большего числа атомов кислорода, что привело бы к разнице в p K a , равной log 10 ( 1 ⁄ 4 ) = –0,6 между хлорноватистой кислотой и хлорной кислотой . . По мере увеличения степени окисления центрального атома хлора большая электронная плотность переносится с атомов кислорода на хлор, уменьшая частичный отрицательный заряд отдельных атомов кислорода. В то же время положительный частичный заряд водорода увеличивается с более высокой степенью окисления. Этим объясняется наблюдаемое повышение кислотности с увеличением степени окисления в оксокислотах хлора.
Электроотрицательность атома меняется в зависимости от гибридизации орбитали, участвующей в связи. Электроны на s-орбиталях удерживаются сильнее, чем электроны на p-орбиталях. Следовательно, связь с атомом, который использует гибридную орбиталь sp x для связи, будет более сильно поляризована по отношению к этому атому, когда гибридная орбиталь имеет более s-характер. То есть при сравнении электроотрицательностей для разных схем гибридизации данного элемента сохраняется порядок χ(sp 3 ) < χ(sp 2 ) < χ(sp) (эта тенденция должна распространяться и на нецелые индексы гибридизации ). Хотя в принципе это справедливо для любого элемента основной группы, значения электроотрицательности, специфичной для гибридизации, чаще всего приводятся для углерода. В органической химии эта электроотрицательность часто используется для предсказания или объяснения полярности связей в органических соединениях, содержащих двойные и тройные связи с углеродом. [ нужна цитата ]
В органической химии электроотрицательность связана больше с различными функциональными группами, чем с отдельными атомами. Термины групповая электроотрицательность и электроотрицательность заместителя используются как синонимы. Однако принято различать индуктивный эффект и резонансный эффект , которые можно описать как σ- и π-электронотрицательности соответственно. Существует ряд линейных соотношений свободной энергии , которые использовались для количественной оценки этих эффектов, из которых наиболее известно уравнение Хэммета . Параметры Кабачника представляют собой групповые электроотрицательности для использования в фосфорорганической химии .
Электроположительность — это мера способности элемента отдавать электроны и, следовательно, образовывать положительные ионы ; таким образом, это антипод электроотрицательности.
В основном это свойство металлов , а это означает, что, как правило, чем больше металлический характер элемента, тем больше его электроположительность. Следовательно, щелочные металлы являются наиболее электроположительными из всех. Это потому, что у них есть единственный электрон во внешней оболочке, и, поскольку она находится относительно далеко от ядра атома, он легко теряется; другими словами, эти металлы имеют низкую энергию ионизации . [32]
В то время как электроотрицательность увеличивается по периодам в таблице Менделеева и уменьшается по группам , электроположительность уменьшается по периодам (слева направо) и увеличивается по группам. Это означает, что элементы в правом верхнем углу периодической таблицы элементов (кислород, сера, хлор и т. д.) будут иметь наибольшую электроотрицательность, а элементы в левом нижнем углу (рубидий, цезий и франций) — наибольшую электроположительность.
{{cite book}}: CS1 maint: location missing publisher (link)Альтернативный URL