
Ацил-КоА — это группа коферментов , которые метаболизируют карбоновые кислоты . Жирные ацил-КоА подвержены бета-окислению , образуя в конечном итоге ацетил-КоА . Ацетил-КоА вступает в цикл лимонной кислоты , в конечном итоге образуя несколько эквивалентов АТФ . Таким образом, жиры преобразуются в АТФ, общий биохимический носитель энергии.
Жиры расщепляются путем преобразования в ацил-КоА. Это преобразование является одним из ответов на высокие энергетические потребности, такие как физические упражнения. [1] Окислительная деградация жирных кислот представляет собой двухэтапный процесс, катализируемый ацил-КоА-синтетазой . [2] Жирные кислоты превращаются в ацилфосфат, предшественник ацил-КоА. Последнее преобразование опосредуется ацил-КоА-синтазой.
В зависимости от длины цепи жирной кислоты используются три типа ацил-КоА-синтаз. [3] Например, субстратами ацил-КоА-синтазы со средней длиной цепи являются жирные кислоты с 4–11 атомами углерода. [4] Фермент ацил-КоА-тиоэстераза преобразует ацил-КоА в свободную жирную кислоту и кофермент А. [4]
Второй этап деградации жирных кислот — бета-окисление. Бета-окисление происходит в митохондриях. [5] После образования в цитозоле ацил-КоА транспортируется в митохондрии, локус бета-окисления. Для транспорта ацил-КоА в митохондрии требуется карнитинпальмитоилтрансфераза 1 (CPT1), которая превращает ацил-КоА в ацилкарнитин, который транспортируется в митохондриальный матрикс. [1] Попадая в матрицу, ацилкарнитин превращается обратно в ацил-КоА с помощью CPT2. [5] Бета-окисление может начаться сейчас, когда ацил-КоА находится в митохондриях.
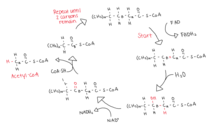
Бета-окисление ацил-КоА происходит в четыре стадии.
1. Ацил-КоА-дегидрогеназа катализирует дегидрирование ацил-КоА, создавая двойную связь между альфа- и бета-углеродами. [6] ФАД является акцептором водорода, образуя ФАДН2. [7]
2. Гидраза эноил-КоА катализирует присоединение воды по вновь образованной двойной связи с образованием спирта. [5] [6]
3. 3-гидроксиацил-КоА-дегидрогеназа окисляет спиртовую группу до кетона. [5] НАДН производится из НАД+ . [6]
4. Тиолаза расщепляет альфа-углерод и кетон, высвобождая одну молекулу ацетил-КоА и ацил-КоА, которая теперь на 2 атома углерода короче. [6]
Этот четырехэтапный процесс повторяется до тех пор, пока ацил-КоА не удалит все атомы углерода из цепи, оставив только ацетил-КоА. За один цикл бета-окисления ацил-КоА создает одну молекулу ацетил-КоА, ФАДН2 и НАДН. [7] Ацетил-КоА затем используется в цикле лимонной кислоты , а ФАДН2 и НАДН отправляются в цепь переноса электронов . [8] Все эти промежуточные продукты в конечном итоге обеспечивают организм энергией, поскольку в конечном итоге преобразуются в АТФ . [8]
Бета-окисление, как и альфа-окисление, также происходит в пероксисоме . [1] Пероксисома отвечает за бета-окисление жирных кислот, которые имеют более 20 атомов углерода в цепи, поскольку пероксисома содержит очень длинноцепочечные ацил-КоА-синтетазы . [9] Эти ферменты лучше приспособлены для окисления ацил-КоА с длинными цепями, с которыми митохондрии не могут справиться.
Бета-окисление удаляет 2 атома углерода за раз, поэтому при окислении 18-углеродной жирной кислоты, такой как стеариновая кислота, потребуется 8 циклов, чтобы полностью разрушить ацил-КоА. [9] В результате образуется 9 ацетил-КоА, каждый из которых содержит по 2 атома углерода, 8 ФАДН2 и 8 НАДН.
Сердечная мышца в первую очередь метаболизирует жир для получения энергии, а метаболизм ацил-КоА был идентифицирован [10] как критическая молекула на ранней стадии недостаточности насоса сердечной мышцы.
Содержание ацил-КоА в клетках коррелирует с резистентностью к инсулину, что позволяет предположить, что он может опосредовать липотоксичность в нежировых тканях. [11] Ацил-КоА: диацилглицерол-ацилтрансфераза (DGAT) играет важную роль в энергетическом обмене благодаря ключевому ферменту в биосинтезе триглицеридов. Синтетическая роль DGAT в жировой ткани, такой как печень и кишечник, местах, где эндогенные уровни ее активности и синтеза триглицеридов высоки, и сравнительно ясна. Кроме того, любые изменения уровня активности могут вызвать изменения системной чувствительности к инсулину и энергетического гомеостаза. [12]
Редкое заболевание, называемое множественным дефицитом ацил-КоА-дегидрогеназы (MADD) [13], представляет собой нарушение метаболизма жирных кислот. Ацил-КоА важен, потому что этот фермент помогает синтезировать ацил-КоА из свободных жирных кислот, что активирует метаболизм жирных кислот. Это нарушенное окисление жирных кислот приводит к множеству различных симптомов, включая тяжелые симптомы, такие как кардиомиопатия и заболевания печени, и легкие симптомы, такие как эпизодическое метаболическое разложение, мышечная слабость и дыхательная недостаточность. MADD — это генетическое заболевание, вызванное мутацией генов ETFA, ETFB и ETFDH. MADD известен как «аутосомно-рецессивное заболевание» [13], поскольку для того, чтобы заболеть этим заболеванием, человек должен получить этот рецессивный ген от обоих родителей.