
Визуализация живых клеток — это исследование живых клеток с помощью покадровой микроскопии . Он используется учеными для лучшего понимания биологических функций посредством изучения клеточной динамики. [1] Визуализация живых клеток была впервые применена в первом десятилетии 21 века. Один из первых покадровых микрокинофильмов о клетках был снят Джулиусом Райсом и показывает оплодотворение и развитие яиц морского ежа. [2] С тех пор было разработано несколько методов микроскопии для более детального изучения живых клеток с меньшими усилиями. Был использован новый тип визуализации с использованием квантовых точек , поскольку они оказались более стабильными. [3] Развитие голотомографической микроскопии игнорировало фототоксичность и другие недостатки окрашивания, применяя цифровое окрашивание на основе показателя преломления клеток. [4] [5]
Биологические системы существуют как сложное взаимодействие бесчисленных клеточных компонентов , взаимодействующих в четырех измерениях, создавая явление, называемое жизнью. Хотя обычно живые организмы превращают в неживые образцы, чтобы использовать традиционные инструменты статической визуализации, чем дальше образец отклоняется от естественных условий, тем больше вероятность того, что рассматриваемые деликатные процессы будут демонстрировать возмущения. [6] Таким образом , обременительная задача по выявлению истинной физиологической идентичности живой ткани требует визуализации с высоким разрешением как в пространстве, так и во времени внутри родительского организма. [7] Технологические достижения в области визуализации живых клеток, предназначенные для получения пространственно-временных изображений внутриклеточных событий в реальном времени, играют важную роль в подтверждении биологической значимости физиологических изменений, наблюдаемых во время экспериментов. Из-за их тесной связи с физиологическими состояниями анализы живых клеток считаются стандартом для исследования сложных и динамических клеточных событий. [8] Поскольку динамические процессы, такие как миграция , развитие клеток и внутриклеточный трафик , все чаще становятся в центре внимания биологических исследований, методы, способные собирать трехмерные данные в реальном времени для клеточных сетей ( in situ ) и целых организмов ( in vivo ), будут становятся незаменимыми инструментами в понимании биологических систем. Общее признание методов визуализации живых клеток привело к быстрому увеличению числа специалистов-практиков и выявило необходимость увеличения пространственного и временного разрешения без ущерба для здоровья клетки. [9]
До появления фазово-контрастного микроскопа наблюдать живые клетки было сложно. Поскольку живые клетки полупрозрачны, их необходимо окрасить , чтобы их можно было увидеть в традиционный световой микроскоп . К сожалению, процесс окрашивания клеток обычно убивает их. С изобретением фазово-контрастной микроскопии стало возможным детально наблюдать неокрашенные живые клетки. После своего появления в 1940-х годах визуализация живых клеток с использованием фазово-контрастной микроскопии быстро стала популярной. [11] Фазово-контрастный микроскоп был популяризирован благодаря серии замедленных видеороликов (см. видео), снятых с помощью фотопленочной камеры. [12] Его изобретатель, Фриц Цернике , был удостоен Нобелевской премии в 1953 году. [13] Другие более поздние методы фазового контраста, используемые для наблюдения неокрашенных клеток, - это модуляция Хоффмана и дифференциально-интерференционная контрастная микроскопия.
Фазово-контрастная микроскопия не позволяет наблюдать специфические белки или другие органические химические соединения, которые образуют сложный механизм клетки. Поэтому для маркировки таких соединений были разработаны синтетические и органические флуоресцентные красители , что позволяет наблюдать их с помощью флуоресцентной микроскопии (см. видео). [15] Однако флуоресцентные пятна фототоксичны , инвазивны и отбеливают при наблюдении. Это ограничивает их использование при наблюдении живых клеток в течение длительных периодов времени. Поэтому неинвазивные методы фазового контраста часто используются в качестве жизненно важного дополнения к флуоресцентной микроскопии при визуализации живых клеток. [16] [17] Однако методы флуоресцентной микроскопии с глубоким обучением помогают снизить световую нагрузку и фототоксичность и позволяют даже повторять живые изображения с высоким разрешением. [18]
В результате быстрого увеличения плотности пикселей цифровых датчиков изображения количественная фазово-контрастная микроскопия стала альтернативным методом микроскопии для визуализации живых клеток. [20] [21] Количественная фазово-контрастная микроскопия имеет преимущество перед флуоресцентной и фазово-контрастной микроскопией в том, что она является одновременно неинвазивной и количественной по своей природе.
Из-за узкой глубины фокуса традиционной микроскопии визуализация живых клеток в настоящее время в значительной степени ограничивается наблюдением клеток в одной плоскости. Большинство реализаций количественной фазово-контрастной микроскопии позволяют создавать и фокусировать изображения в разных фокальных плоскостях за одну экспозицию. Это открывает будущие возможности трехмерной визуализации живых клеток с помощью методов флуоресценции. [22] Количественная фазово-контрастная микроскопия с вращательным сканированием позволяет получать замедленные трехмерные изображения живых клеток с высоким разрешением. [23] [24] [4]
Голотомография (ГТ) — это лазерный метод измерения трехмерной томограммы показателя преломления (RI) микроскопического образца, такого как биологические клетки и ткани. Поскольку RI может служить внутренним контрастом изображения для прозрачных или фазовых объектов, измерения томограмм RI могут обеспечить количественное изображение микроскопических фазовых объектов без меток. Для измерения 3D-томограммы образцов HT использует принцип голографического изображения и обратного рассеяния . Обычно несколько двумерных голографических изображений образца измеряются под разными углами освещения, используя принцип интерферометрического изображения. Затем трехмерная RI-томограмма образца восстанавливается из этих нескольких двумерных голографических изображений путем обратного решения рассеяния света в образце.
Принцип ГТ очень похож на рентгеновскую компьютерную томографию (КТ) или компьютерную томографию . КТ измеряет несколько двумерных рентгеновских изображений человеческого тела под различными углами освещения, а затем получает трехмерную томограмму (поглощение рентгеновских лучей) с использованием теории обратного рассеяния. И рентгеновская КТ, и лазерная ВТ имеют одно и то же основное уравнение – уравнение Гельмгольца , волновое уравнение для монохроматической длины волны. HT также известна как оптическая дифракционная томография.
Сочетание голографии и вращательного сканирования позволяет осуществлять долговременную запись живых клеток без меток.
Неинвазивная оптическая наноскопия может достичь такого латерального разрешения, используя схему квази- 2π -голографического обнаружения и сложную деконволюцию. Пространственные частоты отображаемой клетки не имеют никакого смысла для человеческого глаза. Но эти рассеянные частоты преобразуются в голограмму и синтезируют полосу пропускания, разрешение которой вдвое превышает обычно доступное. Голограммы записываются с разных направлений освещения на плоскости образца и позволяют наблюдать субволновые томографические изменения образца. Наноразмерные апертуры служат для калибровки томографической реконструкции и характеристики системы визуализации с помощью когерентной передаточной функции. Это приводит к реалистичной обратной фильтрации и гарантирует настоящую сложную реконструкцию поля. [24]
В заключение, для трехмерной голотомографической микроскопии разделены две терминологии: (i) оптическое разрешение (реальное) и (ii) разрешение выборки (то, что на экране).
Визуализация живых клеток представляет собой осторожный компромисс между получением изображения с самым высоким разрешением и сохранением жизни клеток как можно дольше. [25] В результате специалисты по микроскопии живых клеток сталкиваются с уникальным набором проблем, которые часто упускаются из виду при работе с фиксированными образцами. Более того, для визуализации живых клеток часто используются специальные оптические системы и детекторы. Например, в идеале микроскопы, используемые для визуализации живых клеток, должны иметь высокое соотношение сигнал/шум , высокую скорость получения изображений для захвата покадровой видео внеклеточных событий и поддерживать долгосрочную жизнеспособность клеток. [26] Однако оптимизация даже одного аспекта получения изображений может оказаться ресурсоемкой и ее следует рассматривать в каждом конкретном случае.
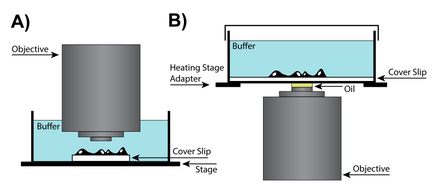
В тех случаях, когда для работы с образцом между объективом и образцом требуется дополнительное пространство, можно использовать сухую линзу, что потенциально требует дополнительной регулировки корректирующего воротника, который изменяет положение линзы в объективе для учета различий. в камерах визуализации. Специальные объективы имеют корректирующие кольца, которые корректируют сферические аберрации с учетом толщины покровного стекла. В сухих объективах с высокой числовой апертурой (NA) регулировочное кольцо корректирующего кольца изменяет положение подвижной группы линз, чтобы учесть различия в том, как внешняя часть линзы фокусирует свет относительно центра. Хотя аберрации свойственны всем конструкциям линз, они становятся более проблематичными для сухих линз, где сохранение разрешения является ключевым моментом. [27]
Масляная иммерсия — это метод, позволяющий повысить разрешение изображения путем погружения линзы и образца в масло с высоким показателем преломления . Поскольку свет преломляется, когда он проходит между средами с разными показателями преломления, помещая масло с тем же показателем преломления, что и стекло, между линзой и предметным стеклом, можно избежать двух переходов между показателями преломления. [28] Однако для большинства применений рекомендуется использовать масляную иммерсию с фиксированными (мертвыми) образцами, поскольку живым клеткам требуется водная среда, а смешивание масла и воды может вызвать серьезные сферические аберрации. В некоторых случаях для более точной реконструкции изображения можно использовать силиконовое масло . Силиконовое масло является привлекательной средой, поскольку оно имеет показатель преломления, близкий к показателю живых клеток, что позволяет создавать изображения с высоким разрешением при минимизации сферических аберраций. [27]
Для визуализации живых клеток требуется образец в водной среде, который часто находится на расстоянии от 50 до 200 микрометров от покровного стекла. Следовательно, водно-иммерсионные линзы могут помочь достичь более высокой разрешающей способности за счет того, что и окружающая среда, и сами клетки будут близки по показателю преломления воды. Водоиммерсионные линзы разработаны с учетом показателя преломления воды и обычно имеют корректирующий воротник, позволяющий регулировать объектив. Кроме того, из-за более высокого показателя преломления воды водоиммерсионные линзы имеют высокую числовую апертуру и могут создавать изображения, превосходящие масляно-иммерсионные линзы, при разрешении плоскостей глубиной более 0 мкм. [27]
Еще одним решением для визуализации живых клеток является погружная линза. Эти линзы представляют собой разновидность водоиммерсионных линз, которые не требуют покровного стекла и могут быть погружены непосредственно в водную среду образца. Одним из основных преимуществ погружной линзы является то, что она имеет большое эффективное рабочее расстояние. [29] Поскольку покровное стекло не требуется, этот тип линзы может приближаться к поверхности образца, и в результате разрешение ограничивается ограничениями, налагаемыми сферической аберрацией, а не физическими ограничениями покровного стекла. Хотя погружаемые линзы могут быть очень полезны, они не идеальны для всех экспериментов, поскольку «погружение» линзы может нарушить работу клеток в образце. Кроме того, поскольку инкубационная камера должна быть открыта для линзы, необходимо внимательно следить за изменениями в среде образца, вызванными испарением. [27]
Сегодня большинство методов визуализации в реальном времени основаны либо на режимах высокой освещенности, либо на флуоресцентном мечении, что одновременно вызывает фототоксичность и ставит под угрозу способность сохранять клетки нетронутыми и живыми в течение долгого времени. Поскольку наши знания в области биологии основаны на наблюдениях, важно минимизировать возмущения, вызванные техникой визуализации.
Развитие конфокальной микроскопии тесно коррелирует с доступностью мощных лазеров, способных достигать высоких интенсивностей светового возбуждения. Однако высокая выходная мощность может повредить чувствительные флуорофоры , поэтому лазеры обычно работают значительно ниже своей полной выходной мощности. [30] Чрезмерное воздействие света может привести к фотоповреждениям из-за фотообесцвечивания или фототоксичности . Эффекты фотообесцвечивания могут значительно снизить качество флуоресцентных изображений, и в последние годы существует значительный спрос на коммерческие флуорофоры с более длительным сроком службы. Одно из решений, серия Alexa Fluor , практически не демонстрирует выцветания даже при высокой интенсивности лазера. [31]
В физиологических условиях многие клетки и типы тканей подвергаются воздействию лишь низкого уровня света. [32] В результате важно свести к минимуму воздействие на живые клетки высоких доз ультрафиолетового (УФ), инфракрасного (ИК) или флуоресцентного возбуждающего света, который может повредить ДНК , повысить клеточную температуру и вызвать фотообесцвечивание. соответственно. [33] Фотоны высокой энергии, поглощаемые флуорофорами и образцом, испускаются на более длинных волнах, пропорциональных стоксову сдвигу . [34] Однако клеточные органеллы могут быть повреждены, когда энергия фотонов вызывает химические и молекулярные изменения, а не повторно излучается. [35] Считается, что основным виновником светоиндуцированной токсичности, испытываемой живыми клетками, являются свободные радикалы, образующиеся в результате возбуждения флуоресцентных молекул. [32] Эти свободные радикалы обладают высокой реакционной способностью и вызывают разрушение клеточных компонентов, что может привести к нефизиологическому поведению.
Одним из методов минимизации фотоповреждения является снижение концентрации кислорода в образце, чтобы избежать образования активных форм кислорода . [36] Однако этот метод не всегда возможен при визуализации живых клеток и может потребовать дополнительного вмешательства. Еще одним методом снижения воздействия свободных радикалов в образце является использование реагентов, препятствующих выцветанию. К сожалению, большинство коммерческих реагентов, препятствующих выцветанию, нельзя использовать для визуализации живых клеток из-за их токсичности. [37] Вместо этого можно использовать естественные поглотители свободных радикалов, такие как витамин С или витамин Е, без существенного изменения физиологического поведения в более коротких временных масштабах. [38] Недавно была разработана и коммерциализирована технология визуализации живых клеток без фототоксичности. Голотомографическая микроскопия позволяет избежать фототоксичности благодаря лазеру малой мощности (класс лазера 1: 0,2 мВт/мм 2 ). [4] [5] [39]