В химии гидроксоний ( гидроксониум в традиционном британском английском ) — общее название катиона [ H 3 O] + , также записываемого как H 3 O + , типа иона оксония, образующегося при протонировании воды . Его часто рассматривают как положительный ион, присутствующий при растворении кислоты Аррениуса в воде, поскольку молекулы кислоты Аррениуса в растворе отдают протон (положительный ион водорода H + ) окружающим молекулам воды ( H 2 O ). Фактически, кислоты должны быть окружены более чем одной молекулой воды, чтобы ионизироваться с образованием водного H + и сопряженного основания. Три основные структуры водного протона получили экспериментальное подтверждение: собственный катион, который представляет собой тетрагидрат, H 3 O + (H 2 O) 3 , катион Цунделя, который представляет собой симметричный дигидрат, H + (H 2 O) 2. , и катион Стоянова, расширенный катион Цунделя, представляющий собой гексагидрат: H + (H 2 O) 2 (H 2 O) 4 . [1] [2] Спектроскопические данные четко определенных ИК-спектров в подавляющем большинстве подтверждают, что катион Стоянова является преобладающей формой. [3] [4] [5] [6] По этой причине было предложено везде, где это возможно, использовать символ H + (aq) вместо иона гидроксония. [2]
Молярная концентрация ионов гидроксония или H + определяет pH раствора по закону
где М = моль/л. Концентрация гидроксид- ионов аналогичным образом определяет pH раствора . Молекулы в чистой воде самодиссоциируют на водные протоны и гидроксид-ионы в следующем равновесии:
В чистой воде равное количество гидроксида и ионов H + , поэтому это нейтральный раствор. При 25 °C (77 °F) чистая вода имеет pH 7 и pH 7 (это значение меняется при изменении температуры: см. Самоионизация воды ). Значение pH менее 7 указывает на кислый раствор, а значение pH более 7 указывает на щелочной раствор. [7]
Согласно номенклатуре органической химии ИЮПАК , ион гидроксония следует называть оксонием . [8] Гидроксоний также может быть однозначно использован для его идентификации. [ нужна цитата ]
Ион оксония – это любой катион, содержащий трехвалентный атом кислорода.
Поскольку O + и N имеют одинаковое количество электронов, H 3 O + изоэлектронен аммиаку . Как показано на изображениях выше, H 3 O + имеет тригональную пирамидальную молекулярную геометрию с атомом кислорода на вершине. Валентный угол H -O-H составляет примерно 113° [9] , а центр масс расположен очень близко к атому кислорода. Поскольку основание пирамиды состоит из трех одинаковых атомов водорода, симметричная верхняя конфигурация молекулы H 3 O + такова, что она принадлежит точечной группе C 3v . Из-за этой симметрии и того факта, что он обладает дипольным моментом, вращательные правила отбора таковы: Δ J = ±1 и Δ K = 0. Переходный диполь расположен вдоль оси c и, поскольку отрицательный заряд локализован вблизи кислорода атома, дипольный момент направлен к вершине, перпендикулярной базовой плоскости. [ нужна цитата ]
Гидратированный протон очень кислый: при 25 °C его p K a составляет примерно 0. [10] Обычно значения p K a aq (H 3 O + ) составляют 0 или –1,74. Первый использует соглашение, согласно которому активность растворителя в разбавленном растворе (в данном случае воды) равна 1, а второй использует значение концентрации воды в чистой жидкости, равное 55,5 М. Сильверстайн показал, что второй значение термодинамически неприемлемо. [11] Разногласия возникают из-за двусмысленности того, что для определения p K a H 3 O + в воде H 2 O должен действовать одновременно как растворенное вещество и растворитель. ИЮПАК не дал официального определения p K a , которое разрешило бы эту двусмысленность. Бургот утверждал, что H 3 O + (водный раствор) + H 2 O (ж) ⇄ H 2 O (водный раствор) + H 3 O + (водный раствор) просто не является термодинамически четко определенным процессом. Для оценки p K a aq (H 3 O + ) Бурго предлагает принять измеренное значение p K a EtOH (H 3 O + ) = 0,3, p K a H 3 O + в этаноле и применить корреляцию уравнение p K a aq = p K a EtOH – 1,0 (± 0,3) для перевода этанола p K a в водное значение, чтобы получить значение p K a aq (H 3 O + ) = –0,7 (± 0,3) . [12] С другой стороны, Сильверстайн показал, что экспериментальные результаты Баллинджера и Лонга [13] подтверждают значение ap K a 0,0 для водного протона. [14] Нилс и Шертель приводят дополнительные аргументы в пользу ap K a , равного 0,0 [15]
Водный протон является наиболее кислым видом, который может существовать в воде (при условии, что воды достаточно для растворения): любая более сильная кислота ионизируется и дает гидратированный протон. Кислотность H + (водн.) является неявным стандартом, используемым для оценки силы кислоты в воде: сильные кислоты должны быть лучшими донорами протонов, чем Н + (водн.), так как в противном случае значительная часть кислоты будет существовать в неактивном состоянии. ионизированное состояние (т.е.: слабая кислота). В отличие от Н + (водн.) в нейтральных растворах, образующихся в результате самодиссоциации воды, в кислых растворах Н + (водн.) сохраняется длительно и концентрируется пропорционально силе растворенной кислоты. [ нужна цитата ]
Первоначально предполагалось, что pH является мерой концентрации ионов водорода в водном растворе. [16] Практически все такие свободные протоны быстро гидратируются; поэтому кислотность водного раствора более точно характеризуется концентрацией в нем H + (водн.). В органических синтезах, таких как реакции, катализируемые кислотами, ион гидроксония ( H 3 O + ) используется взаимозаменяемо с ионом H + ; выбор одного вместо другого не оказывает существенного влияния на механизм реакции. [ нужна цитата ]
Исследователям еще предстоит полностью охарактеризовать сольватацию иона гидроксония в воде, отчасти потому, что существует множество различных значений сольватации. Исследование депрессии температуры замерзания показало, что средний гидратный ион в холодной воде составляет примерно H 3 O + (H 2 O) 6 : [17] в среднем каждый ион гидроксония сольватируется 6 молекулами воды, которые не способны сольватировать другие растворенные вещества. молекулы. [ нужна цитата ]
Некоторые гидратные структуры довольно велики: структура магического ионного числа H 3 O + (H 2 O) 20 (называемая магическим числом из-за ее повышенной стабильности по отношению к гидратным структурам, включающим сопоставимое количество молекул воды – это аналогичное использование термин «магическое число» , как в ядерной физике ), может поместить гидроний внутри додекаэдрической клетки. [18] Однако более позднее моделирование молекулярной динамики методом ab initio показало, что в среднем гидратированный протон находится на поверхности кластера H 3 O + (H 2 O) 20 . [19] Кроме того, некоторые несопоставимые особенности этих симуляций согласуются с их экспериментальными аналогами, что предполагает альтернативную интерпретацию экспериментальных результатов. [ нужна цитата ]

Двумя другими хорошо известными структурами являются катион Цунделя и катион Собственного . Собственная сольватная структура имеет ион гидроксония в центре H 9 O.+4комплекс, в котором гидроксоний имеет прочную водородную связь с тремя соседними молекулами воды. [20] В Цунделе H 5 O+2В сложном комплексе протон поровну принадлежит двум молекулам воды, образующим симметричную водородную связь . [21] Недавние работы показывают, что оба этих комплекса представляют собой идеальные структуры с более общим дефектом сети водородных связей. [22]
Выделение мономера иона гидроксония в жидкой фазе осуществляли в неводном растворе суперкислоты с низкой нуклеофильностью ( HF - SbF 5 SO 2 ). Ион характеризовался ядерным магнитным резонансом 17 O высокого разрешения . [23]
Расчет энтальпий и свободных энергий различных водородных связей вокруг катиона гидроксония в жидкой протонированной воде в 2007 году [24] при комнатной температуре и исследование механизма прыжка протона с использованием молекулярной динамики показали, что водородные связи вокруг иона гидроксония ( образующиеся с тремя водными лигандами в первой сольватной оболочке гидроксония) довольно сильны по сравнению с таковыми в объемной воде. [ нужна цитата ]
Новая модель была предложена Стояновым на основе инфракрасной спектроскопии , в которой протон существует в виде H 13 O.+6ион. Таким образом, положительный заряд делокализован по 6 молекулам воды. [25]
Для многих сильных кислот возможно образование кристаллов гидроксониевой соли, которые относительно стабильны. Эти соли иногда называют моногидратами кислот . Как правило, любая кислота с константой ионизации 109 или выше могут это сделать. Кислоты, константы ионизации которых ниже 109 вообще не может образовывать стабильныесоли H 3 O + . Например, азотная кислота имеет константу ионизации 10.1,4 , а смеси с водой во всех соотношениях являются жидкими при комнатной температуре. Однако хлорная кислота имеет константу ионизации 10.10 , а если жидкую безводную хлорную кислоту и воду объединить в молярном соотношении 1:1, они вступят в реакцию с образованием твердого перхлората гидроксония ( H 3 O + ·ClO−4). [ нужна цитата ]
Ион гидроксония также образует устойчивые соединения с карборановой суперкислотой H(CB 11 H(CH 3 ) 5 Br 6 ) . [26] Рентгеновская кристаллография показывает симметрию C 3v для иона гидроксония, где каждый протон взаимодействует с атомом брома каждого из трех карборановых анионов, находящихся в среднем на расстоянии 320 пм друг от друга. Соль [H 3 O] [H(CB 11 HCl 11 )] также растворима в бензоле . В кристаллах, выращенных из раствора бензола, растворитель сокристаллизуется и катион H 3 O·(C 6 H 6 ) 3 полностью отделяется от аниона. В катионе три молекулы бензола окружают гидроксоний, образуя пи-катионные взаимодействия с атомами водорода. Ближайшее (несвязывающее) сближение аниона хлора с катионом кислорода составляет 348 пм.
Также известно много примеров солей, содержащих гидратированные ионы гидроксония, такие как H 5 O+2ион в HCl·2H 2 O , H 7 O+3и Н 9 О+4оба иона обнаружены в HBr·4H 2 O . [27]
Известно также, что серная кислота образует гидроксониевую соль H 3 O + HSO.−4при температуре ниже 8,49 °C (47,28 °F). [28]
Гидроний является распространенным молекулярным ионом в межзвездной среде и встречается в диффузных [29] и плотных [30] молекулярных облаках, а также в плазменных хвостах комет. [31] Межзвездные источники наблюдений гидрония включают области Стрельца B2, Ориона OMC-1, Ориона BN–IRc2, Ориона KL и кометы Хейла–Боппа.
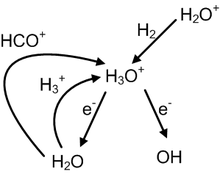
Межзвездный гидроксоний образуется в результате цепочки реакций, начинающихся с ионизации H 2 в H+2космическим излучением. [32] H 3 O + может производить либо OH −, либо H 2 O посредством реакций диссоциативной рекомбинации , которые происходят очень быстро даже при низких (≥10 К) температурах плотных облаков. [33] Это приводит к тому, что гидроний играет очень важную роль в межзвездной ионно-нейтральной химии. [ нужна цитата ]
Астрономы особенно заинтересованы в определении содержания воды в различных межзвездных климатах из-за ее ключевой роли в охлаждении плотных молекулярных газов посредством радиационных процессов. [34] Однако у H 2 O не так много благоприятных переходов для наземных наблюдений. [35] Хотя наблюдения за HDO ( дейтерированной версией воды [36] ) потенциально могут быть использованы для оценки содержания H 2 O , отношение HDO к H 2 O неизвестно очень точно. [35]
С другой стороны, гидроний имеет несколько переходов, которые делают его лучшим кандидатом для обнаружения и идентификации в различных ситуациях. [35] Эта информация использовалась в сочетании с лабораторными измерениями коэффициентов ветвления различных реакций диссоциативной рекомбинации H 3 O + [33] для получения, как полагают, относительно точных содержаний OH - и H 2 O , не требующих прямого наблюдения. этих видов. [37] [38]
Как упоминалось ранее, H 3 O + встречается как в диффузных, так и в плотных молекулярных облаках. Применяя константы скорости реакции ( α , β и γ ), соответствующие всем доступным в настоящее время охарактеризованным реакциям с участием H 3 O + , можно рассчитать k ( T ) для каждой из этих реакций. Умножив эти значения k ( T ) на относительное содержание продуктов, можно определить относительные скорости (в см 3 /с) каждой реакции при данной температуре. Эти относительные скорости можно перевести в абсолютные значения, умножив их на [H 2 ] 2 . [39] Если предположить, что T = 10 K для плотного облака и T = 50 K для диффузного облака, результаты показывают, что наиболее доминирующие механизмы образования и разрушения были одинаковыми для обоих случаев. Следует отметить, что относительные содержания, используемые в этих расчетах, соответствуют TMC-1, плотному молекулярному облаку, и поэтому ожидается, что рассчитанные относительные скорости будут более точными при T = 10 K. Три самых быстрых механизма формирования и разрушения перечислены в таблице ниже, а также их относительная скорость. Обратите внимание, что скорости этих шести реакций таковы, что составляют примерно 99% химических взаимодействий ионов гидроксония в этих условиях. [31] Все три механизма разрушения в таблице ниже классифицируются как реакции диссоциативной рекомбинации . [40]
Также стоит отметить, что относительные скорости реакций образования в таблице выше одинаковы для данной реакции при обеих температурах. Это связано с тем, что константы скорости этих реакций имеют константы β и γ , равные 0, что приводит к k = α , который не зависит от температуры. [ нужна цитата ]
Поскольку все три реакции производят либо H 2 O, либо OH, эти результаты усиливают тесную связь между их относительным содержанием и содержанием H 3 O + . Скорости этих шести реакций таковы, что они составляют примерно 99% химических взаимодействий ионов гидроксония в этих условиях. [ нужна цитата ]
Еще в 1973 году, до первого межзвездного обнаружения, химические модели межзвездной среды (первая из которых соответствовала плотному облаку) предсказывали, что гидроний является распространенным молекулярным ионом и играет важную роль в ионно-нейтральной химии. [41] Однако, прежде чем астрономические поиски могли быть продолжены, все еще оставался вопрос определения спектроскопических особенностей гидроксония в газовой фазе, которые на тот момент были неизвестны. Первые исследования этих характеристик были проведены в 1977 году [42] , за которыми последовали другие эксперименты по спектроскопии более высокого разрешения. После того, как в лаборатории было идентифицировано несколько линий, первое межзвездное обнаружение H 3 O + было сделано двумя группами почти одновременно в 1986 году. [30] [35] В первом из них, опубликованном в июне 1986 года, сообщалось о наблюдении Jвт
К = 1−
1 − 2+
1переход в307 192,41 МГц в OMC-1 и Sgr B2. Во втором, опубликованном в августе, сообщалось о наблюдении того же перехода к туманности Орион-KL. [ нужна цитата ]
За этими первыми открытиями последовали наблюдения ряда дополнительных переходов H 3 O + . Первые наблюдения каждого последующего обнаружения перехода приведены ниже в хронологическом порядке:
В 1991 году 3+
2 − 2−
2переход в364 797 , 427 МГц наблюдалась у OMC-1 и Sgr B2. [43] Год спустя 3+
0 − 2−
0переход в396 272 ,412 МГц наблюдалась в нескольких регионах, самым ясным из которых было облако W3 IRS 5. [38]
Первый дальний ИК 4−
3 − 3+
3переход на длине волны 69,524 мкм (4,3121 ТГц) был осуществлен в 1996 г. вблизи Ориона BN-IRc2. [44] В 2001 году три дополнительных перехода H 3 O + in наблюдались в дальнем инфракрасном диапазоне в Sgr B2; 2−
1 − 1+
1переход на 100,577 мкм (2,98073 ТГц), 1−
1 − 1+
1на 181,054 мкм (1,65582 ТГц) и 2−
0 − 1+
0на частоте 100,869 мкм (2,9721 ТГц). [45]