Нижняя критическая температура растворения ( НКТР ) или нижняя температура консолютации — это критическая температура , ниже которой компоненты смеси смешиваются во всех пропорциях. [1] [2] Слово « ниже» указывает на то, что НКТР является нижней границей температурного интервала частичной смешиваемости или смешиваемости только для определенных составов.
Фазовое поведение полимерных растворов является важным свойством, участвующим в разработке и проектировании большинства процессов, связанных с полимерами. Частично смешивающиеся полимерные растворы часто демонстрируют две границы растворимости, верхнюю критическую температуру растворения (ВКТР) и НКТР, обе из которых зависят от молярной массы и давления. При температурах ниже НКТР система полностью смешивается во всех пропорциях, тогда как выше НКТР происходит частичная смешиваемость жидкостей. [3] [4]
На фазовой диаграмме компонентов смеси НКТС является общим минимумом вогнутых вверх спинодальных и бинодальных (или сосуществующих) кривых. Она в общем случае зависит от давления , увеличиваясь как функция повышенного давления.
Для малых молекул существование НКТР встречается гораздо реже, чем существование верхней критической температуры растворения (ВКРТ), но некоторые случаи все же существуют. Например, система триэтиламин - вода имеет ВКРТ 19 °C, так что эти два вещества смешиваются во всех пропорциях ниже 19 °C, но не при более высоких температурах. [1] [2] Система никотин - вода имеет ВКРТ 61 °C, а также ВКРТ 210 °C при давлениях, достаточно высоких для существования жидкой воды при этой температуре. Таким образом, компоненты смешиваются во всех пропорциях ниже 61 °C и выше 210 °C (при высоком давлении) и частично смешиваются в интервале от 61 до 210 °C. [1] [2]
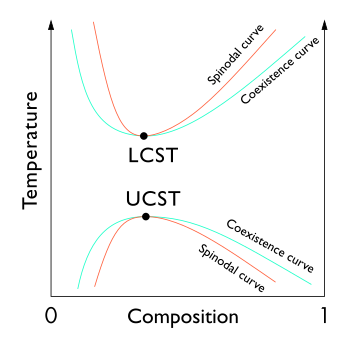
Некоторые полимерные растворы имеют LCST при температурах выше UCST. Как показано на диаграмме, это означает, что существует температурный интервал полной смешиваемости, с частичной смешиваемостью как при более высоких, так и при более низких температурах. [5]
В случае полимерных растворов НКТР также зависит от степени полимеризации полимера , полидисперсности и разветвленности [6] , а также от состава и архитектуры полимера. [7] Одним из наиболее изученных полимеров, водные растворы которых демонстрируют НКТР, является поли(N-изопропилакриламид) . Хотя широко распространено мнение, что этот фазовый переход происходит при 32 °C (90 °F), [8] фактические температуры могут отличаться на 5–10 °C (или даже больше) в зависимости от концентрации полимера, [8] молярной массы полимерных цепей, дисперсности полимера , а также концевых фрагментов. [8] [9] Кроме того, другие молекулы в полимерном растворе, такие как соли или белки, могут изменять температуру точки помутнения. [10] [11] Другим мономером, гомо- и сополимеры которого демонстрируют поведение НКТР в растворе, является 2-(диметиламино)этилметакрилат. [12] [13] [14] [15] [16]
НКТР зависит от способа приготовления полимера и, в случае сополимеров, от соотношения мономеров, а также от гидрофобной или гидрофильной природы полимера.
На сегодняшний день обнаружено более 70 примеров неионных полимеров с НКТР в водном растворе. [17]
Ключевым физическим фактором, отличающим НКТР от поведения других смесей, является то, что разделение фаз НКТР обусловлено неблагоприятной энтропией смешивания . [18] Поскольку смешивание двух фаз происходит спонтанно ниже НКТР, а не выше, изменение свободной энергии Гиббса (ΔG) для смешивания этих двух фаз отрицательно ниже НКТР и положительно выше, а изменение энтропии ΔS = – (dΔG/dT) отрицательно для этого процесса смешивания. Это контрастирует с более распространенным и интуитивно понятным случаем, в котором энтропия управляет смешиванием из-за увеличенного объема, доступного каждому компоненту при смешивании.
В общем, неблагоприятная энтропия смешивания, ответственная за НКТР, имеет одно из двух физических источников. Первое — это ассоциированные взаимодействия между двумя компонентами, такие как сильные полярные взаимодействия или водородные связи , которые предотвращают случайное смешивание. Например, в системе триэтиламин-вода молекулы амина не могут образовывать водородные связи друг с другом, а только с молекулами воды, поэтому в растворе они остаются связанными с молекулами воды с потерей энтропии. Смешивание, которое происходит ниже 19 °C, происходит не из-за энтропии, а из-за энтальпии образования водородных связей. Было показано, что достаточно сильные, геометрически обоснованные, ассоциативные взаимодействия между растворенным веществом и растворителем(ями) достаточны для того, чтобы привести к НКТР. [19]
Вторым физическим фактором, который может привести к НКТС, являются эффекты сжимаемости, особенно в системах полимер-растворитель. [18] Для неполярных систем, таких как полистирол в циклогексане , разделение фаз наблюдалось в запаянных трубках (при высоком давлении) при температурах, приближающихся к критической точке жидкость-пар растворителя. При таких температурах растворитель расширяется гораздо быстрее, чем полимер, сегменты которого ковалентно связаны. Поэтому смешивание требует сжатия растворителя для совместимости полимера, что приводит к потере энтропии. [5]
В статистической механике НКТС может быть теоретически смоделирована с помощью модели решеточной жидкости, расширения теории растворов Флори–Хаггинса , которая включает в себя вакансии и, таким образом, учитывает эффекты переменной плотности и сжимаемости. [18]
Более новые расширения теории растворов Флори-Хаггинса показали, что включение только геометрически обоснованных ассоциативных взаимодействий между растворенным веществом и растворителем достаточно для наблюдения НКТР. [19]
Существует три группы методов корреляции и прогнозирования НКТС. Первая группа предлагает модели, основанные на прочной теоретической основе с использованием экспериментальных данных жидкость–жидкость или пар–жидкость. Эти методы требуют экспериментальных данных для корректировки неизвестных параметров, что приводит к ограниченной прогностической способности. [20] Другой подход использует эмпирические уравнения, которые коррелируют θ (НКТС) с физико-химическими свойствами, такими как плотность, критические свойства и т. д., но страдает от недостатка, что эти свойства не всегда доступны. [21] [22] Новый подход, предложенный Лю и Чжун, разрабатывает линейные модели для прогнозирования θ(НКТС) с использованием индексов молекулярной связности, которые зависят только от структур растворителя и полимера. [23] [24] Последний подход оказался очень полезным методом в исследовании количественных соотношений структура–активность/свойство (QSAR/QSPR) для полимеров и полимерных растворов. Исследования QSAR / QSPR представляют собой попытку сократить элемент проб и ошибок в разработке соединений с желаемой активностью/свойствами путем установления математических соотношений между интересующей активностью/свойством и измеримыми или вычисляемыми параметрами, такими как топологические, физико-химические, стереохимические или электронные индексы. Совсем недавно были опубликованы модели QSPR для прогнозирования θ (LCST) с использованием молекулярных (электронных, физико-химических и т. д.) дескрипторов. [25] Используя проверенные надежные модели QSPR, можно значительно сократить экспериментальное время и усилия, поскольку надежные оценки θ (LCST) для полимерных растворов могут быть получены до того, как они будут фактически синтезированы в лаборатории.
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка )