
Генетическое заболевание – это проблема со здоровьем, вызванная одной или несколькими аномалиями в геноме . Оно может быть вызвано мутацией одного гена ( моногенная), нескольких генов (полигенная) или хромосомной аномалией . Хотя полигенные заболевания являются наиболее распространенными, этот термин чаще всего используется при обсуждении заболеваний, имеющих единственную генетическую причину, либо в гене, либо в хромосоме . [1] [2] Ответственная мутация может возникнуть спонтанно до эмбрионального развития ( мутация de novo ) или может быть унаследована от двух родителей, являющихся носителями дефектного гена ( аутосомно-рецессивное наследование), или от родителя с заболеванием ( аутосомно-доминантное наследование). Когда генетическое заболевание унаследовано от одного или обоих родителей, оно также классифицируется как наследственное заболевание . Некоторые заболевания вызваны мутацией Х-хромосомы и имеют Х-сцепленное наследование. Очень немногие заболевания наследуются по Y-хромосоме или митохондриальной ДНК (из-за их размера). [3]
Известно более 6000 генетических нарушений [4] , и в медицинской литературе постоянно описываются новые генетические нарушения. [5] Более 600 генетических нарушений поддаются лечению. [6] Примерно 1 из 50 человек страдает известным моногенным заболеванием, а примерно 1 из 263 страдает хромосомным заболеванием . [7] Около 65% людей имеют те или иные проблемы со здоровьем в результате врожденных генетических мутаций. [7] Из-за значительного количества генетических нарушений примерно 1 из 21 человека страдает генетическим заболеванием, классифицируемым как « редкое » (обычно определяемое как затрагивающее менее 1 из 2000 человек). Большинство генетических нарушений сами по себе редки. [5] [8]
Генетические нарушения присутствуют еще до рождения, а некоторые генетические нарушения вызывают врожденные дефекты , но врожденные дефекты также могут быть скорее связанными с развитием , чем наследственными . Противоположностью наследственной болезни является приобретенная болезнь . Большинство видов рака , хотя они и связаны с генетическими мутациями небольшой части клеток организма, являются приобретенными заболеваниями. Однако некоторые раковые синдромы , такие как мутации BRCA , являются наследственными генетическими нарушениями. [9]
Одногенное заболевание (или моногенное заболевание ) является результатом мутации одного гена. Одногенные расстройства могут передаваться последующим поколениям несколькими способами. Однако геномный импринтинг и однородительская дисомия могут влиять на характер наследования. Разделение между рецессивным и доминантным типами не является «жестким и быстрым», хотя разделение между аутосомными и Х-сцепленными типами является (поскольку последние типы различаются исключительно на основе хромосомного расположения гена). Например, распространенная форма карликовости , ахондроплазия , обычно считается доминантным заболеванием, но дети с двумя генами ахондроплазии имеют тяжелое и обычно смертельное заболевание скелета, носителем которого можно считать ахондроплазию. Серповидно-клеточная анемия также считается рецессивным заболеванием, но гетерозиготные носители имеют повышенную устойчивость к малярии в раннем детстве, что можно охарактеризовать как родственное доминантное заболевание. [18] Когда пара, у которой один партнер или оба страдают заболеванием или являются носителями моногенного заболевания, желает иметь ребенка, они могут сделать это посредством экстракорпорального оплодотворения, которое позволяет провести преимплантационную генетическую диагностику, чтобы проверить, есть ли у эмбриона генетическое расстройство. [19]
Большинство врожденных нарушений обмена веществ , известных как врожденные нарушения обмена веществ, возникают в результате дефектов одного гена. Многие такие дефекты одного гена могут снизить приспособленность затронутых людей и, следовательно, присутствовать в популяции с более низкой частотой по сравнению с тем, что можно было бы ожидать на основе простых вероятностных расчетов. [20]
Для того чтобы у человека развилось аутосомно-доминантное заболевание, достаточно одной мутировавшей копии гена. У каждого пострадавшего человека обычно есть один затронутый родитель. [21] : 57 Вероятность того, что ребенок унаследует мутировавший ген, составляет 50%. Аутосомно-доминантные состояния иногда имеют пониженную пенетрантность . Это означает, что, хотя необходима только одна мутировавшая копия, не у всех людей, унаследовавших эту мутацию, развивается заболевание. Примерами этого типа расстройств являются болезнь Хантингтона , [21] : 58 нейрофиброматоз 1-го типа , нейрофиброматоз 2-го типа , синдром Марфана , наследственный неполипозный колоректальный рак , наследственные множественные экзостозы (высокопенетрантное аутосомно-доминантное заболевание), туберозный склероз , болезнь фон Виллебранда , и острая перемежающаяся порфирия . Врожденные дефекты также называют врожденными аномалиями. [ нужна цитата ]
Две копии гена должны быть мутированы, чтобы человек заболел аутосомно-рецессивным заболеванием. У пораженного человека обычно есть здоровые родители, каждый из которых несет одну копию мутировавшего гена и называется генетическим носителем . Каждый родитель с дефектным геном обычно не имеет симптомов. [22] Два здоровых человека, каждый из которых является носителем одной копии мутировавшего гена, имеют 25%-ный риск при каждой беременности родить ребенка, страдающего этим расстройством. Примерами расстройств этого типа являются альбинизм , дефицит ацил-КоА-дегидрогеназы средней цепи , муковисцидоз , серповидноклеточная анемия , болезнь Тея-Сакса , болезнь Нимана-Пика , спинальная мышечная атрофия и синдром Робертса . Некоторые другие фенотипы, такие как влажная или сухая ушная сера , также определяются по аутосомно-рецессивному типу. [23] [24] Некоторые аутосомно-рецессивные заболевания распространены потому, что в прошлом носительство одного из дефектных генов приводило к незначительной защите от инфекционных заболеваний или токсинов, таких как туберкулез или малярия . [25] К таким расстройствам относятся муковисцидоз, [26] серповидно-клеточная анемия, [27] фенилкетонурия [28] и талассемия . [29]

Х-сцепленные доминантные расстройства вызваны мутациями в генах Х-хромосомы . Лишь немногие заболевания имеют такой тип наследования, ярким примером является Х-сцепленный гипофосфатемический рахит . Этим расстройствам страдают как мужчины, так и женщины, при этом мужчины обычно страдают более серьезно, чем женщины. Некоторые Х-сцепленные доминантные состояния, такие как синдром Ретта , пигментное недержание 2-го типа и синдром Айкарди , обычно приводят к летальному исходу у мужчин либо внутриутробно , либо вскоре после рождения, и поэтому преимущественно наблюдаются у женщин. Исключением из этого вывода являются чрезвычайно редкие случаи, когда мальчики с синдромом Клайнфельтера (44+xxy) также наследуют Х-сцепленное доминантное заболевание и проявляют симптомы, более сходные с симптомами у женщин с точки зрения тяжести заболевания. Вероятность передачи Х-сцепленного доминантного расстройства у мужчин и женщин различна. Сыновья мужчины с Х-сцепленным доминантным заболеванием не пострадают (поскольку они получают Y-хромосому своего отца), но все его дочери унаследуют это заболевание. У женщины с Х-сцепленным доминантным заболеванием вероятность рождения пораженного плода при каждой беременности составляет 50%, хотя в таких случаях, как пигментное недержание мочи, жизнеспособными обычно являются только потомки женского пола.
Х-сцепленные рецессивные состояния также вызываются мутациями в генах Х-хромосомы. Мужчины болеют гораздо чаще, чем женщины, поскольку у них есть только одна Х-хромосома, необходимая для проявления заболевания. Вероятность передачи расстройства различается у мужчин и женщин. Сыновья мужчины с Х-сцепленным рецессивным заболеванием не пострадают (поскольку они получают Y-хромосому своего отца), но его дочери будут носителями одной копии мутировавшего гена. Женщина, являющаяся носителем Х-сцепленного рецессивного заболевания (XRXr ) , имеет 50%-ный шанс родить сыновей, пораженных этим заболеванием, и 50%-ный шанс родить дочерей-носителей одной копии мутировавшего гена . Х-сцепленные рецессивные состояния включают серьезные заболевания гемофилию А , мышечную дистрофию Дюшенна и синдром Леша-Нихана , а также распространенные и менее серьезные заболевания, такие как облысение по мужскому типу и красно-зеленую дальтонизм . Х-сцепленные рецессивные состояния иногда могут проявляться у женщин из-за искаженной Х-инактивации или моносомии Х ( синдром Тернера ). [ нужна цитата ]
Y-сцепленные расстройства вызваны мутациями Y-хромосомы. Эти состояния могут передаваться только от гетерогаметного пола (например, мужчины) потомству того же пола. Проще говоря, это означает, что Y-сцепленные расстройства у людей могут передаваться только от мужчин к их сыновьям; самки никогда не могут быть затронуты, поскольку у них нет Y-аллосом. [ нужна цитата ]
Y-сцепленные расстройства встречаются чрезвычайно редко, но наиболее известные примеры обычно вызывают бесплодие. Репродукция в таких условиях возможна только путем обхода бесплодия путем медицинского вмешательства.
Этот тип наследования, также известный как материнское наследование, является самым редким и распространяется на 13 генов, кодируемых митохондриальной ДНК . Поскольку только яйцеклетки вносят митохондрии в развивающийся эмбрион, только матери (которые поражены) могут передать состояния митохондриальной ДНК своим детям. Примером этого типа расстройства является наследственная нейропатия зрительного нерва Лебера . [ нужна цитата ]
Важно подчеркнуть, что подавляющее большинство митохондриальных заболеваний (особенно когда симптомы развиваются в раннем возрасте) на самом деле вызваны дефектом ядерного гена , поскольку митохондрии в основном развиваются из немитохондриальной ДНК. Эти заболевания чаще всего наследуются по аутосомно-рецессивному типу. [30]
Генетические нарушения также могут быть сложными, многофакторными или полигенными, то есть они, вероятно, связаны с воздействием нескольких генов в сочетании с образом жизни и факторами окружающей среды. Многофакторные расстройства включают болезни сердца и диабет . Хотя сложные расстройства часто группируются в семьях, они не имеют четкой картины наследования. Это затрудняет определение риска унаследования или передачи этих заболеваний для человека. Сложные расстройства также трудно изучать и лечить, поскольку конкретные факторы, вызывающие большинство этих расстройств, еще не идентифицированы. Исследования, направленные на выявление причины сложных нарушений, могут использовать несколько методических подходов для определения генотип - фенотипических ассоциаций. Один из методов, подход «сначала генотип» , начинается с выявления генетических вариантов у пациентов, а затем определения связанных с ними клинических проявлений. Это противоречит более традиционному подходу, основанному на фенотипе, и может выявить причинные факторы, которые ранее были скрыты из-за клинической гетерогенности , пенетрантности и экспрессивности. [ нужна цитата ]
В родословной полигенные заболевания имеют тенденцию «передаваться по наследству», но наследование не соответствует простым закономерностям, как в случае с менделевскими болезнями. Это не означает, что гены в конечном итоге невозможно обнаружить и изучить. Многие из них также имеют сильную экологическую составляющую (например, кровяное давление ). Другие факторы включают в себя:
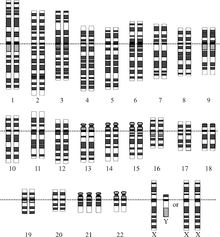
Хромосомное заболевание — это отсутствующая, дополнительная или неправильная часть хромосомной ДНК. [31] Причиной может быть нетипичное количество хромосом или структурная аномалия в одной или нескольких хромосомах. Примером таких нарушений является трисомия 21 (наиболее распространенная форма синдрома Дауна ), при которой во всех клетках имеется дополнительная копия хромосомы 21. [32]
Из-за широкого спектра известных генетических нарушений диагнозы широко варьируются и зависят от заболевания. Большинство генетических нарушений диагностируются до рождения , при рождении или в раннем детстве, однако некоторые из них, такие как болезнь Хантингтона , могут оставаться незамеченными до тех пор, пока у пациента не начнут проявляться симптомы во взрослом возрасте. [33]
Основные аспекты генетического заболевания основаны на наследственности генетического материала. Имея подробный семейный анамнез , можно предвидеть возможные расстройства у детей, что направляет медицинских работников на конкретные обследования в зависимости от расстройства и дает родителям возможность подготовиться к потенциальным изменениям образа жизни, предвидеть возможность мертворождения или рассмотреть возможность прерывания беременности . [34] Пренатальная диагностика может обнаружить наличие характерных отклонений в развитии плода с помощью ультразвука или обнаружить наличие характерных веществ с помощью инвазивных процедур , которые включают введение зондов или игл в матку, например, при амниоцентезе . [35]
Не все генетические нарушения напрямую приводят к смерти; однако не существует известных методов лечения генетических нарушений. Многие генетические нарушения влияют на стадии развития, например, синдром Дауна , тогда как другие приводят к чисто физическим симптомам, таким как мышечная дистрофия . Другие заболевания, такие как болезнь Хантингтона , не проявляют никаких признаков до взрослой жизни. В активное время генетического заболевания пациенты в основном полагаются на поддержание или замедление ухудшения качества жизни и сохранение автономии пациента . Это включает в себя физиотерапию и обезболивание .

Лечение генетических нарушений — это непрекращающаяся битва: во всем мире уже завершено, продолжается или было одобрено более 1800 клинических испытаний генной терапии . [36] Несмотря на это, большинство вариантов лечения вращаются вокруг лечения симптомов расстройств с целью улучшить качество жизни пациентов .
Генная терапия относится к форме лечения, при которой пациенту вводится здоровый ген. Это должно облегчить дефект, вызванный дефектным геном, или замедлить прогрессирование заболевания. Основным препятствием была доставка генов в соответствующие клетки, ткани и органы, пораженные заболеванием. Исследователи изучили, как можно внедрить ген в потенциально триллионы клеток, несущих дефектную копию. Поиск ответа на этот вопрос стал препятствием между пониманием генетического заболевания и его коррекцией. [37]
Примерно 1 из 50 человек страдает известным моногенным заболеванием, а около 1 из 263 страдает хромосомным заболеванием . [7] Около 65% людей имеют те или иные проблемы со здоровьем в результате врожденных генетических мутаций. [7] Из-за значительного количества генетических нарушений примерно 1 из 21 человека страдает генетическим заболеванием, классифицируемым как « редкое » (обычно определяемое как затрагивающее менее 1 из 2000 человек). Большинство генетических нарушений сами по себе редки. [5] [8] Известно более 6000 генетических нарушений, [4] и в медицинской литературе постоянно описываются новые генетические нарушения. [5]
Самое раннее известное генетическое состояние гоминида было у ископаемых видов Paranthropusrobustus , причем более трети особей демонстрировали несовершенный амелогенез . [38]
(рассчитано на основе «1 из 17» редких заболеваний и «80%» редких заболеваний, являющихся генетическими).