Агломерация частиц относится к образованию скоплений в суспензии и представляет собой механизм, приводящий к функциональной дестабилизации коллоидных систем. Во время этого процесса частицы, диспергированные в жидкой фазе , прилипают друг к другу и спонтанно образуют нерегулярные скопления частиц, хлопья или агломераты. Это явление также называется коагуляцией или флокуляцией , а такая суспензия также называется нестабильной . Агломерация частиц может быть вызвана добавлением солей или других химикатов, называемых коагулянтами или флокулянтами . [1]

Агломерация частиц может быть обратимым или необратимым процессом. Агломераты частиц, определяемые как «жесткие агломераты», сложнее повторно диспергировать в исходные отдельные частицы. В ходе агломерации агломераты будут увеличиваться в размерах, и, как следствие, они могут осесть на дно контейнера, что называется седиментацией . В качестве альтернативы, в концентрированных суспензиях может образовываться коллоидный гель , который изменяет свои реологические свойства . Обратный процесс, при котором агломераты частиц повторно диспергируются в виде отдельных частиц, называемый пептизацией , вряд ли происходит спонтанно, но может происходить при перемешивании или сдвиге .
Коллоидные частицы также могут оставаться диспергированными в жидкостях в течение длительных периодов времени (от нескольких дней до нескольких лет). Это явление называется коллоидной стабильностью , и такая суспензия считается функционально стабильной . Стабильные суспензии часто получаются при низких концентрациях соли или путем добавления химических веществ, называемых стабилизаторами или стабилизирующими агентами . Стабильность частиц, коллоидных или иных, чаще всего оценивается с точки зрения дзета-потенциала . Этот параметр обеспечивает легко поддающуюся количественной оценке меру отталкивания между частицами, которое является ключевым ингибитором агрегации частиц.
Аналогичные процессы агломерации происходят и в других дисперсных системах. В эмульсиях они также могут быть связаны с коалесценцией капель и приводить не только к седиментации, но и к сливкообразованию . В аэрозолях частицы в воздухе могут в равной степени объединяться и образовывать более крупные кластеры (например, сажу ).
Хорошо диспергированная коллоидная суспензия состоит из отдельных, разделенных частиц и стабилизируется отталкивающими межчастичными силами. Когда отталкивающие силы ослабевают или становятся притягивающими за счет добавления коагулянта, частицы начинают агрегировать. Первоначально из синглетов A 1 будут образовываться дублеты частиц A 2 по схеме [2]
На ранней стадии процесса агрегации суспензия в основном содержит отдельные частицы. Скорость этого явления характеризуется коэффициентом скорости агрегации k . Поскольку образование дублетов является процессом скорости второго порядка , единицами этого коэффициента являются м 3 с −1 , поскольку концентрации частиц выражаются как число частиц на единицу объема (м −3 ). Поскольку абсолютные скорости агрегации трудно измерить, часто ссылаются на безразмерный коэффициент устойчивости W , определяемый как , где k fast — коэффициент скорости агрегации в быстром режиме, а k — коэффициент при интересующих условиях. Коэффициент устойчивости близок к единице в быстром режиме, увеличивается в медленном режиме и становится очень большим, когда суспензия стабильна.
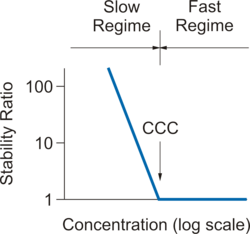
Часто коллоидные частицы суспендируют в воде. В этом случае они накапливают поверхностный заряд , и вокруг каждой частицы образуется двойной электрический слой . [3] Перекрытие диффузных слоев двух сближающихся частиц приводит к отталкивающему потенциалу взаимодействия двойного слоя , что приводит к стабилизации частицы. При добавлении соли в суспензию отталкивание двойного электрического слоя экранируется, а притяжение Ван-дер-Ваальса становится доминирующим и вызывает быструю агрегацию. На рисунке справа показана типичная зависимость коэффициента устойчивости W от концентрации электролита, где обозначены режимы медленной и быстрой агрегации.
В таблице ниже приведены диапазоны критической концентрации коагуляции (ККК) для различного чистого заряда противоиона . [ 4] Заряд выражается в единицах элементарного заряда . Эта зависимость отражает правило Шульце-Харди, [5] [6], которое гласит, что ККК изменяется как обратная шестая степень заряда противоиона. ККК также в некоторой степени зависит от типа иона, даже если они несут одинаковый заряд. Эта зависимость может отражать различные свойства частиц или различное сродство ионов к поверхности частиц. Поскольку частицы часто имеют отрицательный заряд, многовалентные катионы металлов, таким образом, представляют собой высокоэффективные коагулянты.
Адсорбция противоположно заряженных частиц (например, протонов, специфически адсорбирующихся ионов, поверхностно-активных веществ или полиэлектролитов ) может дестабилизировать суспензию частиц за счет нейтрализации заряда или стабилизировать ее за счет накопления заряда, что приводит к быстрой агрегации вблизи точки нейтрализации заряда и медленной агрегации вдали от нее.
Количественная интерпретация коллоидной стабильности была впервые сформулирована в рамках теории ДЛФО . [2] Эта теория подтверждает существование режимов медленной и быстрой агрегации, хотя в медленном режиме зависимость от концентрации соли часто предсказывается как гораздо более сильная, чем наблюдается экспериментально. Правило Шульце-Харди также может быть выведено из теории ДЛФО.
Другие механизмы коллоидной стабилизации также возможны, в частности, с участием полимеров. Адсорбированные или привитые полимеры могут образовывать защитный слой вокруг частиц, вызывать стерические силы отталкивания и приводить к стерической стабилизации, как это происходит с поликарбоксилатным эфиром (PCE), последним поколением химически адаптированных суперпластификаторов, специально разработанных для повышения удобоукладываемости бетона при одновременном снижении содержания в нем воды для улучшения его свойств и долговечности. Когда полимерные цепи адсорбируются на частицах неплотно, полимерная цепь может образовывать мостики между двумя частицами и вызывать мостиковые силы. Эта ситуация называется мостиковой флокуляцией.
Когда агрегация частиц происходит исключительно за счет диффузии, говорят о перикинетической агрегации. Агрегация может быть усилена посредством напряжения сдвига (например, перемешивания). Последний случай называется ортокинетической агрегацией.
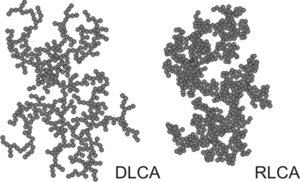
По мере продолжения процесса агрегации образуются более крупные кластеры. Рост происходит в основном за счет столкновений между различными кластерами, и поэтому говорят о процессе агрегации кластер-кластер. Полученные кластеры нерегулярны, но статистически самоподобны. Они являются примерами массовых фракталов , в которых их масса M растет с их типичным размером, характеризуемым радиусом инерции R g как степенной закон [2]
где d — массовая фрактальная размерность. В зависимости от того, быстрая или медленная агрегация, говорят о диффузионно-ограниченной кластерной агрегации (DLCA) или реакционно-ограниченной кластерной агрегации (RLCA). Кластеры имеют разные характеристики в каждом режиме. Кластеры DLCA рыхлые и разветвленные ( d ≈ 1,8), тогда как кластеры RLCA более компактны ( d ≈ 2,1). [7] Распределение размеров кластеров также различается в этих двух режимах. Кластеры DLCA относительно монодисперсны, тогда как распределение размеров кластеров RLCA очень широкое.
Чем больше размер кластера, тем выше скорость их осаждения. Поэтому агрегирующие частицы оседают, и этот механизм обеспечивает способ их отделения от суспензии. При более высоких концентрациях частиц растущие кластеры могут сцепляться и образовывать гель частиц. Такой гель является упругим твердым телом, но отличается от обычных твердых тел очень низким модулем упругости .
Когда агрегация происходит в суспензии, состоящей из одинаковых монодисперсных коллоидных частиц, процесс называется гомоагрегацией (или гомокоагуляцией). Когда агрегация происходит в суспензии, состоящей из разнородных коллоидных частиц, говорят о гетероагрегации (или гетерокоагуляции ) . Самый простой процесс гетероагрегации происходит, когда смешиваются два типа монодисперсных коллоидных частиц. На ранних стадиях могут образовываться три типа дублетов: [8]
В то время как первые два процесса соответствуют гомоагрегации в чистых суспензиях, содержащих частицы A или B, последняя реакция представляет собой фактический процесс гетероагрегации. Каждая из этих реакций характеризуется соответствующими коэффициентами агрегации k AA , k BB и k AB . Например, когда частицы A и B несут положительный и отрицательный заряд соответственно, скорости гомоагрегации могут быть медленными, в то время как скорость гетероагрегации - быстрой. В отличие от гомоагрегации, скорость гетероагрегации ускоряется с уменьшением концентрации соли. Кластеры, образованные на более поздних стадиях таких процессов гетероагрегации, еще более разветвлены, чем те, которые получены во время DLCA ( d ≈ 1,4). [9]
Важным частным случаем процесса гетероагрегации является осаждение частиц на субстрате. [1] Ранние стадии процесса соответствуют прикреплению отдельных частиц к субстрату, который может быть изображен как другая, гораздо более крупная частица. Более поздние стадии могут отражать блокировку субстрата посредством отталкивающих взаимодействий между частицами, в то время как притягивающие взаимодействия могут приводить к многослойному росту, и также называются созреванием. Эти явления имеют отношение к загрязнению мембран или фильтров .
Для изучения агрегации частиц были разработаны многочисленные экспериментальные методы. Наиболее часто используются оптические методы с временным разрешением, основанные на пропускании или рассеянии света. [10]
Пропускание света. Изменение прошедшего света через агрегирующую суспензию можно изучать с помощью обычного спектрофотометра в видимой области. По мере агрегации среда становится более мутной, а ее поглощение увеличивается. Увеличение поглощения можно связать с константой скорости агрегации k , а коэффициент устойчивости можно оценить из таких измерений. Преимущество этого метода в его простоте.
Рассеяние света. Эти методы основаны на зондировании рассеянного света от агрегирующей суспензии с временным разрешением. Статическое рассеяние света дает изменение интенсивности рассеяния, в то время как динамическое рассеяние света — изменение кажущегося гидродинамического радиуса. На ранних стадиях агрегации изменение каждой из этих величин прямо пропорционально константе скорости агрегации k . [11] На более поздних стадиях можно получить информацию об образованных кластерах (например, фрактальную размерность). [7] Рассеяние света хорошо работает для широкого диапазона размеров частиц. Возможно, придется учитывать эффекты многократного рассеяния, поскольку рассеяние становится все более важным для более крупных частиц или более крупных агрегатов. Такими эффектами можно пренебречь в слабомутных суспензиях. Процессы агрегации в сильно рассеивающих системах изучались с помощью методов пропускания , обратного рассеяния или спектроскопии диффузионных волн .
Подсчет отдельных частиц. Этот метод обеспечивает превосходное разрешение, благодаря чему кластеры, состоящие из десятых долей частиц, могут быть разделены индивидуально. [11] Агрегирующая суспензия продавливается через узкий капиллярный счетчик частиц , а размер каждого агрегата анализируется с помощью рассеяния света. Из интенсивности рассеяния можно вывести размер каждого агрегата и построить подробное распределение размеров агрегатов. Если суспензии содержат большое количество соли, можно также использовать счетчик Коултера . С течением времени распределение размеров смещается в сторону более крупных агрегатов, и из этого изменения можно вывести скорости агрегации и распада, включающие различные кластеры. Недостатком метода является то, что агрегаты продавливаются через узкий капилляр при высоком сдвиге, и агрегаты могут разрушаться в этих условиях.
Косвенные методы. Поскольку многие свойства коллоидных суспензий зависят от состояния агрегации взвешенных частиц, для мониторинга агрегации частиц также использовались различные косвенные методы. Хотя получение количественной информации о скоростях агрегации или свойствах кластеров из таких экспериментов может быть затруднительным, они могут быть наиболее ценными для практического применения. Среди этих методов наиболее актуальными являются тесты на осаждение. Когда осматривают ряд пробирок с суспензиями, приготовленными при различной концентрации флокулянта, стабильные суспензии часто остаются диспергированными, в то время как нестабильные оседают. Были разработаны автоматизированные приборы на основе рассеяния/пропускания света для мониторинга осаждения суспензии, и их можно использовать для исследования агрегации частиц. Однако следует понимать, что эти методы не всегда могут правильно отражать фактическое состояние агрегации суспензии. Например, более крупные первичные частицы могут осаждаться даже при отсутствии агрегации, или агрегаты, которые образовали коллоидный гель, останутся во взвешенном состоянии. Другие косвенные методы, позволяющие контролировать состояние агрегата, включают, например, фильтрацию , реологию , поглощение ультразвуковых волн или диэлектрические свойства . [10]
Агрегация частиц — широко распространенное явление, которое спонтанно происходит в природе, но также широко изучается в производстве. Вот некоторые примеры.
Формирование дельты реки . Когда речная вода, несущая взвешенные частицы осадка, достигает соленой воды, агрегация частиц может быть одним из факторов, ответственных за формирование дельты реки. Заряженные частицы стабильны в пресной воде реки, содержащей низкий уровень соли, но они становятся нестабильными в морской воде, содержащей высокий уровень соли. В последней среде частицы агрегируются, более крупные агрегаты осаждаются и таким образом создают дельту реки.
Изготовление бумаги . В пульпу добавляются удерживающие добавки для ускорения формирования бумаги. Эти добавки являются коагулирующими добавками, которые ускоряют агрегацию между волокнами целлюлозы и частицами наполнителя. Часто для этой цели используют катионные полиэлектролиты.
Очистка воды . Очистка городских сточных вод обычно включает фазу, на которой удаляются мелкие твердые частицы. Это разделение достигается путем добавления флокулянта или коагулирующего агента, который вызывает агрегацию взвешенных твердых частиц. Агрегаты обычно разделяются путем осаждения, что приводит к образованию канализационного ила. Обычно используемые флокулянты при очистке воды включают многовалентные ионы металлов (например, Fe 3+ или Al 3+ ), полиэлектролиты или и то, и другое.
Производство сыра . Ключевым этапом в производстве сыра является разделение молока на твердый творог и жидкую сыворотку. Это разделение достигается путем индуцирования процессов агрегации между мицеллами казеина путем подкисления молока или добавления сычужного фермента. Подкисление нейтрализует карбоксилатные группы на мицеллах и вызывает агрегацию.