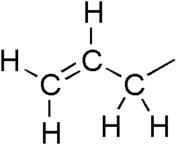
В органической химии аллильная группа представляет собой заместитель со структурной формулой –CH 2 –HC=CH 2 . Он состоит из метиленового мостика ( -CH 2 - ), присоединенного к винильной группе ( -CH=CH 2 ). [1] [2] Название происходит от научного названия чеснока Allium sativum . В 1844 году Теодор Вертхайм выделил из чесночного масла аллильное производное и назвал его « Швефелаллил ». [3] [4] Термин «аллил» применяется ко многим соединениям, связанным с H 2 C=CH-CH 2 , некоторые из которых имеют практическое или повседневное значение, например, аллилхлорид .
Аллилирование – это любая химическая реакция , в ходе которой к субстрату добавляется аллильная группа . [1]
Участок, соседний с ненасыщенным атомом углерода, называется аллильным положением или аллильным участком . Группу, прикрепленную к этому сайту, иногда называют allylic . Таким образом, CH 2 =CHCH 2 OH «имеет аллильную гидроксильную группу ». Аллильные связи C-H примерно на 15% слабее, чем связи C-H в обычных углеродных центрах sp 3 и, следовательно, более реакционноспособны.
Бензильная и аллильная кислоты родственны по структуре, силе связи и реакционной способности. Другими реакциями, которые имеют тенденцию происходить с аллильными соединениями, являются аллильное окисление , еновые реакции и реакция Цуджи-Троста . Бензильные группы родственны аллильным группам; оба демонстрируют повышенную реактивность.
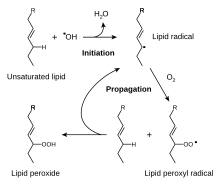
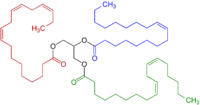
Группа CH 2 , соединенная с двумя винильными группами, называется двойной аллильной. Энергия диссоциации связей C-H на двуаллильном центре примерно на 10% меньше энергии диссоциации связи C-H, которая является аллильной. Ослабленные связи С-Н отражают высокую стабильность образующихся пентадиенильных радикалов. Соединения, содержащие связи C=C-CH 2 -C=C , например производные линолевой кислоты , склонны к автоокислению, что может привести к полимеризации или образованию полутвердых веществ. Эта модель реактивности является фундаментальной для пленкообразующего поведения « олифы », которые являются компонентами масляных красок и лаков .
Термин гомоаллильный относится к положению на углеродном скелете рядом с аллильным положением. В бут-3-енилхлориде CH 2 =CHCH 2 CH 2 Cl хлорид является гомоаллильным, поскольку он связан с гомоаллильным участком.

Аллильная группа широко встречается в органической химии. [1] Аллильные радикалы , анионы и катионы часто рассматриваются как промежуточные соединения в реакциях . Все они имеют три смежных sp²-гибридных углеродных центра и все обеспечивают стабильность за счет резонанса. [5] Каждый вид может быть представлен двумя резонансными структурами с зарядом или неспаренным электроном, распределенным в обеих позициях 1,3.

С точки зрения теории МО , диаграмма МО имеет три молекулярные орбитали: первая связывающая, вторая несвязывающая и орбиталь с более высокой энергией является разрыхляющей. [2]

[6]
Эта повышенная реактивность аллильных групп имеет множество практических последствий. Вулканизация серой различных каучуков использует преобразование аллильных групп CH 2 в сшивки CH-S x -CH . Аналогично олифы, такие как льняное масло, сшиваются посредством окисления аллильных (или дважды аллильных) участков. Это сшивание лежит в основе свойств красок и порчи пищевых продуктов из-за прогоркания .
В промышленном производстве акрилонитрила путем аммоксидирования пропена используется легкое окисление аллильных центров C-H:
По оценкам, 800 000 тонн (1997 г.) аллилхлорида производится путем хлорирования пропилена :
Это предшественник аллилового спирта и эпихлоргидрина .
Аллирование — это присоединение аллильной группы к субстрату, обычно другому органическому соединению. Классически аллилирование включает реакцию карбаниона с аллилхлоридом. Альтернативы включают аллилирование карбонила с помощью аллилметаллических реагентов, таких как аллилтриметилсилан , [7] [8] [9] или катализируемое иридием аллилирование Крише .
Аллилирование может осуществляться также путем сопряженного присоединения : присоединения аллильной группы к бета-положению енона . Реакция Хосоми -Сакураи является распространенным методом сопряженного аллилирования. [10]
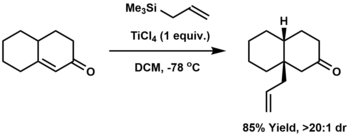
К аллильной группе можно присоединить множество заместителей, образуя стабильные соединения. Коммерчески важные аллильные соединения включают:
{{cite journal}}: CS1 maint: multiple names: authors list (link)