Альфа-кератин , или α-кератин, представляет собой тип кератина , обнаруженного у позвоночных млекопитающих . Этот белок является основным компонентом волос , рогов , когтей , ногтей и слоя эпидермиса кожи . Альфа-кератин представляет собой волокнистый структурный белок , то есть он состоит из аминокислот , которые образуют повторяющуюся вторичную структуру. Вторичная структура α-кератина очень похожа на структуру традиционной белковой α-спирали и образует спиральную спираль . [1] Благодаря своей плотно намотанной структуре он может функционировать как один из самых прочных биологических материалов и выполняет различные функции у млекопитающих: от хищных когтей до волос для согрева. α-кератин синтезируется посредством биосинтеза белка с использованием транскрипции и трансляции , но по мере того, как клетка созревает и наполняется α-кератином, она умирает, создавая прочную несосудистую единицу кератинизированной ткани . [2]

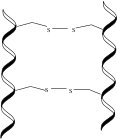
α-кератин представляет собой полипептидную цепь , обычно с высоким содержанием аланина , лейцина , аргинина и цистеина , которая образует правостороннюю α-спираль . [3] [4] Две из этих полипептидных цепей скручиваются вместе, образуя левостороннюю спиральную структуру, известную как спиральная спираль . Эти спиральные димеры длиной примерно 45 нм связаны между собой дисульфидными связями с использованием многих аминокислот цистеина, содержащихся в α-кератинах . [2] Затем димеры выравниваются, их концы соединяются с концами других димеров, и две из этих новых цепей соединяются по длине, все через дисульфидные связи, образуя протофиламент. [5] Два протофиламента объединяются с образованием протофибриллы, а четыре протофибриллы полимеризуются с образованием промежуточной нити (IF). IF является основной субъединицей α-кератинов. Эти IF способны конденсироваться в образование суперклубка диаметром около 7 нм и могут быть типа I , кислого, или типа II , основного. В конечном итоге IF внедряются в кератиновый матрикс , который богат либо цистеином , либо остатками глицина , тирозина и фенилаланина . Различные типы, расположение и матрицы этих IFs объясняют большие различия в структурах α-кератина, обнаруженных у млекопитающих. [6]
Синтез α-кератина начинается вблизи фокальных спаек на клеточной мембране . Там предшественники кератиновых нитей проходят процесс, известный как нуклеация , при котором предшественники кератиновых димеров и нитей удлиняются, сливаются и связываются вместе. [2] Во время этого синтеза предшественники кератиновых нитей транспортируются актиновыми волокнами в клетке по направлению к ядру . Там промежуточные нити альфа-кератина будут собираться и формировать сети структур, диктуемые использованием кератиновой клетки, когда ядро одновременно деградирует. [7] Однако, при необходимости, вместо того, чтобы продолжать расти, кератиновый комплекс разбирается на ненитевидные предшественники кератина, которые могут диффундировать по цитоплазме клетки . Эти кератиновые нити можно будет использовать в будущем синтезе кератина либо для реорганизации окончательной структуры, либо для создания другого кератинового комплекса. Когда клетка наполнена правильным кератином и правильно структурирована, она подвергается стабилизации кератина и умирает, что является формой запрограммированной гибели клеток . В результате образуются полностью созревшие бессосудистые кератиновые клетки. [8] Эти полностью созревшие или ороговевшие клетки альфа-кератина являются основными компонентами волос, внешнего слоя ногтей и рогов, а также слоя эпидермиса кожи. [9]
Наиболее биологически важным свойством альфа-кератина является его структурная стабильность. Под воздействием механического воздействия структуры α-кератина могут сохранять свою форму и, следовательно, защищать то, что их окружает. [10] При сильном натяжении альфа-кератин может даже превратиться в бета-кератин , более сильное кератиновое образование, имеющее вторичную структуру бета-складчатых пластинок . [11] Ткани альфа-кератина также демонстрируют признаки вязкоэластичности , что позволяет им растягиваться и в некоторой степени поглощать удары, хотя они не защищены от переломов . На прочность альфа-кератина также влияет содержание воды в матрице промежуточных нитей; более высокое содержание воды снижает прочность и жесткость кератиновой клетки из-за ее влияния на различные водородные связи в сети альфа-кератина. [2]
Белки альфа-кератины могут быть одного из двух типов: типа I или типа II . У человека имеется 54 гена кератина, 28 из которых кодируют тип I, а 26 — тип II. [12] Белки типа I являются кислыми, то есть содержат больше кислых аминокислот, таких как аспарагиновая кислота , тогда как белки типа II являются основными, то есть содержат больше основных аминокислот, таких как лизин . [13] Эта дифференциация особенно важна для альфа-кератинов, потому что при синтезе его субъединичного димера, спиральной спирали , одна белковая спираль должна быть типа I, а другая - типа II. [2] Даже в типах I и II существуют кислые и основные кератины, которые особенно дополняют друг друга в каждом организме. Например, в коже человека K5 , альфа-кератин типа II, в основном соединяется с K14 , альфа-кератином типа I, образуя альфа-кератиновый комплекс слоя клеток эпидермиса кожи. [14]
Твердые альфа-кератины, например те, которые содержатся в ногтях, имеют более высокое содержание цистеина в своей первичной структуре . Это вызывает увеличение количества дисульфидных связей , которые способны стабилизировать структуру кератина, позволяя ему противостоять более высокому уровню силы перед разрушением. С другой стороны, мягкие альфа-кератины, например те, что содержатся в коже, содержат сравнительно меньшее количество дисульфидных связей, что делает их структуру более гибкой. [1]
{{cite book}}: CS1 maint: несколько имен: список авторов ( ссылка )