
Аналептик в медицине является стимулятором центральной нервной системы . Термин «аналептик» обычно относится к стимуляторам дыхания (например, доксапраму ). Аналептики — это стимуляторы центральной нервной системы (ЦНС), которые включают широкий спектр лекарств, используемых для лечения депрессии, синдрома дефицита внимания и гиперактивности ( СДВГ ) и угнетения дыхания . Аналептики также можно использовать в качестве противосудорожных средств , при этом низкие дозы вызывают у пациентов повышенное внимание, беспокойство и учащенное дыхание . [1] Основное медицинское применение этих препаратов — в качестве средства восстановления после анестезии или для лечения неотложной депрессии дыхания . [2] Другими препаратами этой категории являются преткамид , пентилентетразол и никетамид . Никетамид в настоящее время отменен из-за риска судорог. Аналептики недавно стали использоваться для лучшего понимания лечения передозировки барбитуратов . Благодаря использованию агентов исследователи смогли лечить оглушение и угнетение дыхания. [3]

На протяжении всей истории аналептики использовались для двух основных целей: помочь пациентам более эффективно восстановиться после наркоза и справиться с респираторным дистрессом и апноэ, особенно у младенцев.
Аналептики можно использовать для ускорения выздоровления от пропофола , ремифентанила и севофлурана . В клинических условиях аналептики, такие как доксапрам, использовались, чтобы помочь пациентам лучше восстановиться после наркоза, а также для устранения некоторых потенциальных негативных побочных эффектов сильнодействующих анестетиков.
Три наиболее распространенных клинических аналептических применения кофеина — это лечение астмы , апноэ недоношенных и бронхолегочной дисплазии у новорожденных. [4] Кофеин является слабым бронходилятатором , что объясняет облегчение последствий астмы. Некоторые предварительные исследования показывают, что кофеин снижает заболеваемость церебральным параличом и задержкой когнитивных функций, но необходимы дополнительные исследования. [5] Апноэ недоношенных официально описывается как остановка дыхания более чем на 15–20 секунд, обычно сопровождающаяся брадикардией и гипоксией . [6] Эта остановка дыхания происходит из-за недоразвития центра управления дыханием, продолговатого мозга , у недоношенных детей.
Обширные исследования также показывают, что кофеин значительно снижает возникновение бронхолегочной дисплазии, которая представляет собой хроническое заболевание легких, обусловленное потребностью в дополнительном кислороде после 36-недельного постменструального периода. [6] Бронхолегочная дисплазия часто встречается у младенцев с низкой массой тела при рождении (<2500 г) и очень низкой массой тела при рождении (<1500 г), которым были подключены аппараты искусственной вентиляции легких для лечения респираторного дистресс-синдрома . В настоящее время методы лечения бронхолегочной дисплазии не известны, поскольку считается, что риски лечения перевешивают необходимость использования аппарата искусственной вентиляции легких. Кофеин только снижает возникновение.
Теофиллин больше не используется в качестве респираторного аналептика у новорожденных. Теофиллин имеет очень узкий терапевтический индекс, поэтому его дозировку необходимо контролировать путем прямого измерения уровня теофиллина в сыворотке, чтобы избежать токсичности.
Аналептики представляют собой разнообразную группу лекарств, которые действуют различными химическими путями; аналептики действуют через четыре основных механизма стимуляции дыхания. Аналептики могут действовать как блокаторы калиевых каналов , ампакины , агонисты рецепторов серотонина и антагонисты аденозина .
Двумя распространенными блокаторами калиевых каналов являются доксапрам и GAL-021 . Оба действуют на калиевые каналы в каротидных тельцах . Эти клетки отвечают за восприятие низких концентраций кислорода и передачу информации в ЦНС, что в конечном итоге приводит к усилению дыхания. Блокирование калиевых каналов на мембранах этих клеток эффективно деполяризует мембранный потенциал , что, в свою очередь, приводит к открытию потенциалзависимых кальциевых каналов и высвобождению нейромедиаторов. Это начинает процесс передачи сигнала в ЦНС. Доксапрам блокирует протекающие калиевые каналы в семействе калиевых каналов тандомного порового домена, в то время как GAL-021 блокирует BK-каналы или большие калиевые каналы, которые активируются изменением электронного потенциала мембраны или увеличением внутреннего кальция. [7]
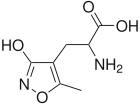
Ампакины являются второй распространенной формой аналептиков, которая вызывает другой механизм аналептического ответа. Они связываются с рецепторами AMPA или альфа-амино-3-гидрокси-5-метил-4-изоксазолпропионатными рецепторами в составе пре-Бетцингеровского комплекса . Пре-Бетцингеровский комплекс входит в состав вентральной дыхательной группы и индукция долговременных потенциалов в постсинаптической мембране этих нейронов приводит к увеличению частоты дыхания. Эндогенным лигандом рецептора AMPA является глутамат , а ампакины отражают взаимодействие глутамата с рецепторами. Связывание лиганда приводит к открытию рецепторов AMPA и позволяет ионам натрия проникать в клетку, что приводит к деполяризации и передаче сигнала . На данный момент CX717 является наиболее успешным ампакином в испытаниях на людях и имеет очень мало побочных эффектов. [7]
Третий общий механизм, которым пользуются аналептики, — это действие агонистов рецепторов серотонина. Буспирон и мозаприд успешно усиливают дыхание у животных путем связывания с рецепторами серотонина, которые представляют собой рецепторы, связанные с G-белком , которые при активации индуцируют каскад вторичных мессенджеров, и в данном случае этот каскад приводит к аналептической реакции. [7]
Что касается дыхания, кофеин действует как конкурентный антагонист аденозина . Исследователи обнаружили это, вводя аденозин или его производные, и обнаружили, что эффекты были противоположны эффектам кофеина. Известно, что повышенный уровень аденозина вызывает угнетение спонтанной электрической активности нейронов, торможение нейротрансмиссии и снижение высвобождения нейромедиаторов. Аденозин подавляет дыхательную активность, блокируя электрическую активность дыхательных нейронов. [8] Кофеин, как антагонист аденозина, стимулирует эти дыхательные нейроны, вызывая увеличение минутного объема дыхания .
Доксапрам представляет собой внутривенный стимулятор ЦНС и дыхания, который обычно используется для лечения угнетения дыхания, вызванного анестезией или хронической обструктивной болезнью легких . Его также можно использовать для лечения неонатального апноэ , но оно может быть опасным, поэтому следует соблюдать осторожность. Доксапрам использовался для лечения угнетения дыхания при передозировке наркотиков , но для многих лекарств он неэффективен. Побочные эффекты доксапрама редки, но при передозировке наблюдалось возникновение гипертензии , тахикардии , тремора , спастичности и гиперактивных рефлексов . [9]

Встречающиеся в природе соединения кофеин и теофиллин структурно классифицируются как метилированные ксантины . Побочные эффекты, обычно наблюдаемые при использовании ксантинов, включают нервное возбуждение, чрезмерную энергичность и бессонницу . Менее распространенные побочные эффекты могут включать диурез , раздражение желудочно-кишечного тракта и редко звон в ушах . В высоких дозах они также могут вызывать психологическую зависимость . [9]
После их появления в начале 20-го века аналептики использовались для изучения новой опасной для жизни проблемы передозировки барбитуратов . До 1930-х годов для лечения передозировки барбитуратами использовались природные стимуляторы, такие как камфора и кофеин . [10] Между 1930 и 1960 годами синтетические аналептики, такие как никетамид , пентилентетразол , бемегрид , амфетамин и метилфенидат, заменили встречающиеся в природе соединения при лечении передозировки барбитуратов . В последнее время аналептики стали использовать для лечения СДВГ из-за более эффективных способов лечения передозировки барбитуратов. [11]
Одним из первых широко применяемых аналептиков был стрихнин , вызывающий возбуждение ЦНС путем антагонизма тормозного нейромедиатора глицина . [1] Стрихнин относится к категории противосудорожных средств наряду с пикротоксином и бикукуллином , хотя эти противосудорожные вещества ингибируют рецепторы ГАМК , а не глицина. Стрихнин использовался до начала 20 века, когда было обнаружено, что он является высокотоксичным противосудорожным средством. Стрихнин теперь доступен в качестве родентицида и в качестве примеси в таких наркотиках, как героин . [1] Два других конвульсанта противодействуют рецепторам ГАМК, но ни один из них сегодня широко не доступен. [1]
Использование доксапрама у людей сокращается, хотя он является эффективным стимулятором ЦНС и дыхания, в первую очередь из-за того, что анестетики более короткого действия становятся все более распространенными, а также потому, что некоторые исследования показали потенциальные побочные эффекты у младенцев. [2] [12] Некоторые исследования недоношенных детей показали, что доксапрам вызывает снижение мозгового кровотока и увеличение потребности мозга в кислороде. Это привело к тому, что у этих младенцев был более высокий риск развития задержки умственного развития, чем у младенцев, не получавших препарат. [2] Таким образом, доксапрам был исключен из многих методов лечения людей из-за его потенциальной опасности.