Аргон — химический элемент ; он имеет символ Ar и атомный номер 18. Он находится в 18-й группе периодической таблицы и является благородным газом . [9] Аргон является третьим по распространенности газом в атмосфере Земли , его содержание составляет 0,934% (9340 ppmv ). Его более чем в два раза больше, чем водяного пара (который в среднем составляет около 4000 ppmv, но сильно варьируется), в 23 раза больше, чем углекислого газа (400 ppmv), и более чем в 500 раз больше, чем неона (18 ppmv). Аргон — самый распространенный благородный газ в земной коре , составляющий 0,00015% земной коры.
Почти весь аргон в атмосфере Земли представляет собой радиогенный аргон-40 , образующийся в результате распада калия -40 в земной коре. Во Вселенной аргон-36 на сегодняшний день является наиболее распространенным изотопом аргона , поскольку его легче всего производить в результате звездного нуклеосинтеза в сверхновых .
Название «аргон» происходит от греческого слова ἀργόν , формы среднего единственного числа от ἀργός , означающего «ленивый» или «неактивный», что указывает на тот факт, что элемент почти не вступает в химические реакции. Полный октет (восемь электронов) во внешней атомной оболочке делает аргон стабильным и устойчивым к связыванию с другими элементами. Температура тройной точки 83,8058 К является определяющей фиксированной точкой Международной температурной шкалы 1990 года .
Аргон добывают в промышленности путем фракционной перегонки жидкого воздуха . В основном он используется в качестве инертного защитного газа при сварке и других высокотемпературных промышленных процессах, где обычно нереактивные вещества становятся реактивными; например, в графитовых электропечах используется атмосфера аргона, чтобы предотвратить горение графита. Он также используется в лампах накаливания , люминесцентных лампах и других газоразрядных лампах. Он производит характерный сине-зеленый газовый лазер . Он также используется в люминесцентных тлеющих стартёрах.

Аргон имеет примерно такую же растворимость в воде, как и кислород, и в 2,5 раза лучше растворяется в воде, чем азот . Аргон бесцветен, не имеет запаха, негорюч и нетоксичен в твердом, жидком или газообразном состоянии. [10] Аргон химически инертен в большинстве условий и не образует подтвержденных стабильных соединений при комнатной температуре.
Хотя аргон является благородным газом , он может образовывать некоторые соединения в различных экстремальных условиях. Был продемонстрирован фторгидрид аргона (HArF), соединение аргона с фтором и водородом , стабильное при температуре ниже 17 К (-256,1 ° C; -429,1 ° F). [11] [12] Хотя нейтральные химические соединения аргона в основном состоянии в настоящее время ограничены HArF, аргон может образовывать клатраты с водой, когда атомы аргона захватываются решеткой молекул воды. [13] Ионы , такие как ArH+
и комплексы в возбужденном состоянии , такие как ArF, были продемонстрированы. Теоретический расчет предсказывает еще несколько соединений аргона , которые должны быть стабильными [14], но пока не синтезированы.

Аргон ( греческий ἀργόν , форма среднего единственного числа от ἀργός , что означает «ленивый» или «неактивный») назван в честь его химической неактивности. Это химическое свойство первого открытого благородного газа произвело впечатление на авторов названия. [15] [16] Генри Кавендиш в 1785 году подозревал, что инертный газ является компонентом воздуха. [17]
Аргон был впервые выделен из воздуха в 1894 году лордом Рэлеем и сэром Уильямом Рамзи в Университетском колледже Лондона путем удаления кислорода , углекислого газа , воды и азота из образца чистого воздуха. [18] [19] [20] Впервые они добились этого, повторив эксперимент Генри Кавендиша . Они поймали смесь атмосферного воздуха с дополнительным кислородом в перевернутой пробирке (А) над большим количеством разбавленного раствора щелочи (Б), которым в первоначальном эксперименте Кавендиша был гидроксид калия [17] , и пропустили ток через провода изолированы U-образными стеклянными трубками (СС), которые герметизируются вокруг платиновых проволочных электродов, оставляя концы проводов (DD) открытыми для газа и изолированными от раствора щелочи. Дуга питалась от батареи из пяти элементов Гроува и катушки Румкорфа среднего размера. Щелочь поглотила образующиеся при дуге оксиды азота, а также углекислый газ. Они эксплуатировали дугу до тех пор, пока в течение часа или двух не прекращалось уменьшение объема газа, а спектральные линии азота не исчезали при исследовании газа. Оставшийся кислород подвергся реакции со щелочным пирогаллатом, в результате чего остался явно нереакционноспособный газ, который они назвали аргоном.

Прежде чем изолировать газ, они определили, что азот, полученный из химических соединений, на 0,5% легче азота из атмосферы. Разница была незначительной, но она была достаточно важной, чтобы привлечь их внимание на многие месяцы. Они пришли к выводу, что в воздухе был смешанный с азотом еще один газ. [21] Аргон также был обнаружен в 1882 году благодаря независимым исследованиям Х. Ф. Ньюолла и У. Н. Хартли. [22] Каждый из них наблюдал новые линии в спектре излучения воздуха, которые не соответствовали известным элементам.
До 1957 года символом аргона была «А», но теперь это «Ar». [23]
Аргон составляет 0,934% по объему и 1,288% по массе атмосферы Земли . [24] Воздух является основным промышленным источником очищенного аргона. Аргон выделяют из воздуха путем фракционирования, чаще всего с помощью криогенной фракционной перегонки — процесса, в ходе которого также получают очищенный азот , кислород , неон , криптон и ксенон . [25] Земная кора и морская вода содержат 1,2 ppm и 0,45 ppm аргона соответственно. [26]
Основные изотопы аргона, обнаруженные на Земле:40
Ар (99,6%),36
Ar (0,34%) и38
Ар (0,06%). Встречающиеся в природе40
К , с периодом полураспада 1,25 × 109 лет, снижается до стабильного40
Ar (11,2%) путем захвата электронов или эмиссии позитронов , а также до стабильных40
Са (88,8%) путем бета-распада . Эти свойства и соотношения используются для определения возраста пород методом K-Ar датирования . [26] [27]
В атмосфере Земли,39
Ar образуется в результате активности космических лучей , в первую очередь путем захвата нейтронов40
Ar с последующей двухнейтронной эмиссией. В подземной среде он также образуется за счет захвата нейтронов39
K с последующей эмиссией протонов.37
Ar создается в результате захвата нейтронов40
Ca с последующим выбросом альфа-частиц в результате подземных ядерных взрывов . Период полураспада составляет 35 дней. [27]
В разных местах Солнечной системы изотопный состав аргона сильно различается. Если основным источником аргона является распад40К в скалах,40
Ar будет доминирующим изотопом, как и на Земле. В аргоне, производимом непосредственно в результате звездного нуклеосинтеза, преобладает нуклид альфа-процесса.36
Ар . Соответственно, солнечный аргон содержит 84,6%36
Ar (по измерениям солнечного ветра ) [28] , а соотношение трех изотопов 36 Ar : 38 Ar : 40 Ar в атмосферах внешних планет составляет 8400 : 1600 : 1. [29] Это контрастирует с низким содержанием первобытного 36
Содержание Ar в атмосфере Земли составляет всего 31,5 ppmv (= 9340 ppmv × 0,337%), что сравнимо с содержанием неона (18,18 ppmv) на Земле и с межпланетными газами, измеренными зондами .
В атмосферах Марса , Меркурия и Титана (крупнейшего спутника Сатурна ) содержится аргон, преимущественно в виде40
Ар . [30]
Преобладание радиогенных 40
Аргон является причиной того, что стандартный атомный вес земного аргона больше, чем у следующего элемента, калия , и этот факт вызвал недоумение, когда был открыт аргон. Менделеев расположил элементы в своей таблице Менделеева в порядке атомного веса, но инертность аргона предполагала его размещение перед химически активным щелочным металлом . Позже Генри Мозли решил эту проблему, показав, что периодическая таблица на самом деле расположена в порядке атомного номера (см. «История периодической таблицы »).
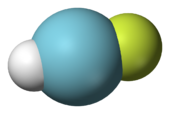
Полный октет электронов аргона указывает на полные подоболочки s и p. Эта полновалентная оболочка делает аргон очень стабильным и чрезвычайно устойчивым к связыванию с другими элементами. До 1962 года аргон и другие благородные газы считались химически инертными и неспособными образовывать соединения; однако с тех пор были синтезированы соединения более тяжелых благородных газов. Первое соединение аргона с пентакарбонилом вольфрама W(CO) 5 Ar было выделено в 1975 году. Однако в то время оно не получило широкого признания. [31] В августе 2000 года другое соединение аргона, фторгидрид аргона (HArF), было получено исследователями из Хельсинкского университета путем освещения ультрафиолетовым светом замороженного аргона, содержащего небольшое количество фторида водорода с йодидом цезия . Это открытие привело к признанию того, что аргон может образовывать слабосвязанные соединения, хотя оно и не было первым. [12] [32] [33] Он стабилен до 17 Кельвинов (-256 ° C). Метастабильный ArCF 2+
2дикатион, валентно- изоэлектронный с карбонилфторидом и фосгеном , наблюдался в 2010 году. [34] Аргон-36 в форме ионов гидрида аргона ( аргония ) был обнаружен в межзвездной среде , связанной со сверхновой Крабовидной туманностью ; это была первая молекула благородного газа, обнаруженная в космическом пространстве . [35] [36]
Твердый гидрид аргона (Ar(H 2 ) 2 ) имеет ту же кристаллическую структуру, что и фаза Лавеса MgZn 2 . Он образуется при давлениях от 4,3 до 220 ГПа, хотя измерения комбинационного рассеяния света показывают, что молекулы H 2 в Ar(H 2 ) 2 диссоциируют при давлении выше 175 ГПа. [37]
Аргон в промышленности выделяют фракционной перегонкой жидкого воздуха в криогенной воздухоразделительной установке; процесс, который отделяет жидкий азот , который кипит при 77,3 К, от аргона, который кипит при 87,3 К, и жидкого кислорода , который кипит при 90,2 К. Ежегодно во всем мире производится около 700 000 тонн аргона. [26] [38]

Аргон имеет несколько полезных свойств:
Другие благородные газы в равной степени подходят для большинства этих применений, но аргон, безусловно, является самым дешевым. Он недорог, поскольку в природе встречается в воздухе и легко получается как побочный продукт криогенного разделения воздуха при производстве жидкого кислорода и жидкого азота : основные компоненты воздуха используются в крупных промышленных масштабах. Другие благородные газы (кроме гелия ) также производятся таким же способом, но аргона, безусловно, больше всего. Основная часть его применений возникает просто потому, что он инертен и относительно дешев.
Аргон используется в некоторых высокотемпературных промышленных процессах, где обычно нереактивные вещества становятся реактивными. Например, в графитовых электропечах используется атмосфера аргона, чтобы предотвратить горение графита.
В некоторых из этих процессов присутствие газов азота или кислорода может вызвать дефекты материала. Аргон используется при некоторых видах дуговой сварки , таких как газовая дуговая сварка и газовая вольфрамовая дуговая сварка , а также при обработке титана и других химически активных элементов. В атмосфере аргона также выращивают кристаллы кремния и германия .
Аргон используется в птицеводстве для удушения птиц либо для массовой выбраковки после вспышек заболеваний, либо в качестве средства убоя, более гуманного, чем оглушение электрическим током . Аргон плотнее воздуха и вытесняет кислород вблизи земли при удушье инертным газом . [39] [40] Его нереактивная природа делает его пригодным для использования в пищевых продуктах, а поскольку он заменяет кислород в мертвой птице, аргон также увеличивает срок хранения. [41]
Аргон иногда используется для тушения пожаров , когда ценное оборудование может быть повреждено водой или пеной. [42]
Жидкий аргон используется в качестве мишени для экспериментов с нейтрино и прямых поисков темной материи . Взаимодействие между гипотетическими вимпами и ядром аргона производит сцинтилляционный свет, который регистрируется фотоумножителями . Двухфазные детекторы, содержащие газообразный аргон, используются для регистрации ионизированных электронов, образующихся во время рассеяния вимпа на ядре. Как и большинство других сжиженных благородных газов, аргон имеет высокий сцинтилляционный световой выход (около 51 фотон/кэВ [43] ), прозрачен для собственного сцинтилляционного света и относительно легко очищается. По сравнению с ксеноном аргон дешевле и имеет четкий профиль времени сцинтилляции, что позволяет отделить электронную отдачу от ядерной. С другой стороны, его собственный фон бета-излучения больше из-за39
Загрязнение аргоном , если только не использовать аргон из подземных источников, у которого гораздо меньше39
Загрязнение аром . Большая часть аргона в атмосфере Земли образовалась в результате захвата электронов долгоживущих40
К (40
К + е − →40
Ar + ν) присутствует в природном калии на Земле.39
Активность Ar в атмосфере поддерживается за счет космогенного производства посредством реакции нокаута.40
Ар (n,2n)39
Ar и подобные реакции. Период полураспада39
Ару всего 269 лет. В результате подземный Ар, экранированный скалами и водой, имеет гораздо меньше39
Загрязнение аром . [44] Детекторы темной материи, работающие в настоящее время с жидким аргоном, включают DarkSide , WArP , ArDM , microCLEAN и DEAP . Нейтринные эксперименты включают ICARUS и MicroBooNE , оба из которых используют жидкий аргон высокой чистоты в камере временной проекции для мелкозернистого трехмерного изображения взаимодействий нейтрино.
В Университете Линчепинга, Швеция, инертный газ используется в вакуумной камере, в которую вводится плазма для ионизации металлических пленок. [45] В результате этого процесса получается пленка, пригодная для производства компьютерных процессоров. Новый процесс устранит необходимость в химических ваннах и использовании дорогих, опасных и редких материалов.

Аргон используется для вытеснения воздуха, содержащего кислород и влагу, в упаковочном материале для продления срока хранения содержимого (аргон имеет европейский код пищевой добавки E938). Воздушное окисление, гидролиз и другие химические реакции, которые разлагают продукты, замедляются или полностью предотвращаются. Химические и фармацевтические препараты высокой чистоты иногда упаковывают и герметизируют в аргоне. [46]
В виноделии аргон используется в различных сферах деятельности, чтобы обеспечить барьер против кислорода на поверхности жидкости, который может испортить вино, стимулируя как микробный метаболизм (как в случае с уксуснокислыми бактериями ), так и стандартную окислительно-восстановительную химию.
Аргон иногда используется в качестве пропеллента в аэрозольных баллончиках.
Аргон также используется в качестве консерванта для таких продуктов, как лак , полиуретан и краска, путем вытеснения воздуха для подготовки контейнера к хранению. [47]
С 2002 года Американский национальный архив хранит важные национальные документы, такие как Декларация независимости и Конституция , в футлярах, наполненных аргоном, чтобы предотвратить их разрушение. Аргон предпочтительнее гелия, который использовался в предыдущие пять десятилетий, поскольку газообразный гелий выходит через межмолекулярные поры в большинстве контейнеров и его необходимо регулярно заменять. [48]

Аргон может использоваться в качестве инертного газа в линиях Шленка и перчаточных боксах . Аргон предпочтительнее менее дорогого азота в тех случаях, когда азот может вступать в реакцию с реагентами или аппаратом.
Аргон может использоваться в качестве газа-носителя в газовой хроматографии и масс-спектрометрии с ионизацией электрораспылением ; это предпочтительный газ для плазмы, используемой в ИСП- спектроскопии . Аргон предпочтителен для нанесения напылением образцов для сканирующей электронной микроскопии . Газообразный аргон также широко используется для напыления тонких пленок в микроэлектронике и для очистки пластин в микропроизводстве .
В процедурах криохирургии , таких как криоабляция, используется жидкий аргон для разрушения тканей, таких как раковые клетки. Он используется в процедуре, называемой «коагуляция с усилением аргона», форме электрохирургии с аргоновой плазмой . Процедура сопряжена с риском газовой эмболии и привела к смерти как минимум одного пациента. [49]
Синие аргоновые лазеры используются в хирургии для сварки артерий, разрушения опухолей и коррекции дефектов глаз. [26]
Аргон также использовался экспериментально для замены азота в дыхательной или декомпрессионной смеси, известной как Аргокс , для ускорения выведения растворенного азота из крови. [50]

Лампы накаливания заполнены аргоном, чтобы предохранить нити накала от окисления при высокой температуре. [51] Он используется для особого способа ионизации и излучения света, например, в плазменных шарах и калориметрии в экспериментальной физике элементарных частиц . Газоразрядные лампы, наполненные чистым аргоном, дают сиреневый/фиолетовый свет; с аргоном и небольшим количеством ртути — синий свет. Аргон также используется в синих и зеленых аргон-ионных лазерах .
Аргон используется для теплоизоляции энергосберегающих окон . [52] Аргон также используется в техническом подводном плавании с аквалангом для надувания сухого костюма, поскольку он инертен и имеет низкую теплопроводность. [53]
Аргон используется в качестве топлива при разработке магнитоплазменной ракеты с переменным удельным импульсом (VASIMR). Сжатому газу аргону разрешено расширяться для охлаждения головок ГСН некоторых версий ракеты AIM-9 Sidewinder и других ракет, в которых используются охлаждаемые тепловые головки ГСН. Газ хранится под высоким давлением . [54]
Аргон-39, период полураспада которого составляет 269 лет, использовался для ряда целей, в первую очередь для датирования ледяных кернов и грунтовых вод . Кроме того, калий-аргоновое датирование и связанное с ним аргон-аргоновое датирование используются для датирования осадочных , метаморфических и магматических пород . [26]
Аргон использовался спортсменами в качестве допинга для имитации гипоксических состояний. В 2014 году Всемирное антидопинговое агентство (ВАДА) добавило аргон и ксенон в список запрещенных веществ и методов, хотя на данный момент надежных тестов на злоупотребление не существует. [55]
Хотя аргон не токсичен, он на 38% плотнее воздуха и поэтому считается опасным удушающим веществом в закрытых помещениях. Его трудно обнаружить, поскольку он бесцветен, не имеет запаха и вкуса. Инцидент 1994 года, когда мужчина задохнулся после того, как вошел в наполненный аргоном участок строящегося нефтепровода на Аляске , подчеркивает опасность утечки аргона из резервуара в замкнутых пространствах и подчеркивает необходимость надлежащего использования, хранения и обращения. [56]
{{cite web}}: CS1 maint: неподходящий URL ( ссылка ){{cite journal}}: CS1 maint: DOI неактивен по состоянию на июнь 2024 г. ( ссылка ){{cite journal}}: CS1 maint: неподходящий URL ( ссылка ){{cite web}}: CS1 maint: числовые имена: список авторов ( ссылка )