Гемофилия B , также называемая гемофилией B , является нарушением свертываемости крови , вызывающим легкое образование синяков и кровотечение из-за наследственной мутации гена фактора IX , и приводящим к дефициту фактора IX. Это встречается реже, чем дефицит фактора VIII ( гемофилия A ). [3]
Гемофилия B была впервые признана как отдельное заболевание в 1952 году. [4] Она также известна под эпонимом болезнь Кристмаса , [1] названная в честь Стивена Кристмаса , первого пациента, у которого была описана гемофилия B. Кроме того, первый отчет о ее идентификации был опубликован в рождественском выпуске British Medical Journal . [4] [5]
Большинство людей, страдающих гемофилией B и испытывающих симптомы, — мужчины. [6] Распространенность гемофилии B среди населения составляет около одного на 40 000; гемофилия B составляет около 15% пациентов с гемофилией. [6] Многие женщины-носители заболевания не имеют симптомов. [6] Однако, по оценкам, у 10-25% женщин-носителей наблюдаются легкие симптомы; в редких случаях у женщин могут быть умеренные или тяжелые симптомы. [6]
Симптомы включают легкое образование синяков , кровотечение из мочевыводящих путей ( гематурия ), носовое кровотечение ( эпистаксис ) и кровотечение в суставы ( гемартроз ). [1]
Пациенты с нарушениями свертываемости крови демонстрируют более высокую заболеваемость пародонтозом, а также кариесом зубов, что связано со страхом кровотечения, что приводит к отсутствию гигиены полости рта и ухода за полостью рта. Наиболее заметным проявлением легкой формы гемофилии B в полости рта будет кровотечение десен во время отшелушивания молочных зубов или длительное кровотечение после инвазивной процедуры/удаления зуба; При тяжелой форме гемофилии может наблюдаться спонтанное кровотечение из тканей полости рта (например, мягкого неба, языка, слизистой оболочки щеки), губ и десен с экхимозами. В редких случаях может наблюдаться гемартроз (кровотечение в суставную щель) височно-нижнечелюстного сустава (ВНЧС). [7]
Пациенты с гемофилией будут испытывать много эпизодов орального кровотечения в течение своей жизни. В среднем 29,1 кровотечений в год достаточно серьезны, чтобы потребовать замены фактора у пациентов с дефицитом F VIII, 9% из которых были связаны с оральными структурами. Дети с тяжелой формой гемофилии имеют значительно более низкую распространенность кариеса зубов и более низкие показатели зубного налета по сравнению с сопоставимыми здоровыми контрольными группами. [8]
Ген фактора IX расположен на Х-хромосоме (Xq27.1-q27.2). Это сцепленный с Х-хромосомой рецессивный признак, что объясняет, почему мужчины страдают в большем количестве. [9] [10]
В 1990 году Джордж Браунли и Мерлин Кроссли показали, что два набора генетических мутаций препятствуют присоединению двух ключевых белков к ДНК людей с редкой и необычной формой гемофилии B – гемофилией B Лейдена , при которой у пациентов наблюдаются эпизоды чрезмерного кровотечения в детстве, но после полового созревания возникают лишь незначительные проблемы с кровотечением. [10]
Отсутствие прикрепления белка к ДНК, таким образом, отключает ген, который вырабатывает фактор свертывания крови IX , который предотвращает чрезмерное кровотечение. [10]
Дефицит фактора IX приводит к повышенной склонности к кровотечениям , которые могут быть как спонтанными, так и в ответ на легкую травму. [11]
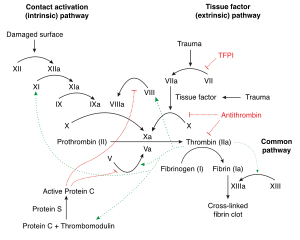
Дефицит фактора IX может вызвать помехи в каскаде коагуляции, тем самым вызывая спонтанное кровотечение при травме. Фактор IX при активации активирует фактор X , который помогает преобразованию фибриногена в фибрин . [11]
Фактор IX становится активным в конечном итоге при коагуляции кофактором фактора VIII (в частности IXa). Тромбоциты обеспечивают место связывания для обоих кофакторов. Этот комплекс (в пути коагуляции) в конечном итоге активирует фактор X. [12]
Диагностика гемофилии B может быть проведена с помощью следующих тестов/методов: [2]
Дифференциальная диагностика этого наследственного заболевания следующая: гемофилия А , дефицит фактора XI , болезнь Виллебранда , нарушения фибриногена и синдром Бернара–Сулье [10]
Лечение проводится с перерывами, когда наблюдается значительное кровотечение. Оно включает внутривенное вливание фактора IX и/или переливание крови. НПВП следует избегать после постановки диагноза, поскольку они могут усугубить кровотечение. Любая хирургическая процедура должна проводиться с сопутствующей транексамовой кислотой . [4] [13]
Этранакоген дезапарвовец (Hemgenix) был одобрен для медицинского применения в Соединенных Штатах в ноябре 2022 года. [6] Это первый препарат генной терапии, одобренный Управлением по контролю за продуктами и лекарствами США (FDA) для лечения гемофилии B. [6]
Хирургическое лечение, включая простое удаление зуба, должно быть спланировано так, чтобы свести к минимуму риск кровотечения, чрезмерного образования синяков или образования гематомы. Мягкие вакуумные шины могут использоваться для обеспечения местной защиты после удаления зуба или длительного кровотечения после удаления. [14]
В июле 2022 года были объявлены результаты кандидата на генную терапию гемофилии B под названием FLT180, который работает с использованием аденоассоциированного вируса (AAV) для восстановления белка фактора свертывания крови IX (FIX); нормальные уровни белка наблюдались при низких дозах терапии, но для снижения риска иммунных реакций, связанных с вектором, потребовалась иммуносупрессия. [15] [16] [17]

Стивен Кристмас (12 февраля 1947 г. – 20 декабря 1993 г.) был первым пациентом, у которого в 1952 году была описана болезнь Кристмаса (или гемофилия B). Кристмас родился в британской семье в Лондоне . Он был сыном кино- и телеактера Эрика Кристмаса . [18] Он эмигрировал в Торонто, Онтарио , Канада, со своей семьей и был там в возрасте двух лет, когда в Больнице для больных детей был диагностирован гемофилия . Семья вернулась в Лондон в 1952 году, чтобы навестить своих родственников, и во время поездки Стивен был госпитализирован. Образец его крови был отправлен в Оксфордский центр гемофилии в Оксфорде , где Розмари Биггс и Роберт Гвин Макфарлейн обнаружили, что у него не было дефицита фактора VIII , который обычно снижается при классической гемофилии, а другого белка, который получил название фактор Кристмаса в его честь (а позже и фактор IX ). [18] Стивен зависел от переливания крови и плазмы и был инфицирован ВИЧ в период, когда кровь не проверялась на наличие этого вируса. Он стал активным работником Канадского общества гемофилии и боролся за безопасность переливания с тех пор, как заразился, но заболел СПИДом и умер от него в 1993 году. [18]
В 1950-х и 1960-х годах, с появлением новых технологий и постепенным прогрессом в медицине, ученые-фармацевты нашли способ извлекать фактор IX из свежезамороженной плазмы (СЗП) и вводить его больным гемофилией B. Хотя они нашли способ лечения этого заболевания, СЗП содержала лишь небольшое количество фактора IX , что требовало больших количеств СЗП для лечения фактического эпизода кровотечения, в результате чего человеку требовалась госпитализация. К середине 1960-х годов ученые нашли способ получать большее количество фактора IX из СЗП. К концу 1960-х годов ученые-фармацевты нашли методы отделения фактора IX от плазмы , что позволяет аккуратно упаковывать флаконы с концентратами фактора IX. С появлением концентратов фактора IX людям стало проще получать лечение дома. [19] Хотя эти достижения в медицине оказали значительное положительное влияние на лечение гемофилии, с этим было связано много осложнений. К началу 1980-х годов ученые обнаружили, что созданные ими лекарства переносят вирусы , передающиеся через кровь , такие как гепатит и ВИЧ , вирус, вызывающий СПИД. С появлением этих смертельных вирусов ученым пришлось искать более совершенные методы скрининга продуктов крови, которые они получали от доноров. В 1982 году ученые совершили прорыв в медицине и смогли клонировать ген фактора IX . Благодаря этой новой разработке снизился риск многих вирусов. Хотя новый фактор был создан, он не был доступен для пациентов с гемофилией B до 1997 года. [ необходима цитата ]
В 2009 году анализ генетических маркеров показал, что гемофилия B является заболеванием крови, поражающим многие европейские королевские семьи Великобритании, Германии, России и Испании: так называемая «королевская болезнь». [20] [21]